















ЛЕКЦИЯ 9
Перемещение и сжатие газов (компрессоры)
Общие сведения. Термодинамические основы процесса сжатия газов
Поршневые компрессоры
Центробежные и осевые компрессорные машины
Ротационные компрессоры и газодувки
Вакуум-насосы
Ротационные компрессоры и газодувки
9.1. Общие сведения
На предприятиях химической промышленности подвергаются переработке значительные количества газов и их смесей. Сжатие газов используют для перемещения их по трубопроводам и аппаратам, создания вакуума. Сжатые газы применяют для перемешивания, распыления жидкостей и т. п. Диапазон давлений, применяемых в химических производствах, колеблется в широких пределах — от 10–8 до 103 Па.
Машины, предназначенные для перемещения и сжатия газов, называют компрессорными машинами.
Отношение конечного давления ![]() , создаваемого
компрессорной машиной, к начальному давлению
, создаваемого
компрессорной машиной, к начальному давлению ![]() , при
котором происходит всасывание газа, называется степенью сжатия.
, при
котором происходит всасывание газа, называется степенью сжатия.
В зависимости от величины степени сжатия различают следующие типы компрессорных машин:
1) вентиляторы 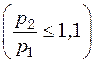 – для перемещения
больших количеств газов;
– для перемещения
больших количеств газов;
2) газодувки 1,1 < 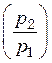 <
3,0 — для перемещения газов при относительно высоком сопротивлении газопроводящей
сети;
<
3,0 — для перемещения газов при относительно высоком сопротивлении газопроводящей
сети;
3) компрессоры 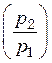 > 3,0 – для
создания высоких давлений;
> 3,0 – для
создания высоких давлений;
4) вакуум-насосы – для отсасывания газов при давлении ниже атмосферного
9.2. Термодинамические основы процесса сжатия газов
Сжатие реального газа сопровождается изменением его объема, давления и температуры. Соотношение между этими параметрами при давлении не более 1 МПахарактеризуется уравнением состояния идеальных газов.
При давлениях более 1 МПа следует пользоваться уравнением Ван-дер-Ваальса или другим уравнением, более точно описывающим зависимость между объемом, давлением и температурой газа при повышенных давлениях
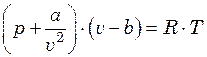 , (9.1)
, (9.1)
где ![]() –
давление газа, Па;
–
давление газа, Па; ![]() – удельный объем газа, м3/кг;
R = 8314/M – газовая постоянная, Дж/(кг·К); М –
молекулярная масса газа, кг/кмоль; а и b – величины, постоянные
для данного газа.
– удельный объем газа, м3/кг;
R = 8314/M – газовая постоянная, Дж/(кг·К); М –
молекулярная масса газа, кг/кмоль; а и b – величины, постоянные
для данного газа.
Величины а и b могут быть рассчитаны по критическим параметрам газа (Ткр и ркр):
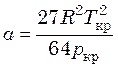 ;
; 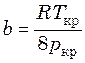 . (9.2)
. (9.2)
Однако на практике для определения параметров газа при различных его состояниях чаще пользуются термодинамическими диаграммами: Т–S (температура–энтропия), p–i (зависимость давления от энтальпии), p–V (зависимость давления от объема).
|
Рисунок 4.1 – Т–S диаграмма |
На диаграмме Т–S (рис. 9.1) линия АKВ представляет собой пограничную кривую, которая делит диаграмму на отдельные области, соответствующие определенным фазовым состояниям вещества. Область, расположенная слева от пограничной кривой, представляет собой жидкую фазу, справа – область сухого пара (газа). В области, ограниченной кривой АВK и осью абсцисс, одновременно сосуществуют две фазы – жидкость и пар. Линия АK соответствует полной конденсации пара, здесь степень сухости x = 0. Линия KВ соответствует полному испарению, x = 1. Максимум кривой соответствует критической точке K, в которой возможны все три состояния вещества. Помимо пограничной кривой на диаграмму нанесены линии постоянных температур (изотермы, Т = const) и энтропии (S = const), направленные параллельно осям координат, изобары (p = const), линии постоянных энтальпий (i = const). Изобары в области влажного пара направлены так же, как и изотермы; в области перегретого пара они меняют направление круто вверх. В области жидкой фазы изобары почти сливаются с пограничной кривой, так как жидкости практически несжимаемы.
Все параметры газа на диаграмме Т–S отнесены к 1 кг газа.
Процессы сжатия газов. Конечное давление газа при сжатии зависит от условий теплообмена газа с окружающей средой. Теоретически возможны два предельных случая сжатия:
1) изотермический процесс – все выделяющееся при сжатии тепло полностью
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.