


























2 Cпециальная часть
2.1 Металлургические расчёты
2.1.1 Расчёт материального баланса процесса разложения германиевого концентрата
Исходный состав концентрата принимаем по данным заводской практики[8] и сводим в таблицу. Расчет процесса разложения германиевого концентрата проводится по технологической схеме, представленной на рисунке 2.1.
Таблица 2.1 – Вещественный состав германиевого концентрата, %:
|
Ge |
Na |
Ca |
Fe |
Al |
As |
Zn |
Pb |
SiO2 |
Прочие |
|
13,54 |
1,51 |
4,55 |
7,61 |
8,45 |
4,75 |
5,81 |
0,30 |
13,28 |
40,20 |
Минералогический состав концентрата выглядит следующим образом:
Ge содержится в виде GeO2, Na2O·GeO2, CaO·GeO2 и FeO·GeO2 в соотношении 0,82 : 0,04 : 0,08 : 0,06;
Ca – в виде CaO·GeO2 и CaSO4;
Fe – в виде FeO·GeO2 и Fe2O3;
Na – в виде NaO·GeO2 и Na2O;
Al – в виде Al2O3;
As –в виде As2O3;
Zn – в виде ZnO;
Pb – в виде PbO;
По данным о составе концентрата проводим расчет рационального состава германиевого концентрата.
Расчет ведем на 100 кг концентрата.
1. Определяем количество GeO2 в концентрате:
(mGe)GeO2 = (mGe)к-т · 0,82 = 13,54 · 0,82 = 11,1 кг
mGeO2 = (mGe)GeO2 · М GeO2 / AGe = 11,1 · 104,59 / 72,59 = 15,99 кг
(mO2)GeO2 = mGeO2 – (mGe)GeO2 = 15,99 – 11,1 = 4,89 кг
2. Определяем количество Na2O·GeO2 в концентрате:
(mGe)Na2O·GeO2 = (mGe)к-т · 0,04 = 13,54 · 0,04 = 0,54 кг
mNa2O·GeO2 = (mGe)Na2O·GeO2 · МNa2O·GeO2 /AGe = 0,54 · 166,57 / 72,59 =
= 1,24 кг
(mNa)Na2O·GeO2 = mNa2O·GeO2 · 2ANa / МNa2O·GeO2 = 1,24 · 2 · 22,99 / 166,57 =
= 0,34 кг
(mO2)Na2O·GeO2 = mNa2O·GeO2 – (mGe)Na2O·GeO2 – (mNa)Na2O·GeO2 = 1,24 – 0,54 –
– 0,34 = 0,36 кг
3. Определяем количество CaO·GeO2 в концентрате:
(mGe)CaO·GeO2 = (mGe)к-т · 0,08 = 13,54 · 0,08 = 1,08 кг
mCaO·GeO2 = (mGe)CaO·GeO2 · МCaO·GeO2 / AGe = 1,08 · 160,67 / 72,59 = 2,39 кг
(mCa)CaO·GeO2 = mCaO·GeO2 · ACa / МCaO·GeO2 = 2,39 · 40,08 / 160,67 = 0,6 кг
(mO2)CaO·GeO2 = mCaO·GeO2 – (mGe)CaO·GeO2 – (mCa)CaO·GeO2 = 2,39 – 1,08 –
– 0,6 = 0,71 кг
4. Определяем количество FeO·GeO2 в концентрате:
(mGe)FeO·GeO2 = (mGe)к-т · 0,06 = 13,54 · 0,06 = 0,81 кг
mFeO·GeO2 = (mGe)FeO·GeO2 · МFeO·GeO2 / AGe = 0,81 · 176,44 / 72,59 = 1,97 кг
(mFe)FeO·GeO2 = mFeO·GeO2 · AFe / МFeO·GeO2 = 1,97 · 55,85 / 176,44 = 0,62 кг
(mO2)FeO·GeO2 = mFeO·GeO2 – (mGe)FeO·GeO2 – (mFe)FeO·GeO2 = 1,97 – 0,81 –
– 0,62 = 0,54 кг
5. Определяем количество CaSO4 в концентрате:
(mCa)CaSO4 = (mCa)к-т – (mCa)CaO·GeO2 = 4,55 – 0,6 = 3,95 кг
mCaSO4 = (mCa)CaSO4 · МCaSO4 / ACa = 3,95 · 136,14 / 40,08 = 13,42 кг
(mS)CaSO4 = mCaSO4 · AS / МCaSO4 = 13,42 · 32,06/ 136,14 = 3,16 кг
(mO2)CaSO4 = mCaSO4 – (mCa)CaSO4 – (mS)CaSO4 = 13,42 – 3,95 – 3,16 = 6,31 кг
6. Определяем количество Fe2O3 в концентрате:
(mFe)Fe2O3 = (mFe)к-т – (mFe)FeO·GeO2 = 7,61 – 0,62 = 6,99 кг
mFe2O3 = (mFe)Fe2O3 / 2AFe · МFe2O3 = 6,99 · 159,70 / 2 · 55,85 = 10,0 кг
(mO2)Fe2O3 = mFe2O3 – (mFe)Fe2O3 = 10,0 – 6,99 = 3,01 кг
7. Определяем количество Na2O в концентрате:
(mNa)Na2O = (mNa)к-т – (mNa)Na2O·GeO2 = 1,51 – 0,34 = 1,17 кг
mNa2O = (mNa)Na2O · МNa2O / 2ANa = 1,17 · 61,98 / 2 · 22,99 = 1,58 кг
(mO2)Na2O = mNa2O – (mNa)Na2O = 1,58 – 1,17 = 0,41 кг
8. Определяем количество Al2O3 в концентрате:
mAl2O3 = (mAl)Al2O3 · МAl2O3 / 2AAl = 8,45 · 101,96 / 2 · 26,98 = 15,97 кг
(mO2)Al2O3 = mAl2O3 – (mAl)Al2O3 = 15,97 – 8,45 = 7,52 кг
9. Определяем количество As2O3 в концентрате:
mAs2O3 = (mAs)As2O3 · МAs2O3 / 2AAs = 4,75 · 197,84 / 2 · 74,92 = 6,28 кг
(mO2)As2O3 = mAs2O3 – (mAs)As2O3 = 6,28 – 4,75 = 1,53 кг
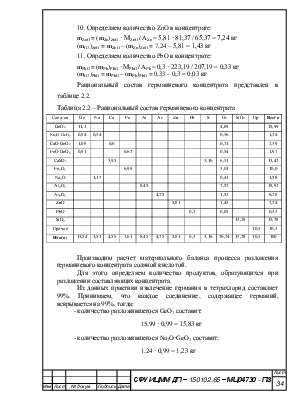
10. Определяем количество ZnO в концентрате:
mZnO = (mZn)ZnO · МZnO / AZn = 5,81 · 81,37 / 65,37 = 7,24 кг
(mO2)ZnO = mZnO – (mZn)ZnO = 7,24 – 5,81 = 1,43 кг
11. Определяем количество PbO в концентрате:
mPbO = (mPb)PbO · МPbO / APb = 0,3 · 223,19 / 207,19 = 0,33 кг
(mO2)PbO = mPbO – (mPb)PbO = 0,33 – 0,3 = 0,03 кг
Рациональный состав германиевого концентрата представлен в таблице 2.2.
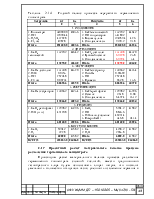
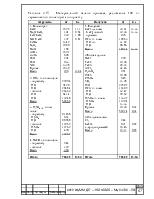
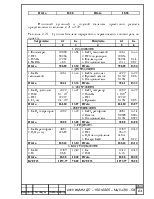
Таблица 2.2 – Рациональный состав германиевого концентрата
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.