Наряду с этим, надо выделить причины, связанные с инструментальными особенностями проведения спектроскопических экспериментов.
Поэтому в спектроскопии принято для каждого исследуемого вещества экспериментально проверять выполнение закона Бугера-Ламберта-Бэра. С этой целью проводят измерения оптической плотности на фиксированной длине волны для ряда растворов с различной концентрацией. По полученным данным строится калибровочный график зависимости Dλ от С, по которому судят о наличии пропорциональности. В идеальном случае точки на графике должны попадать на прямую, проходящую через начало координат. Тангенс угла наклона этой прямой и есть коэффициент экстинкции исследуемого вещества.
Кроме того, немаловажное значение для точности эксперимента имеет и используемый диапазон оптических плотностей. Многие современные спектрофотометры позволяют измерять оптическую плотность в пределах 0 < D < 4, однако, точность полученных значений будет существенно различаться в разных точках этого диапазона.
Анализ спектров многокомпонентных систем
Анализ спектров поглощения многокомпонентных смесей является достаточно сложной задачей. Поэтому в качестве простейшего примера рассмотрим ситуацию, когда в растворе содержится два вида частиц А и В. При этом накладывается условие, что эти частицы поглощают свет в исследуемой области спектра и могут превращаться друг в друга в результате необратимой или обратимой химической реакции (например, изомеризация, комплексообразование и т. д.). Кроме того, их концентрации связаны отношением СА + CВ = С0 = const. Тогда по спектру поглощения можно определить значения САи СВ. Правда, для проведения анализа требуется, чтобы спектры этих частиц существенно отличались в некоторой области длин волн.
Предположим, что в выбранной спектральной области спектры определяемых веществ совершенно не перекрываются. Тогда рабочую длину волны следует выбрать так, чтобы одно вещество не имело на ней поглощения, а второе поглощало бы максимально. В этом случае по известному значению С0и оптической плотности на выбранной длине волны Dλлегко определяется концентрация каждой из частиц.
Рассмотрим более сложную ситуацию, когда спектры обеих частиц полностью перекрываются. В этом случае в качестве рабочей длины волны следует выбрать область, где бы коэффициенты экстинкции εAи εBразличались максимально. Выражение для оптической плотности двухкомпонентной системы на данной длине волны записывается как
Dλ = l · (εACA + εBCB).
Поскольку суммарная концентрация частиц С0 поддерживается постоянной, то это выражение можно переписать в виде
Dλ = l · (εBC0 + (εA – εB)· CA).
Как видно из этой формулы, если при некоторой длине волны λ* коэффициенты экстинкции обеих поглощающих форм равны (εA = εB), то оптическая плотность на данной длине волны Dλ* определяется только начальной концентрацией частиц С0 и не зависит от соотношения равновесных форм. Поэтому спектральные кривые растворов любого состава будут пересекаться в одной точке, которая называется изобестической.
Наличие на спектрах поглощения одной или нескольких изобестических точек является хорошим критерием, позволяющим судить о наличии в растворе равновесия.
Точность анализа смеси также зависит от правильного выбора рабочей длины волны и будет тем выше, чем больше значение производной:
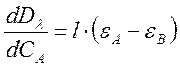 .
.
При заданной толщине кюветы l чувствительность растет с увеличением разницы (εA - εB),достигая максимального значения в точках, где эта разница принимает наибольшее значение. Такие точки называют характеристическими.
Применение спектроскопии для анализа кислотно-основных равновесий. Определение степени диссоциации слабой кислоты
Анализ кислотно-основных равновесий в растворах является одной из наиболее важных областей приложения спектроскопии в физической химии.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.