Ниже приведен возможный механизм протекания конденсации анилина с полухлористой серой. Образование незамещеннй соли наблюдалось в этой реакции и ранее [9].
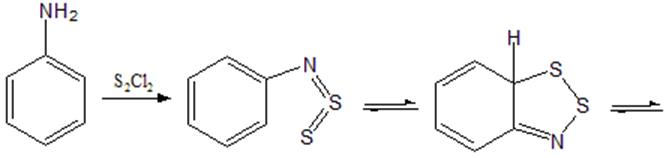
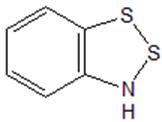
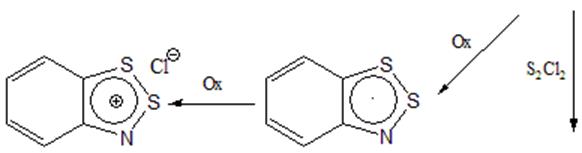
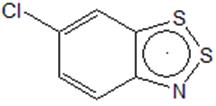
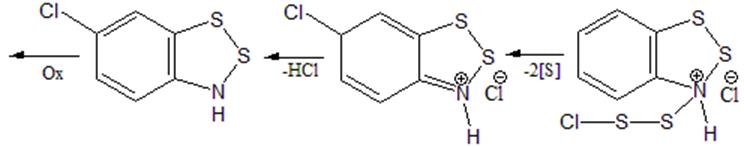
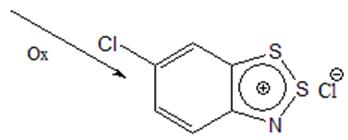
Схема 11
Для реакции с малононитрилом использовали наиболее чистый образец. Продукт был получен в соответствии с уравнением реакции, представленной на схеме 1.
(6H-1,2,3-Бензодитиазол-6-илиден)пропандинитрил, выделенный из реакционной смеси хроматографией, при перекристаллизации дал чернильно-синие кристаллы. Растворы продукта имеют насыщенную синюю окраску. При перекристаллизации из толуола было замечено, что вещество растворяется, но медленно, что привело к тому, что при охлаждении продукт не выкристаллизовывался, и часть растворителя была упарена.
ЯМР-спектр полученного вещества 2 немного отличается от литературных данных, вследствие использования другого растворителя при снятии спектра. Был использован менее полярный растворитель (CDCl3 вместо ДМСО-d6), что привело к некоторому смещению сигналов и их сближению и получению спектра второго порядка. В спектре наблюдаются мультиплеты при 7.61-7.59 м.д. (2Н, предположительно Н-4 и Н-5) и при 7.56 м.д. (предположительно Н-7). Литературные данные: 7.88, 7.82, 7.50, м.д.[3].
Полученный продукт плавится при температуре 288-290ºС, что немного выше литературных данных (283-285 ºС) [3].
5 Выводы
1. При реакции анилина с полухлористой серой получается основным продуктом является хлорид 6-хлоро-1,2,3-бензодитиазолия, однако образуется и незамещенная по положению 6 соль.
2. При реакции полученной соли Херца с малононитрилом был выделен продукт, охарактеризованный по данным спектрального анализа, а также температуре плавления как (6H-1,2,3-бензодитиазол-6-илиден)пропандинитрил.
Список литературы
1. Стрелец Б.Х., Эфрос Л.С. О строении бензотиазатиониевых соединений (соединений Герца) и продуктов их гидролиза // Журнал органической химии. − 1969. − Т.5, №1. − С. 153−158.
2. Warburton W. K. Arylthiazathiolium salts and o-aminoaryl thiols. The Herz reaction. // Chemical reviews. − 1957. − V. 57, № 5. − P. 1011−1020.
3. Koutentis P. A., Rees C. W. Reaction of Herz salts with malononitrile: a general route to (6H-1,2,3-benzodithiazol-6-ylidene)malononitriles // J. Chem. Soc.. − 2002. − № 1. − P. 315−319.
4. Стрелец Б.Х., Эфрос Л.С. К вопросу о механизме хлорирования в реакци Герца // Химия гетероциклических соединений. − 1969. − № 3. − С. 565–566.
5. Акулин Ю. И., Гельмонт М.М., Стрелец Б.Х., Эфрос Л.С. Строение и реакционная способность солей бензо-1,2,3-дитиазолия и их селенистых аналогов // Химия гетероциклических соединений. − 1978. − №7. − С. 912−916.
6. Стрелец Б.Х., Эфрос Л.С., Тодрес З.В. К вопросу об ориентации и механизме реакции ароматических аминов с полухлористой серой // Химия гедероциклических соединений. − 1970. − № 3. − С. 351−354.
7. Стрелец Б.Х., Эфрос Л.С., Акулин Ю. И. Реакция солей бензо-1,2,3-дитиазолия с ароматическими аминами // Химия гетероциклических соединений. − 1976. − №2. − С. 183−185.
8. Акулин Ю. И., Стрелец Б.Х., Эфрос Л.С. Реакции солей бензо-1,2,3-дитиазолия и их селенистых аналогов с аминами // Химия гетероциклических соединений. − 1977. − №11. − С. 1499−1502.
9. Mayer R. S,N. Compounds via amines and sulfur halides // Phosph. Sulf. − 1985. − V. 23. − P. 277 − 296.
10. Тодрес З.В., Стрелец Б.Х., Эфрос Л.С. Исследование в области ароматических гетероциклов. Об особенностях строения соединений ряда дегидро-1,2,3-бензодитиазолийхлорида // Химия гетероциклических соединений. − 1971. − №8. − С. 1043−1047.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.