


Теория на экзамене 15 января 2000 года, группы 741, 742, 643
1. (400) Линейный и квадратичный эффекты Штарка. (После теоретической части проиллюстрировать определением изменения энергии 1s орбитали атома водорода в однородном электрическом поле E).
Решение: В первом порядке теории возмущений DE(1) = <1s|-eEz|1s> = 0 из-за равенства нулю угловой части интеграла <Y00|Y10|Y00> = 0. Во втором порядке теории возмущений в соответствии с правилами отбора
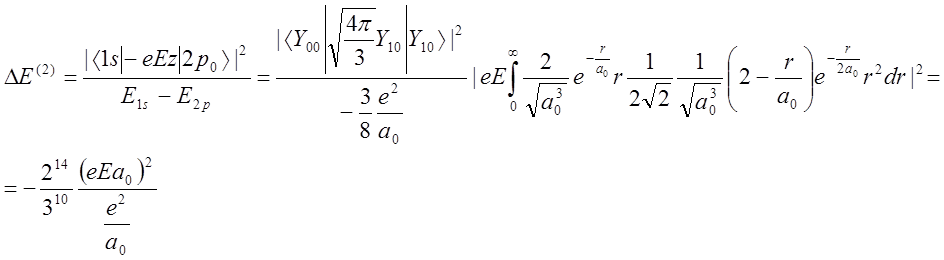 Таким образом,
во втором порядке теории возмущений энергия 1s-орбитали понизится за счет отталкивания от 2p0 орбитали.
Таким образом,
во втором порядке теории возмущений энергия 1s-орбитали понизится за счет отталкивания от 2p0 орбитали.
2. (300) Классификация термов и нахождение основного терма линейных молекул. (После теоретической части проиллюстрировать определением основного терма линейного радикала Н-Сl-Н).
Решение: Основной терм радикала Н-Сl-Н - 2Pu.
3. (500) Теория представлений, неприводимые представления, таблицы характеров. (После теоретической части проиллюстрировать построением таблицы характеров для D3d группы).
|
|
Решение: Группа D3d - это два развернутых на 600 правильных треугольника с параллельными плоскостяси и с разнесенными центрами на одной оси. После этого определения можно перечислить операции симметрии и составить таблицу характеров.
|
D3d |
E |
2C3 |
3C2' |
I |
2S6 |
3sv |
|
A1' |
1 |
1 |
1 |
1 |
1 |
1 |
|
A2' |
1 |
1 |
1 |
-1 |
-1 |
-1 |
|
A1'' |
1 |
1 |
-1 |
1 |
1 |
-1 |
|
A2'' |
1 |
1 |
-1 |
-1 |
-1 |
1 |
|
E' |
2 |
-1 |
0 |
2 |
-1 |
0 |
|
E'' |
2 |
-1 |
0 |
-2 |
1 |
0 |
4. (400) Свойства альтернантных p-систем. (После теоретической части показать, что p-электронный заряд на всех центрах в альтернантных системах равен единице).
5. (400) Определение стабильности p-систем: молекулы, радикалы.
Задачи на экзамене 15 января 2000 года, группы 741, 742, 643
1. (200) За счет спин-орбитального взаимодействия полное расщепление терма 2S+1L (расстояние между мультиплетами с максимальным и минимальным значениями J) равно 14l. Определить величины S и L.
Решение: Полное расщепление равно DE = lS(2L+1). Учитывая, что L - целое число, а S - целое или полуцелое, можно определить, что S = 2 и L = 3.
2. (500) Определить расщепление уровней (функции и энергии) возбужденного состояния атома водорода с главным квантовым числом 2 в слабом внешнем магнитном поле.
Решение: Электрон может находится на 4-х вырожденных орбиталях 2s, 2p1, 2p0, 2p-1. Если он находится на 2s орбитали реализуется терм 2S1/2. При нахождении на 2p орбиталях возникают термы 2P3/2 и 2P1/2, функции которых легко определяются. Определение g-факторов позволяет определить расщепление этих термов в магнитном поле.
|
Терм |
MJ |
g-фактор |
Энергия |
Функция |
|
2P3/2 |
3/2 |
4/3 |
2bH |
2p1a |
|
2S1/2 |
1/2 |
2 |
bH |
2sa |
|
2P3/2 |
1/2 |
4/3 |
(2/3)bH |
|
|
2P1/2 |
1/2 |
2/3 |
(1/3)bH |
|
|
2P1/2 |
-1/2 |
2/3 |
-(1/3)bH |
|
|
2P3/2 |
-1/2 |
4/3 |
-(2/3)bH |
|
|
2S1/2 |
-1/2 |
2 |
-bH |
2sb |
|
2P3/2 |
-3/2 |
4/3 |
-2bH |
2p-1b |
|
|
|
|
3. (300) Определить центр, на котором существует максимальная и минимальная спиновые плотности, и определить их величины для p-радикала, строение которого показано на рисунке.
Решение: На втором рисунке указана нумерация звездчатых центров. Спиновая плотность:
r10 = 0, r9 = r11 = r14 = r15 = r16 = r17 = 1/112, r1 = r6 = r7 = r8 = r12 = r13 = 4/112, r2 = r5 = 16/112, r3 = r4 = 25/112.
4. (300) Определить разложение на неприводимые представления симметричной части прямых произведений [P´P]s и [D´D]s группы С¥v.
Решение: Ниже в таблице представлены строчки
характеров представлений из которых следует, что [P´P]s = S+ + D и [D´D]s = S+ + G. Необходимо
использовать формулу 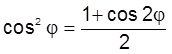 . Операция R2 при нахождении строчки характеров [P´P]s и [D´D]s для Сj
равна С2j.
. Операция R2 при нахождении строчки характеров [P´P]s и [D´D]s для Сj
равна С2j.
|
С¥v |
E |
2Cj |
........ |
¥sv |
|
S+ |
1 |
1 |
..... |
1 |
|
S- |
1 |
1 |
..... |
-1 |
|
P |
2 |
2cosj |
..... |
0 |
|
D |
2 |
2cos2j |
..... |
0 |
|
[P´P] = S+ + S- + D |
4 = 1 + 1 + 2 |
4cos2j = 1 + 1 + 2cos2j |
..... |
0 = 1 + (-1) + 0 |
|
[P´P]s = S+ + D |
3 = 1 + 2 |
1 + 2cos2j = 1 + 2cos2j |
..... |
1 = 1 + 0 |
|
[D´D] = S+ + S- + G |
4 = 1 + 1 + 2 |
4cos22j = 1 + 1 + 2cos4j |
..... |
0 = 1 + (-1) + 0 |
|
[D´D]s = S+ + G |
3 = 1 + 2 |
1 + 2cos22j = 1 + 2cos4j |
..... |
1 = 1 + 0 |
5. (400) Рассмотреть предпочтительное направление присоединения атома H к пентадиенильному p-радикалу.
Решение: Направление присоединения определяется меньшей энергией оставшейся p-системы. При присоединении атома Н к первому (концевому) атому углерода остается p-система бутадиена, энергия которой равна 4a + 4.44b. Присоединение ко второму центру оставляет один изолированный p-центр и аллильный радикал, энергии которых равны 4a + 2.82b. При присоединении по центральному (третьему) атому углерода остаются две этиленовые p-системы с энергией 4a + 4b. Таким образом, присоединение наиболее эффективно по первому центру, затем по третьему и наимене эффективно по второму.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.