
ЦЕЛЬ РАБОТЫ: изучение ЭДС гальванических элементов и потенциалы отельных элементов, термодинамические процессы, протекающие при работе гальванического элемента.
Источники постоянного тока, в которых электрическая энергия получается за счет энергии химической реакции, называются гальваническими элементами. Гальванический элемент состоит из положительного и отрицательного электродов. Электрод представляет собой электрохимическую систему, состоящую из двух фаз. На границе раздела фаз протекает электродный процесс, в результате которого происходит переход электрических зарядов из одной фазы в другую. Каждая фаза при этом приобретает свой электрический заряд. На границе их раздела создается двойной электрический слой, которому соответствует скачек потенциала.
В зависимости от характера и природы соприкасающихся сред различают контактный потенциал, диффузионный потенциал и потенциал на границе раздела твердой и жидкой фаз.
Контактная разность потенциалов возникает на границе соприкосновения 2-х металлов за счет перехода электронов из одного металла в другой. Из двух соприкасающихся металлов положительно заряжается тот, работа выхода электронов из которого меньше.
По свойствам веществ, участвующих в электронной реакции, по природе потенциалопределяющих ионов принята следующая классификация электродов: электроды первого рода, второго рода, газовые, окислительно-восстановительные и ионоселективные электроды.
Электроды первого рода – это электроды, обратимые или к катиону или к аноду. Обратимы по отношению к катиону (аниону) – это значит, что потенциал определяющими ионами являются катионы (анионы). От их активности (концентрации) зависит величина электродного потенциала.
Электродами второго рода называются электроды обратимые относительно катиона и аниона. В потенциалопределяющей реакции на этом электроде принимают участие как катионы, так и анионы.
Газовый электрод представляет собой систему, состоящую из инертного металлического проводника, погруженного в раствор, содержащий одноименные ионы с газом и насыщенный им под давлением.
Химическими элементами называются электрохимические цепи, состоящие из 2-х электродов, отличающихся по физическим и химическим свойствам, потенциалопределяющие реакции их различны.
Концентрационными называются гальванические элементы, состоящие из 2-х электродов одинаковых по физическим, химическим свойствам и природе электродной реакции, погруженных в одинаковые растворы различной концентрации (активности).
|
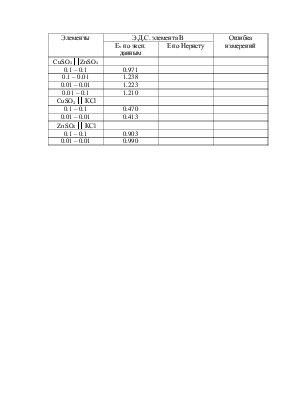
Элементы |
Э.Д.С. элемента В |
Ошибка измерений |
|
|
Ех по эксп. данным |
Е по Нернсту |
||
|
CuSO4 ïïZnSO4 |
|||
|
0.1 – 0.1 |
0.971 |
||
|
0.1 – 0.01 |
1.238 |
||
|
0.01 – 0.01 |
1.223 |
||
|
0.01 – 0.1 |
1.210 |
||
|
CuSO4 ïï КСl |
|||
|
0.1 – 0.1 |
0.470 |
||
|
0.01 – 0.01 |
0.413 |
||
|
ZnSO4 ïï КСl |
|||
|
0.1 – 0.1 |
0.903 |
||
|
0.01 – 0.01 |
0.990 |
||
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.