Лабораторная работа 21
Изучение зависимости коэффициента вязкости жидкости от температуры.
Механизмы вязкости в газах и жидкостях существенно отличаются. В жидкостях расстояние между молекулами значительно меньше, чем в газах. Поэтому на движение молекул в жидкостях, в первую очередь, влияет межмолекулярное взаимодействие, ограничивая их подвижность. Вязкость жидкостей значительно больше, чем у газов и уменьшается с ростом температуры (у газов наоборот).
Молекулы жидкости могут совершать малые колебания лишь в пределах, ограниченных межмолекулярными расстояниями. Однако время от времени колеблющаяся молекула в результате флуктуации может получить от соседних молекул избыточную энергию, достаточную для того, чтобы совершить скачок на некоторое расстояние. В новом месте частица проведет некоторое время t, совершая колебания, пока снова не получит в результате флуктуации, нужную для скачка энергию; она вновь совершит скачок, и т. д. Такие колебания, сменяющиеся скачками – это и есть тепловые движения молекул жидкости. По образному выражению Френкеля Я.И., молекулы в жидкости ведут кочевой образ жизни, при котором кратковременные переезды сменяются относительно длительными периодами «оседлой» жизни. Среднее время t «оседлой» жизни молекул называется временем релаксации. Оно зависит от температуры. С повышением температуры t очень быстро уменьшается, что обуславливает увеличение подвижности молекул жидкости и, соответственно, уменьшение вязкости.
Для того, чтобы молекула жидкости перескочила из одного положения равновесия в другое, она должна нарушить связи с соседними молекулами. Для этого требуется затратить некоторую энергию W, т.е. молекула должна преодолеть потенциальный барьер высотой W. Величина W называется энергией активации.
Длительность пребывания молекулы в данном месте жидкости определяется вероятностью для молекулы получить энергию W, достаточную для скачка. А эта вероятность выражается законом Больцмана
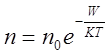
Здесь n-число молекул в единице объёма, энергия которых равна W, n0 – число молекул в единице объёма с энергией W= 0.
Чем
больше вероятность получения молекулой энергии W, тем
меньше будет время «оседлости» t, т.е. 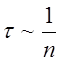 . Поэтому для среднего времени релаксации
можно написать выражение
. Поэтому для среднего времени релаксации
можно написать выражение
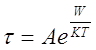 .
.
Множитель А имеет смысл периода колебания молекулы.
Очевидно, что жидкость будет тем более текучей (с тем меньшей вязкостью), чем меньше время t«оседлости» молекул и , значит, чем чаще происходит скачок.
Эти соображения приводят к выражению для коэффициента вязкости, называемому уравнением Френкеля-Андраде
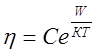 (1)
(1)
Множитель С, входящий в это выражение, зависит от рода жидкости, частоты колебаний молекул и температуры (~Т). При обычных температурах (kТ<W) из формулы (1) следует, что вязкость жидкости уменьшается с повышением температуры (в противоположность газам). Однако при достаточно больших температурах, когда kТ>W, вязкость начинает возрастать с температурой (как у газов).
Прологарифмируем формулу (1)
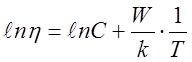 (2)
(2)
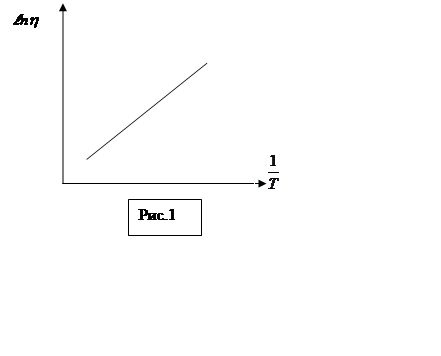
График зависимости ![]() от
от ![]() представляет
собой прямую (рис.1). Из наклона этой прямой можно определить энергию активации
W.
представляет
собой прямую (рис.1). Из наклона этой прямой можно определить энергию активации
W.
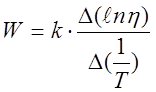 (3)
(3)
k – постоянная Больцмана.
Это энергия активации для одной молекулы.
Энергия активации в расчёте на один моль жидкости
WМ = W·NА, NА- число Авогадро.
По справочным данным для водыWМ »16 Дж/моль.
В данной работе экспериментально определяется коэффициент вязкости воды при различных температурах и на основе этих измерений определяется энергия активации.
Экспериментально коэффициент вязкости измеряется вискозиметром с падающим шариком (метод Стокса).
На шарик действуют три силы: сила тяжести Р,
направленная вниз; сила внутреннего трения ![]() и
выталкивающая сила Fв,
направленные вверх. Шарик сначала падает ускоренно, но затем очень быстро
наступает равновесие, т.е.
и
выталкивающая сила Fв,
направленные вверх. Шарик сначала падает ускоренно, но затем очень быстро
наступает равновесие, т.е.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.