

Глава 6. ПРОСТАГЛАНДИНЫ. ЛЕЙКОТРИЕНЫ
Простагландины, лейкотриены, а также тромбоксаны, эпоксиды, липоксины и гидроксипероксины относятся к эйкозаноидам (от греч. еicosa – двадцать) - короткодействующим высокоактивным клеточным медиаторам – «местным» гормонам. Почти все они являются жирными кислотами, продуктами метаболизма арахидоновой кислоты, содержащей 20 атомов углерода. Некоторые эйкозаноиды могут быть синтезированы из С18 жирных кислот (линолевой и a-линоленовой).
Исследования простагландинов начались в 1930 году, когда гинекологи Курцрок и Либ обнаружили, что сперма человека вызывает сокращение маточной мускулатуры. В 1934 году Гольдблат и Ван Эйлер независимо друг от друга нашли в семенной жидкости человека вазоактивную жирную кислоту, снижающую артериальное давление у кроликов. Ван Эйлер назвал это вещество простагландином, так как считал, что оно образуется простатой. Структура первых двух простагландинов была определена в 1962 году Бергстрёмом, который назвал их простагландинами F и Е соответственно их способности растворяться в фосфатном буфере или эфире.
Всего известно 10 групп специфических молекул простагландинов, получивших буквенные индексы от А до J. Каждая группа простагландинов состоит из трех серий под номером 1, 2 или 3, определяющим степень насыщения (количество двойных связей) алифатической боковой цепи. Для простагландина F дополнительное обозначение a или b характеризует пространственную конфигурацию гидроксильной группы при С9. Простагландины G2 и Н2 нестабильны и служат предшественниками для дальнейшего синтеза эйкозаноидов (так же, как и 5-, и 15-гидроксиэйкозатетраенаты).
Эйкозаноиды не депонируются в клетке, их синтез регулируется активностью микросомальных ферментов и содержанием субстрата для синтеза – свободных жирных кислот:
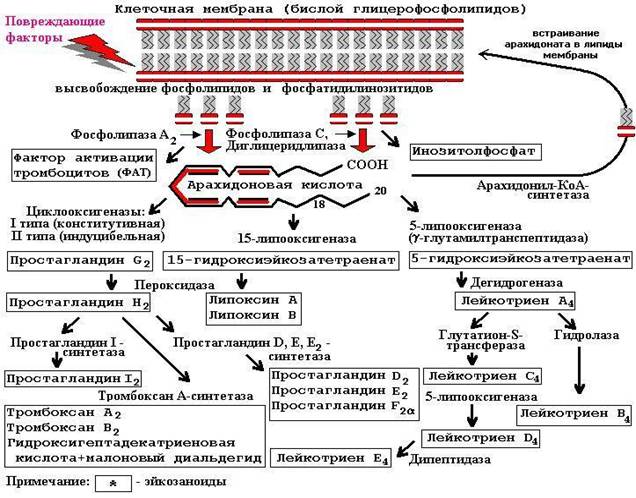
Рисунок 6.1. Схема синтеза эйкозаноидов.
Ферменты синтеза эйкозаноидов являются тканеспецифичными. Например, в эндотелиальных клетках сосудов синтезируются простагландины Е2 и I2 (простациклин), а в тромбоцитах – тромбоксаны.
При расщеплении фосфолипазой А2 фосфолипидов клеточных мембран образуются арахидоновая кислота и фактор активации тромбоцитов – сильный патофизиологический медиатор бронхоспазма и шока. Ингибиторами фосфолипазы А2 являются глюкокортикостероиды – гидрокортизон, преднизолон, дексаметазон и другие (см. раздел «Гормоны коры надпочечников и их синтетические аналоги»), оказывающие наиболее мощный противовоспалительный эффект.
Синтез простагландинов катализируется гемопротеидом циклооксигеназой (ЦОГ, СОХ, эндопероксид-простагландин Н2-синтаза), которая имеется у большинства животных и обнаружена во всех клетках человека, кроме эритроцитов и лимфоцитов.
Блокаторами циклооксигеназного пути окисления арахидоната являются НПВС (см. разделы «Ненаркотические анальгетики» и «Противовоспалительные средства»), например, ацетилсалициловая кислота (необратимый ингибитор ЦОГ), диклофенак, индометацин, нимесулид (обратимые ингибиторы ЦОГ). Все НПВС конкурентно вытесняют арахидоновую кислоту из активного центра циклооксигеназы.
Существует два типа циклооксигеназы: ЦОГ-1 и ЦОГ-2. Эти изоферменты отличаются по химическому составу (на 4 аминокислоты), и по локализации в организме. В организме доминирующей формой, обеспечивающей выработку защитных факторов в ЖКТ, регулирующей тонус бронхов и гемостаз, является постоянно активная (конститутивная) форма - ЦОГ-1.
Экспрессия гена ЦОГ-2 активируется кининами только при массивном повреждении клеточных мембран, продукты ее катализа (простагландины Е2, F2a и I2) запускают болевую и воспалительную реакцию. Экспрессия ЦОГ-2 в очаге воспаления, в путях проведения болевых импульсов (в спинном мозге), и в центре терморегуляции (в гипоталамусе) может быть ослаблена глюкокортикостероидными гормонами и нимесулидом.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.