Кремний, германий, многие диэлектрические и слабопроводящие минералы, некоторые металлургические шлаки имеют слабый металлический блеск в отраженном свете и непрозрачны. При малой толщине (менее 0,01 см) эти вещества частично или полностью прозрачны, например, тонкие слои кремния пропускают излучение красной области видимого света и инфракрасное излучение. Металлический блеск и вообще состав отраженного спектра объясняется наличием в металлах свободных электронов, легко рассеивающих энергию поглощенной электромагнитной волны уже в тонком поверхностном слое. Глубина проникновения волн в металлы
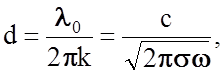 (2.4.21)
(2.4.21)
где k - комплексная часть показателя преломления для излучения с длиной волны l0, c - скорость света, s - удельная проводимость вещества. Например, излучение с длиной волны l = 500 нм, соответствующее примерно середине видимого диапазона, проникает в алюминий на глубину около 0,1 мм и рассеивается в виде ленц-джоулева тепла.
Возникновение высокочастотных токов в тонком поверхностном слое металлов называется скин-эффектом. Причем лишь незначительная доля энергии падающей волны поглощается таким путем в объеме металла, если на его поверхности нет оксидных или иных пленок. Большая часть отбрасывается в окружающую среду в виде вторичных отраженных волн. Слабый металлический блеск кремния и других материалов с узкой запрещенной зоной (Е £ 1 эВ) можно объяснить взаимодействием падающей волны с электронами, переброшенными за счет энергии квантов из валентной зоны в зону проводимости.
Во многих случаях окраску бесцветных веществ создают изменением их химического состава, введением в состав инородных ионов, молекул или коллоидных частиц.
Так, чистая окись алюминия Al2O3 бесцветна. Замена 0,5% ионов Аl+3 на ионы Cr+3 приводит к получению розового или красного – в зависимости от количественного содержания примеси - рубина, а примесь Ti+3 превращает бесцветную окись алюминия в голубой сапфир (иногда сапфирами называют бесцветные технические изделия из Аl2O3). Такие красители называют ионными. Применительно к силикатному стеклу это - Fe+2/Fe+3, Mn+2/Mn+3, Co+2, Ni+2, Cr+3/Cr+6, Ti+3/Ti+4, Ce+3/Ce+4 и другие, причем цвет и интенсивность окрашивания сильно зависят не только от количества примеси, но и от ее валентности. Например, красный цвет рубина объясняется тем, что ионы Сг+3 интенсивно поглощают и рассеивают в окружающую решетку энергию квантов из зеленой части спектра. Такое же резонансное поглощение некоторых длин волн из белого видимого спектра характерно и для других ионов-красителей, совместное их применение позволяет широко варьировать декоративные качества изделий.
В соответствии с теорией Рэлея интенсивность рассеяния пропорциональна l-4; подбирая размер частиц-микрокристаллов сульфидов и селенидов в объеме стекла или ситалла (глушение) или добиваясь выделения коллоидных частичек - обычно благородных металлов, меди, селена, сурьмы - в объеме прозрачного материала, можно добиться необходимой окраски. Классические примеры здесь - получение рубинового стекла введением AuCl3 в количество 0,02...0,03% в пересчете на золото, получение желтого стекла введением серебра, глушение эмалей и глазурей применением легкоплавких стекол с добавлением тугоплавкого мелкодисперсного глушителя. Глушение может достигаться и термической обработкой, при которой в аморфном объеме возникает множество мелких выделений кристаллической фазы с иным показателем преломления.
Некоторые физические особенности в окрашивании кристаллов и аморфных материалов возникают, если изменение цвета обусловлено наличием центров окраски. Если прозрачный кристалл галоидного соединения, например, КСl, нагревать в атмосфере, содержащей пары калия, то кристаллы приобретают голубую окраску; кристаллы NaCl после нагревания в парах натрия становятся желтыми, наличием центров окраски разного типа объясняется цвет кристаллов алмаза. Простейшие центры окраски F- и V-типа являются следствием локального нарушения стехиометрии в некоторых точках объема кристалла. В частности, нагревание КСl в парах калия приводит к нарушению стехиометрии - внедряется добавочное количество атомов калия с избыточной концентрацией до 1016…1018 см-3. Нарушение стехиометрии приводит к недостатку в объеме анионов Cl-, возникают анионные вакансии, способные захватывать и удерживать электроны (рис.2.4.7). Группа атомов, содержащая внутри анионную вакансию, и представляет собой F-центр. Избыток же анионов может привести к появлению центров окраски V-типа, где катионная вакансия захватывает и удерживает дырку.
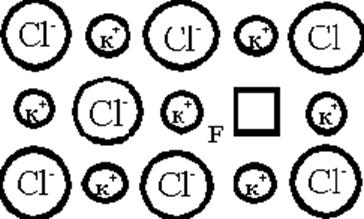 Рис.2.4.7. Схема возникновения F-центра окраски,
представляющего анионную вакансию, захватившую электрон
Рис.2.4.7. Схема возникновения F-центра окраски,
представляющего анионную вакансию, захватившую электрон
Центры окраски ведут себя подобно атомам, они способны поглощать кванты света и возбуждаться, затем, возвращаясь в нормальное состояние - испускать свет. Максимум поглощения для кристаллов КС1 соответствует энергии 2.2 эВ (l = 565 нм), для NaCl - энергии 2,7 эВ ( l = 460 нм). F- и V-центры окраски могут группироваться в комплексы и тогда их называют M- и R-центрами. Центры окраски могут образоваться и вследствие группирования вакансий при их термической диффузии, они могут быть внедрены в материалы в ходе их бомбардировки электронами, нейтронами, квантами, рентгеновского и g-излучения.
Возникновение центров окраски под действием облучения светом видимого диапазона и их диссоциация под действием термического возбуждения лежат в основе производства фотохромных стекол, способных варьировать окраску в зависимости от освещенности и температуры.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.