Графически величина ![]() изображена на рис. 58.
Максимум на кривой отвечает критическому размеру кристаллического зародыша,
который находится в обратно пропорциональной зависимости от величины переохлаждения.
Здесь понятие критического размера зародыша соответствует его размеру,
способному расти – увеличиваться в размерах. Анализируя кривую на рис. 59 можно
видеть, что если размер зародыша меньше критического r
< rкр, то увеличение радиуса «r» сопровождается возрастанием D F – свободной энергии. А
согласно одному из основных положений термодинамики все самопроизвольно
протекающие процессы характеризуются уменьшением свободной энергии.
Следовательно, если r < rкр,
то рост такого зародыша невозможен. И, напротив, если r
> rкр (нисходящая ветвь кривой),
то увеличение размера зародыша «r»
сопровождается снижением свободной энергии. Поэтому такой зародыш способен к
росту.
изображена на рис. 58.
Максимум на кривой отвечает критическому размеру кристаллического зародыша,
который находится в обратно пропорциональной зависимости от величины переохлаждения.
Здесь понятие критического размера зародыша соответствует его размеру,
способному расти – увеличиваться в размерах. Анализируя кривую на рис. 59 можно
видеть, что если размер зародыша меньше критического r
< rкр, то увеличение радиуса «r» сопровождается возрастанием D F – свободной энергии. А
согласно одному из основных положений термодинамики все самопроизвольно
протекающие процессы характеризуются уменьшением свободной энергии.
Следовательно, если r < rкр,
то рост такого зародыша невозможен. И, напротив, если r
> rкр (нисходящая ветвь кривой),
то увеличение размера зародыша «r»
сопровождается снижением свободной энергии. Поэтому такой зародыш способен к
росту.
Изложенная логика процесса кристаллизации приводит к тупиковому выводу, так называемому термодинамическому парадоксу кристаллизации. Суть парадокса состоит в том, что кристаллический зародыш размером меньше критического не может расти, но чтобы зародыш достиг критического размера он должен пройти процесс перехода от малого размера к большему, т.е. процесс роста.
Возникший термодинамический парадокс кристаллизации разрешается вероятностным законом (статистическая природа). Статистически на основе неравномерности флуктуаций образуются при определенном переохлаждении зародыши разных размеров, в том числе некоторые из зародышей будут иметь размеры больше критического. И эти кристаллические зародыши будут расти, и увеличиваться в размерах.
Таким образом, процесс зарождения центров кристаллизации рассматривается как вероятностный процесс. Скорость кристаллизации как вероятность существования флуктуаций с размерами больше rкр описывается выражением:
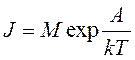 , где А – работа образования кристаллического зародыша; k – постоянная Больцмана; М – величина,
характеризующая обмен между атомами жидкой и твердой фаз, т.е. рост
кристаллических зародышей:
, где А – работа образования кристаллического зародыша; k – постоянная Больцмана; М – величина,
характеризующая обмен между атомами жидкой и твердой фаз, т.е. рост
кристаллических зародышей:
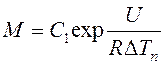 , здесь С1 – множитель, численно равный числу
атомов в мольном объеме расплава: С1 = 1023; U – энергия активации.
, здесь С1 – множитель, численно равный числу
атомов в мольном объеме расплава: С1 = 1023; U – энергия активации.
Работа образования кристаллического зародыша выражается:
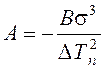 .
.
В окончательном виде скорость кристаллизации представляется:
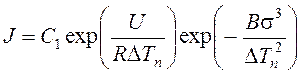 .
.
|
|
|
Рис. 59. Зависимость скорости кристаллизации J от величины переохлаждения DТn |
Поведение двух множителей – экспонент в зависимости от переохлаждения неодинаково: первый множитель с ростом переохлаждения снижается (кривая 1, рис. 59), а второй множитель с ростом переохлаждения возрастает (кривая 2, рис. 59). Произведение двух множителей выразится кривой с максимумом (кривая 3, рис. 59), отражающей физическую сущность максимума для кристаллического зародыша критических размеров.
Рассмотренные выше закономерности отражают так называемую самопроизвольную кристаллизацию, при которой кристаллические зародыши образуются в результате флуктуаций атомов металлов, образующих группу атомов с взаимным расположением, подобным их расположению в кристаллической решетке металла. В реальных условиях кристаллизация носит вынужденный характер, т.е. в металле всегда есть готовые кристаллические зародыши в виде твердых включений, неметаллических включений, примесей. Вынужденная кристаллизация характеризуется весьма малыми величинами переохлаждения, не превышающими долей градуса. Особенно малую величину переохлаждение имеет на фронте затвердевания, т.е. на поверхностях растущих кристаллитов – не более 0,1°С.
Подчеркнем, что все изложенное относится к так называемой первичной кристаллизации, т.е. к формированию структуры при переходе из жидкого состояния в твердое. При последующей обработке давлением, термической обработке отливок происходит изменение кристаллической структуры – перекристаллизация.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.