Масса слоя железа толщиной 0,1 мм на площади 1 м2 равна:
![]() г.
г.
Следовательно, требуемое количество кислорода составит 780·0,43=336 г.
Количество образующейся Fe2O3 можно определить из отношения
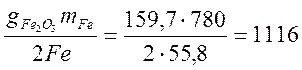 г.
г.
При выводе этого соотношения принято во внимание, что формулу гидроокиси железа можно представить в следующем виде :
![]() .
.
7-2. По условиям примера 7-1. Определить количество образующегося водорода в предположении, что коррозия происходит с участием ионов водорода, т.е. с водородной деполяризацией.
Решение.
Основное уравнение процесса коррозии с водородной деполяризацией может быть представлено в следующем виде:
![]() .
.
Оно
позволяет составить пропорцию, рещение которой даёт следующее
выражение: 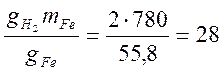 г,
г,
что составит 310 л в нормальных условиях.
7-3. Щёлочность и сухой остаток котловой воды двух котлов, установленных в промышленной котельной, соответственно равны: ЩКВ= 12 мг-экв/кг ; SКВ= 3700 мг/кг и ЩКВ= 4 мг-экв/кг ; SКВ= 600 мг/кг.
В каком котле котловая вода более агрессивна в отношении межкристаллитной коррозии, если судить об этом по её относительной щёлочности при условии, что котловую воду не фосфатируют ?
Решение.
Относительная щёлочность котловой воды для первого котла равна:
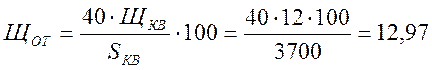 %.
%.
Для
второго котла , соответственно, :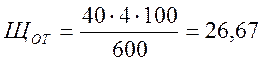 %.
%.
Так
как ЩОТ второго котла превышает допустимое значение (![]() %), поэтому котловая вода в нём более
агрессивная чем в первом котле в отношении межкристаллитной коррозии.
%), поэтому котловая вода в нём более
агрессивная чем в первом котле в отношении межкристаллитной коррозии.
8. Водно-химические режимы
8.1 Водно-химические режимы барабанных котлов
8.1.1 Гидразинно-аммиачный водный режим
Загрязнение питательной воды ТЭС продуктами коррозии конструкционных материалов (оксидами железа, меди, цинка) обусловлено присутствием в ней коррозионно-активных газов О2 и СО2.
Обогащение питательной воды углекислотой сопровождается резким снижением рН среды в соответствии с реакцией:
![]() ;
;
![]() .
.
В таких условиях протекает водородная деполяризация, в результате чего на катодных участках выделяется молекулярный водород Н2, а при одновременном присутствии в воде О2 и СО2 ещё и коррозия с кислородной деполяризацией, образуя ионы ОН-. Анодные участки металла растворяются, посылая в раствор ионы Fe2+, которые с ионами ОН- образуют Fe(OH)2. В присутствии кислорода Fe(OH)2 окисляется до Fe(OH)3. При параллельных процессах кислородной и водородной деполяризации твёрдая фаза гидроксидов железа, имея слабое сцепление с поверхностью металла, поступает в питательную воду [6].
На скорость процессов коррозии с кислородной и водородной деполяризацией оказывает влияние рН среды. Так, коррозия с водородной деполяризацией практически прекращается при значении рН раствора более 8,8. Поэтому, для обеспечения нормируемого качества питательной воды водный режим барабанных котлов во всех случаях должен быть щелочным.
Для подавления коррозии с водородной деполяризацией на электростанциях применяется амминирование питательной воды. Ионы гидроксила, образующиеся при диссоциации аммиака, нейтрализуют ионы водорода, обусловленные диссоциацией свободной углекислоты:
![]() ;
;
![]() ;
;
![]() .
.
Для полного связывания 1мг СО2 требуется 0,4 мг NH3 . В результате нейтрализации угольной кислоты аммиаком образуется карбонат или бикарбонат аммония NH4HCO3, (NH4)2CO3.
В рабочих условиях котлов происходит разложение продуктов амминирования согласно уравнениям:
![]() ;
;
![]() .
.
Из воды в пар переходят NH3 и СО2 и удаляются с ним из котла. В котловой воде остаётся не более 10-15 % аммиака, введённого с питательной водой, причём часть его удаляется продувкой.
В перегретом паре NH3 и СО2 существуют раздельно, а при конденсации пара они взаимодействуют с образованием карбоната аммония. Таким образом, достигается полное исключение или существенное снижение скорости углекислотной коррозии.
В связи стем, что в тепловой схеме ТЭС непрерывно удаляются NH3 и СО2 в деаэраторах, с отсосом паровоздушной смеси из конденсаторов и теплообменных аппаратов, для поддержания рН питательной воды в оптимальных пределах (9,1±0,1) необходима непрерывная подача аммиака в питательный контур.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.