Разрушение защитных плёнок может также наступить при химическом воздействии на них концентрированных едкого натра или кислых солей при упаривании воды.. При этом едкий натр наиболее опасен для металла, так как он не упаривается досуха вследствие того, что при 320 0С переходит в расплав, обладающий весьма высокой коррозионной агресивностью. При оценке влияния солей на устойчивость плёнок необходимо иметь в виду, что в результате испарения на поверхности нагрева возникает тонкий плёночный слой воды с большой концентрацией веществ, находящихся в растворённом и нерастворённом состоянии в воде всего объёма котла . Естественно, что температура в граничном слое выше температуры всего объёма воды. Протекание всех водно-химических реакций и коррозионного процесса завершается в данном слое. В граничном слое могут образовываться отложения веществ, хотя концентрация их в объёме воды далека от предела растворимости. Поэтому на поверхности металла при испарении воды могут осаждаться легкорастворимые в воде соли, концентрация которых быстро достигает предела растворимости при испарении воды в граничном слое. Эти соли затем снова переходят в раствор, т.е. в «ядерный» слой воды всего объёма котла при его остановке. Явлению «хайд аута» наиболее сильно подвержены Na3PO4 и другие фосфаты натрия , растворимость которых при 340 0С снижается до 0,2 % (25-30 % при комнатной температуре). Под слоем соединений фосфатов, выпадающих на поверхности стали, может развиваться пароводяная коррозия с образованием бороздок, что обусловлено разрушающим действием отложений на защитные плёнки. В реакции с железом принимает участие как кислый фосфат, так и концентрат щелочи – продукты гидролиза тринатийфосфата. Продуктом «хайд аута» является Na2HPO4, который разъедает металл.
При оценке коррозионной агрессивности котловой воды при дозировании различных фосфатов установлено, что определяющим фактором является не химическая природа фосфатов, а отношение Na+ : РО43- в котловой воде [8]. Наименьшая скорость коррозии отвечает отношению Na+ : РО43- = 2,7 ÷ 3,2 . Уменьшение или увеличение этого отношения приводит к повышению содержания водорода в воде. Агрессивность котловой воды в отношении хрупких разрушений при прочих равных условиях в значительной мере зависит от относительной щёлочности, %, котловой воды, которую можно определить по формуле :
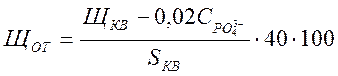 ,
(7-9)
,
(7-9)
где ![]() - солесодержание котловой воды, мг/кг ;
- солесодержание котловой воды, мг/кг ; ![]() - концентрация фосфатов в котловой воде,
если фосфатирование проводится тринатрийфосфатом, мг/кг.
- концентрация фосфатов в котловой воде,
если фосфатирование проводится тринатрийфосфатом, мг/кг.
Для котлов, работающих без фосфатирования, формула приобретает более простой вид :
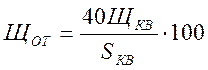 .
(7-10)
.
(7-10)
Принято считать, что допустимое значение относительной щёлочности котловой воды Щот не должно превышать 20 %. Если в питательную систему добавляют умягчённую воду, то относительная щёлочность воды зависит от состава исходной воды и метода её обработки. Для некоторых методов обработки могут быть выведены следующие зависимости:
а) прямоточное Na-катионирование
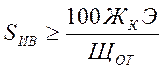 ;
(7-11)
;
(7-11)
б) известкование и содоизвесткование
![]()
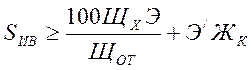 ;
(7-12)
;
(7-12)
в) Н-Na-катионирование
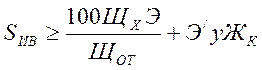 ,
(7-13)
,
(7-13)
где ЩХ
– щёлочность умягчённой воды, мг-экв/кг; SИВ
– сухой остаток исходной воды, мг/кг; Э – эквивалент для NaOH;
![]() - доля воды, поступающей на Н-катионитные
фильтры; Э/ - снижение сухого остатка исходной воды, приходящейся на
1 мг-экв/кг удалённой карбонатной жёсткости, мг.
- доля воды, поступающей на Н-катионитные
фильтры; Э/ - снижение сухого остатка исходной воды, приходящейся на
1 мг-экв/кг удалённой карбонатной жёсткости, мг.
Следовательно,
произведения ![]() и
и ![]() характеризуют
общее снижение сухого остатка исходной воды в результате её обработки. При ориентировочных
расчётах значение Э/ можно принимать равным 45 мг. Как следует из
приведённых зависимостей, чтобы относительная щёлочность котловой воды не
превышала предельного значения, сухой остаток исходной воды не должен быть
менее некоторого определённого значения.
характеризуют
общее снижение сухого остатка исходной воды в результате её обработки. При ориентировочных
расчётах значение Э/ можно принимать равным 45 мг. Как следует из
приведённых зависимостей, чтобы относительная щёлочность котловой воды не
превышала предельного значения, сухой остаток исходной воды не должен быть
менее некоторого определённого значения.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.