5.Конверсия монооксида углерода. Равновесие процесса. Роль температуры в глубине переработки СО в продукты. Уравнение для расчёта константы равновесия. Кинетика процесса. Двухступенчатая организация процесса. I ступень: катализаторы и параметры процесса. Утилизация тепла газов после первой ступени. II ступень: катализаторы и параметры процесса. Методика расчёта МБ процесса конверсии СО. (1)
Газ после 2-й ступени конверсии СН4 состоит (в пересчете на сух газ) %об: СН4 н.б.0,5; СО н.б. 10-13; СО2 н.б. 6,5-8,5; Н2 н.б. 56-60; N2 н.б. 20-23, далее идет конверсия СО водяным паром: СО+Н2О = СО2 +Н2, - 41 (1).
К1 = Рсо2Рн2/РсоРн2о, f при различных температурах К1 м.б. вычислено через формулу:
lgK1 = A/T + BlgT + CT – DT2 – E (A,B,C,D,E – числовые константы.; Т – температура)
При повышении температуры К уменьшается, т.е. равновесие смещается влево, т.е. надо стремится к реализации низкотемпературной конверсии СО. (1) идет без изменения объема, т.е. повышение давления не смещает равновесия, но дает преимущества: увеличивается объемность реакции, уменьшается размер аппарата. Поддерживают 3-5-ти кратный избыток пара, т.к. степень конверсии СО увеличивается при избытке пара. В процессе участвует пар, оставшийся после конверсии СН4, соотношение пар : газ = 0,4-0,7. Реакция (1) идет быстро, если есть Кt. Ведение экзотермических процессов на единственном большом слое Кt-ра без отвода Q не выгодно, т.к. температура в контактной зоне увеличивается и равновесие смещается в другую сторону. Поэтому конверсию в современных схемах под Р = 3МПа ведут в 2 ступени.
1-ую: на среднетемпературном Кt-(СТК) реагирует большая часть СО и температура увеличивается от 330-380 на входе до 390-440 на выходе. Аппарат работает в адиабатическом режиме. Содержание СО после 1-ой ступени н.б.4%об. Тепло реакции утилизируется в котле-утилизаторе.
Во 2-ой ступени на НТК превращается СО почти до равновесных остаточных концентраций. Температура газа на входе в реактор 2-ой ступени 200-240, Теплоемкость в слое Кt-ра увеличивается лишь на 10-150С, т.к. здесь превращается незначительное кол-во СО. Содержание СО после 2-й ступени н.б. 0,.6%об. На 1-ой ступени используются недорогие Fe-Cr-ые Кt. В частности СТК-1-5 (Fe в пересчете на Fe2O3 н.м. 88; Cr (на Cr2O3) н.м. 7; Al (на Al2O3) 5%мас). Важные характеристики Кt-ров: активность - определяет объем Кt-ра в аппарате. Механическая прочность - определяет величину сопротивления слоя. Теплоемкость - характеризует температурную стойкость Кt-ра. Активность СТК-1-5 не высока, яды для него S-органические, Н2S, соединения Р, Аr, Si, Cl, пыль, сажа. Служба 2-8 лет. Допустимая температура в слое Кt-ра 320-520, удельная поверхность 25-30 м2/г, активность н.м. 1,4см3/г*с, при 3500С Средняя прочность н.м. 3,5 МПа (по образующей). Теплоемкость 0,84-0,96 кДж/кг*К (при 300-5000С). На 2-й ступени используется НТК-4 содержащий Cr (на Сr2O3) н.м. 14+-1,5; Сu (на СuО)54+-3; Zn (наZnO) 11+-1,5; Al (на Al2O3) 19,6+-2. Допустимая температура в слое Кt-ра 200-250. Удельная поверхность 50-60; активность 5-6 (при 2250С), средняя прочность 25 (по торцу); теплоемкость 0,71 при 2000С. Срок службы Кt-ра НТК 2-5лет. НТК сильно подвержен отравлению ядами. Яды прочно связываются в ZnO и CuO. Отравление S и Cl необратимо.
Конвертор СО 1-й ступени – вертикальный аппарат, D=5м, Н=10,2 м , под Р=3МПа.
С повышением давления в системе степень использования внутренней поверхности Кt-ра увеличивается, а производительность единицы объема Кt-ра(z) увеличивается пропорциально квадратному корню из относительного давления: z = z0√р/р0.
Z0 – производительность единицы объема Кt-ра при Р атм; Р,Р0 – давление в системе и стандартное атмосферное Р = 0,1мпа. Конверсия СО на Кt-ре из Fe2O3 состоит в попеременном окислении-восстании поверхностного мономолекулярного слоя Кt по схеме:
1 ступень [K]+H2O=[K]O+H2
[K]-активный участник
2 ступень [K]O+ CO=[K]+CO2
ток поверхности Кt- ра.
суммарная: CO+H2O=H2+CO2 лимитирует процесс 2-я стадия.
V-ть реакции на Кt-ре описывается уравнением 1-го порядка относительно СО.
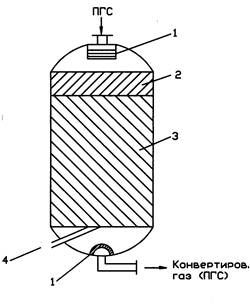 1-
распределительные устройства,
1-
распределительные устройства,
2 – насадка,
3 – Кt-р,
4 – линия выгрузки Кt-ра
Объем Kt-ра СТК-1-5 80,6м3; ∆Р=0,04-0,3МПа; производительность по сухому газу на входе =184800 и по влажному газу 292000 м3/ч. Конвертор 2-й ступени такой же, но используется НТК-4 70,1м3. Конверсия СО идет в области внутренней диффузии, т.е. торможение идет в порах Кt-ра и меняется с температурой и давлением.
V = kpco,
k - константа скорости реакции,
рсо- парциальное давление СО. Точнее V-ть реакции на СТК и НТК:
V = k(pcoph2o – Кph2pco2)/(Арн2о+рсо2)
К- константа равновесия р-и (1) при температуре процесса,
А – величина, зависитт от t.
Для Fe-Cr-вых СТК при 400-5000С (и для НТК при 200-3000С) используются уравнения для А и k:
Lgk = 7440/Т+10,2;
lgА = -1926/Т+2,32.
В кинетической области константа скорости реакции (1) от t:
k = 4,95*107*e-86000/RT, 86000-Еа, Дж/моль.
МБ
Цель: определение состава газа после 1 ступени конверсии.
Исходные данные:
1) на 100 м3 сухого газа поступающего в конвертор.
2) состав на входе: Н2 = 56,96; N2 = 22,18; CO = 12,69; CO2 = 7,59; CH4 = 0,3; Ar = 0,28.
3) объемное отношение пар: сухой газ на входе в конвертор 0,588;
4) Температура ПГС на входе 440º;
5) Соотношение между компонентами газа на выходе при достижении равновесия задается константой скорости реакции при 4400С К = 8,2.
6) степень достижения равновесия реакции конверсии СО - 0,9
Расчет: через реактор идет 1 поток ПГС на Fe-Cr-ом Кt-ре, идет р-я (1).
Принимаем за Х – объем прореагировавшего СО при условии достижения равновесия, м3.
1) К1 = Рсо2Рн2/РсоРн2о,
Р – парциальное давление, рi =vi Робщ /Vобщ,(*)
Подставляем (*) в К1 получаем:
К=vco2vн2/vcovн2о,
v-объемы компонентов в состоянии равновесия, м3.
2) расчет объемов компонентов на входе в конвертор. Из отношения = 0,588 находим Vвод. пара.
3) выражаем объемы компонентов в состоянии равновесия, через Х.
4) рассчитаем Х при 4400С, подставив Vi в выражение для К.
5) в конверторе СО 1-й ступени равновесие реакции (1) еще не достигается, поэтому рассчитываем фактически прореагировавший Vco.
6) рассчитываем фактический объем компонентов в газе на выходе из конвектора,м3
7) заполним табл. объем и состав газа после конвертора СО 1-й ступени (на 100м3 сухого исходного газа): Н2, N2, CO, CO2, CH4, Ar, H2O пар.
8) расчет отношения пар : газ после конвертора СО 1-й ступени.
34.Дать полную характеристику конвертору монооксида углерода, как реактору. Материал конвертора.
Конвертор СО.
1) по характеру процесса: на 1 стадии не достигается равновесие, на 2 практически до равновесия. остаточное СО не б 0,6%.
2) по фаз состоянию: гетерогенно-каталитический
3) по тепловому эффекту: экзотермический.
4) по температуре: среднетемпературный.
5) по давлению 3,3 МПа – высокий
6) по степени перемешивания – идеального вытеснения.
7) по температурному режиму: если не учитывать потерь через стенку – адиабатический, 8) по времени – непрерывный, сталь легированная хром, никель, титан.
Задача: Равновесие реакции конверсии СО:
lgК=2485,5/Т+1,565*lgТ-0,066*10-3*Т+0,207 *105/ Т2 –6,946.
Напишите эту реакцию, рассчитайте К при 400 оС.
Расчет:
СО+Н2О«СО2+Н2О, Н = -41. Т = 400+273=673 К.
lgК = 1,0829Þ К=12,103.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.