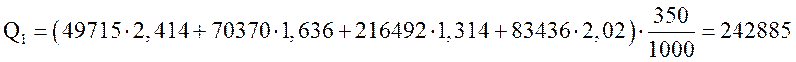 МДж/ч.
МДж/ч.
Тепло химической реакции
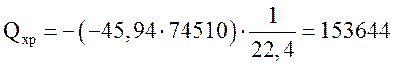 МДж/ч.
МДж/ч.
Потери тепла принимаем 0,5 % от прихода тепла. Тогда потери тепла составят
Qп = (91280+153644)×0,005= 1225 МДж/ч.
Отводимое в тепло
Qто = 91280+153644–242855–1225 = 814 МДж/ч.
Таблица 3.4
Тепловой баланс колонны синтеза аммиака
Приход
МДж/ч
%
Расход
МДж/ч
%
1. Тепло с исходным газом
91280
37,27
1. Тепло с газовой смесью
242855
99,16
2. Тепло химической реакции
153644
62,73
2. Отводимое тепло
814
0,33
3. Потери тепла
1225
0,50
Итого
244924
100
Итого
244924
100
Тепловой баланс 1-ого слоя колонны синтеза аммиака имеет вид
Q0 + Qxp = Q1 + Qп,
где Q0 – физическое тепло, вносимое исходной газовой смесью;
Qхр – тепло химической реакции;
Q1 – физическое тепло, уносимое газовой смесью;
Qп – потери тепла в окружающую среду.
Температура на входе в первый слой катализатора составляет 390°С. Тогда тепло, вносимое с исходной газовой смесью составит
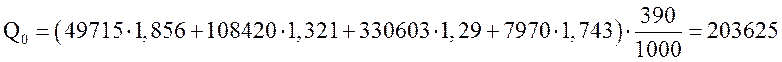 МДж/ч.
МДж/ч.
Рассчитаем теплоемкости компонентов газовой смеси на выходе из 1-ого слоя колонны при температуре 500 °С, или 773 К
ЧГУ.З.РК.240301.000.004.ПЗ
Лист
26
Из
Лист
№ докум.
Подп.
Дата
метан 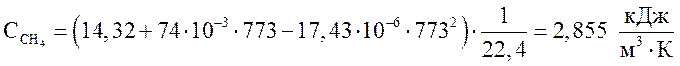 ,
,
азот 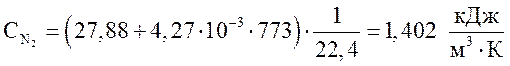 ,
,
водород 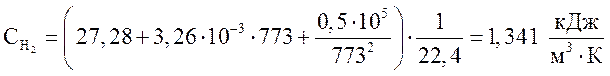 ,
,
аммиак 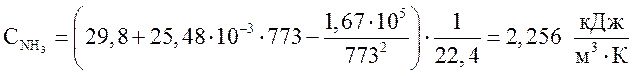 .
.
Тепло химической реакции
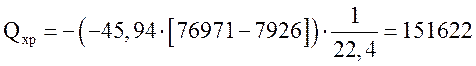 МДж/ч.
МДж/ч.
Потери тепла принимаем 0,5 % от прихода тепла. Тогда потери тепла составят
Qп = (91280+151622)×0,005= 1215 МДж/ч.
Тогда тепло с газовой смесью на выходе из 1-ого слоя колонны синтеза составит
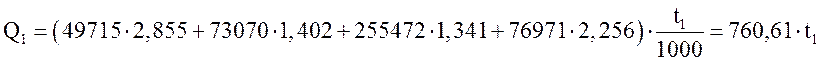 МДж/ч.
МДж/ч.
Таким образом, получаем уравнение:
203625 + 151622 = 760,61×t1 + 1215.
Решая полученное уравнение, имеем
t1 = 495 °С,
а физическое тепло, уходящее с 1-ой полки:
Q1 = 760,61×495 = 354032 МДж/ч.
Для охлаждения газа после 1-ой полки подается байпас с температурой 130 °С. Температура газа на входе во 2-ой слой не должна превышать 460 °С.
Тепловой баланс примет следующий вид
Q1 + Qб = Q2
где Qб – тепло, вносимое байпасом;
Q2 – тепло приходящее на 2-ую полку.
Тепло, приходящее с байпасом, можно представить как
![]() .
.
Qб = (0,6991×1,290 + 0,2095×1,321 + 0,0154×1,743 + 0,0969×1,865)×130/1000×Vб = 0,180×Vб
Теплоемкости компонентов на входе во 2-ой слой после смешения с байпасом при температуре 460 °С (733 К)
ЧГУ.З.РК.240301.000.004.ПЗ
Лист
27
Из
Лист
№ докум.
Подп.
Дата
метан 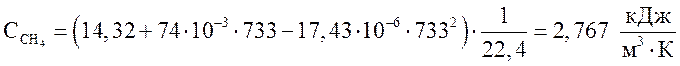 ,
,
азот 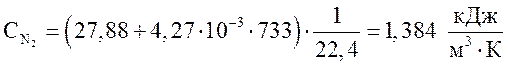 ,
,
водород 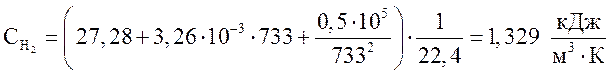 ,
,
аммиак 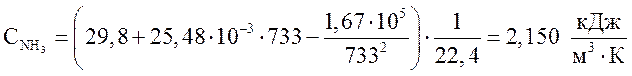 .
.
Тогда тепло, вносимое с газом на 2-ую полку (после смешения с байпасом), можно представить как
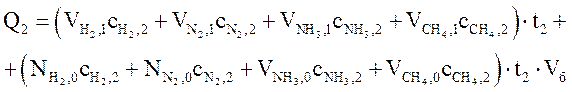
Q2 = (224667×1,329 + 73095×1,384 + 76987×2,150 + 49769×2,767)×460/1000 +
+ (0,6991×1,329 + 0,2095×1,384 + 0,0154×2,150 + 0,0969×2,767)×460/1000×Vб =
= 247230 + 0,699×Vб
Таким образом, получаем уравнение
354032 + 0,180×Vб = 247230 + 0,699×Vб
Решая полученное уравнение, имеем
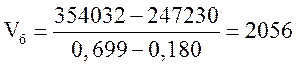 нм3/ч.
нм3/ч.
3.3.3. Конструктивный расчет основного аппарата
4.5.1. Расчет 1-ого слоя катализатора
Расчет объема катализатора
Кинетическое уравнение реакции синтеза аммиака
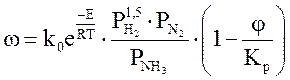
или
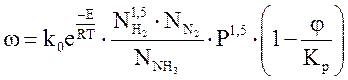
ЧГУ.З.РК.240301.000.004.ПЗ
Лист
28
Из
Лист
№ докум.
Подп.
Дата
ЧГУ.З.РК.240301.000.011.ПЗ
Лист
Из
Лист
№ докум.
Подп.
Дата
где k0 – предэкпонента константы скорости;
Е – энергия активации;
Р – общее давление.
Рассчитаем средние концентрации компонентов в слое
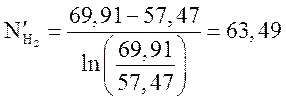 об.%;
об.%;
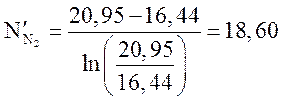 об.%;
об.%;
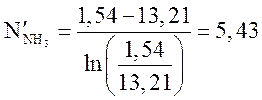 об.%.
об.%.
Средняя температура в слое
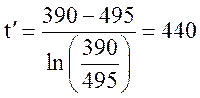 °С.
°С.
Средние парциальные давления:
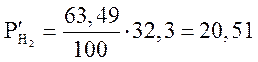 МПа;
МПа;
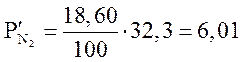 МПа;
МПа;
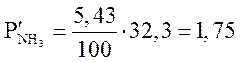 МПа.
МПа.
Тогда
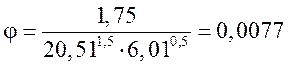 МПа-1
МПа-1
Константа равновесия при средней температуре
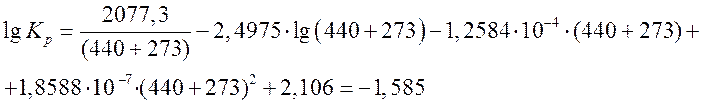
Откуда
Кр = 0,026 атм–1
ЧГУ.З.РК.240301.000.004.ПЗ
Лист
29
Из
Лист
№ докум.
Подп.
Дата
Предэкспонециальный
множитель составляет 1,5×103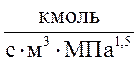 ; энергия активации 80
кДж/моль. Тогда скорость реакции
; энергия активации 80
кДж/моль. Тогда скорость реакции
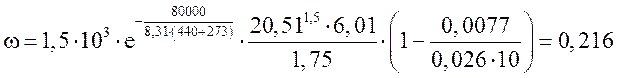
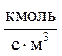
Нагрузка на катализатор
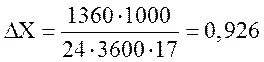 кмоль/с
кмоль/с
Тогда объем катализатора
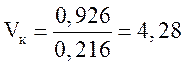 м3.
м3.
Принимаем объем катализатора 4,7 м3.
Расчет сопротивления слоя катализатора
Перепад давления в слой катализатора рассчитываем по формуле [10]:
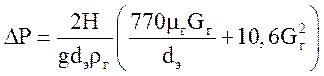 ,
,
где dэ – эквивалентный диаметр частиц;
Gг – массовая скорость газа (кг/м2с);
mг – вязкость газа.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.