![]() кг/ч;
кг/ч;
метана ![]() нм3/ч,
нм3/ч,
плотность
метана 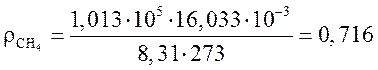 кг/м3,
кг/м3,
![]() кг/ч;
кг/ч;
По условию в колонне образуется аммиак 56667 кг/ч. Тогда объем образовавшегося аммиака составит
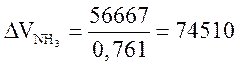 нм3/ч.
нм3/ч.
Объем аммиака на выходе из колонны:
![]() нм3/ч, или
нм3/ч, или
![]() кг/ч.
кг/ч.
Объем водорода на выходе из колонны:
![]() нм3/ч, или
нм3/ч, или
![]() кг/ч.
кг/ч.
Объем азота на выходе из колонны:
![]() нм3/ч, или
нм3/ч, или
![]() кг/ч.
кг/ч.
ЧГУ.З.РК.240301.000.004.ПЗ
Лист
22
Из
Лист
№ докум.
Подп.
Дата
Таблица 3.1
Сводный материальный баланс колонны синтеза аммиака
Приход
нм3/ч
кг/ч
об.%
Расход
нм3/ч
кг/ч
об.%
1. Аммиак
2. Водород
3. Азот
4. Аргон
5. Метан
7926
328258
107625
20031
49769
6028
29550
134638
25058
35630
1,54
69,91
20,95
3,90
9,69
1. Аммиак
2. Водород
3. Азот
4. Аргон
5. Метан
82436
216492
70370
20031
49769
62694
19488
88032
25058
35630
18,87
49,30
16,03
3,90
9,69
Итого
513608
230903
100
Итого
439098
230903
100
Расчет I-ой катализаторной полки
Принимаем концентрацию аммиака после первой катализаторной полки 70 % от концентрации аммиака на выходе из колонны [6]. Тогда
![]() об.%.
об.%.
Конечную концентрацию аммиака после первой полки можно выразить как
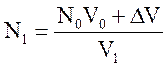 ,
,
где N0 – концентрация аммиака на входе;
V0 – объем газа на входе;
DV – объем образующегося аммиака;
V1 – объем газа на выходе.
Объем газа на выходе можно представить с учетом стехиометрии реакции синтеза аммиака
V1 = V0 – DV
Подставляя это выражение в уравнение для расчета концентрации аммиака на выходе и преобразуя его, имеем
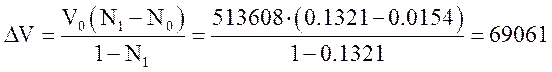 нм3/ч.
нм3/ч.
Тогда объем газа после 1-ой полки составит
V1 = 513608–69061 = 444547 нм3/ч.
Объем аммиака после 1-ой полки составит
7926+69061 = 76987 нм3/ч.
Объем водорода после 1-ой полки составит
328258–1,5×69061 = 224667 нм3/ч.
ЧГУ.З.РК.240301.000.004.ПЗ
Лист
23
Из
Лист
№ докум.
Подп.
Дата
Объем азота после 1-ой полки составит
107625–0,5×69061 = 73095 нм3/ч.
Таблица 3.2
Материальный баланс 1-ой катализаторной полки
Приход
Нм3/ч
% об.
Расход
нм3/ч
% об.
1. Аммиак
2. Водород
3. Азот
4. Аргон
5. Метан
7926
328258
107625
20031
49769
1,54
69,91
20,95
3,90
9,69
1. Аммиак
2. Водород
3. Азот
4. Аргон
5. Метан
76987
224667
73095
20031
49769
13,21
57,47
16,44
4,51
11,19
Итого
513608
100
Итого
444547
100
3.3.2. Расчеты тепловых балансов
Таблица 3.3
Температурные ряды и теплоты образования веществ, участвующих в процессе [9]
Соединение
Температурный ряд
Энтальпия,
КДж/моль
A
b
C (c’)
СН4
14,32
74,69×10–3
–17,43×10–6
–74,85
N2
27,88
4,27×10–3
0
0
H2
27,28
3,26×10–3
0,5×105
0
NH3
29,8
25,48×10–3
–1,67×105
–46,19
ЧГУ.З.РК.240301.000.004.ПЗ
Лист
24
Из
Лист
№ докум.
Подп.
Дата
Тепловой баланс колонны синтеза
Тепловой баланс колонны синтеза аммиака имеет вид
Q0 + Qxp = Q1 + Qто+ Qп,
где Q0 – физическое тепло, вносимое исходной газовой смесью;
Qхр – тепло химической реакции;
Q1 – физическое тепло, уносимое газовой смесью;
Qто – тепло, отводимое в слое катализатора;
Qп – потери тепла в окружающуюсреду.
Рассчитаем теплоемкости компонентов газовой смеси на входе в колонну при температуре 130 °С, или 403 К
метан 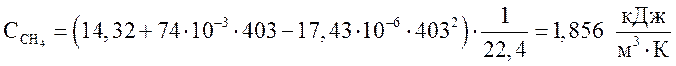 ,
,
азот 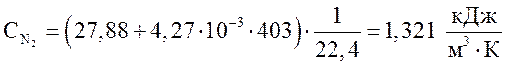 ,
,
водород 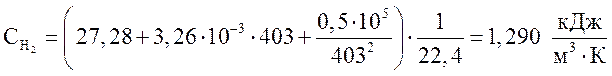 ,
,
аммиак 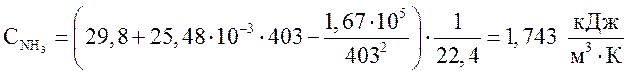 .
.
Тогда тепло, вносимое с исходной газовой смесью составит
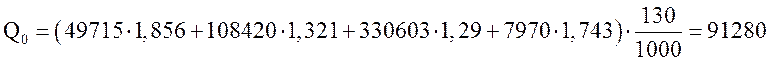 МДж/ч.
МДж/ч.
Рассчитаем теплоемкости компонентов газовой смеси на выходе из колонны при температуре 350 °С, или 623 К
метан 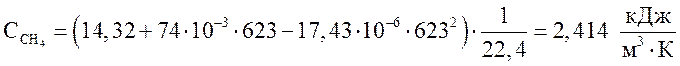 ,
,
азот 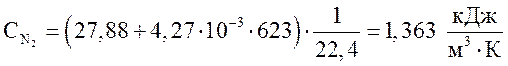 ,
,
водород 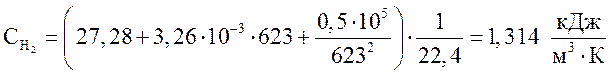 ,
,
аммиак 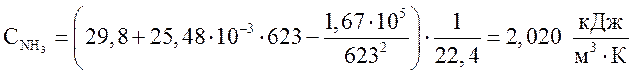 .
.
ЧГУ.З.РК.240301.000.004.ПЗ
Лист
25
Из
Лист
№ докум.
Подп.
Дата
Тогда тепло, с газовой смесью на выходе из колонны синтеза составит
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.