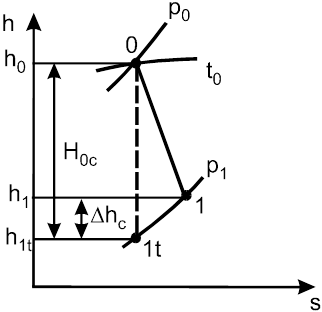
Эта часть кинетической энергии потока вследствие трения превращается в теплоту, вследствие чего повышается энтальпия газа (или пара). Поэтому действительное состояние газа (или пара) на выходе из сопла изображается в hs-диаграмме точкой 1, расположенной на той же изобаре р1 правее теоретической точки 1t (рис.1.24). Действительный процесс истечения отклоняется от изоэнтропы (s1>s1t), в диаграмме он представляет линию 0-1.
Из рис.1.24 также видно, что h0 – h1 < h0 — h1t, что соответствует неравенству c1 < c1t, так как
c1 = j![]() , м/с.
(1.76)
, м/с.
(1.76)
 |
В инженерной практике поправки на трение учитываются после расчета теоретической скорости с1t истечения газа или пара (без трения).
При расчете теоретической скорости истечения газа или водяного пара пользуются формулой (1.62) в виде
![]() , (1.77)
, (1.77)
где энтальпии h0 и h1t, кДж/кг, определяются по таблице либо по h,s-диаграмме соответствующего рабочего тела.
Для критической скорости формула (1.77) запишется так:
![]() , (1.78)
, (1.78)
где hкр определяется по изоэнтропе sкр=s0 при давлении ркр.
1.10.6.Процесс дросселирования
При прохождении потока газа (пара) через суженое сечение в каком-либо участке канала происходит падение его давления. Процесс уменьшения давления, в результате которого нет ни увеличения кинетической энергии, ни совершения технической работы, называется дросселированием (мятием). Этот процесс часто встречается в технике (например, в клапанах, заслонках, дроссельных шайбах и других местных сопротивлениях).
На рис.1.25 показан канал, имеющий резкое сужение проходного сечения, и графики изменения параметров и скорости потока вдоль оси канала. Падение давления при дросселировании на величину Dр объясняется потерей части кинетической энергии потока из-за трения и вихреобразования на местном сопротивлении. Данный необратимый процесс происходит в условиях изолированной системы, без подвода тепла извне, и поэтому описывается уравнением адиабатного течения dh=- d(с2/2). Запишем его для двух сечений 1 и 2, достаточно удаленных от местного сопротивления:
![]() .
(1.79)
.
(1.79)
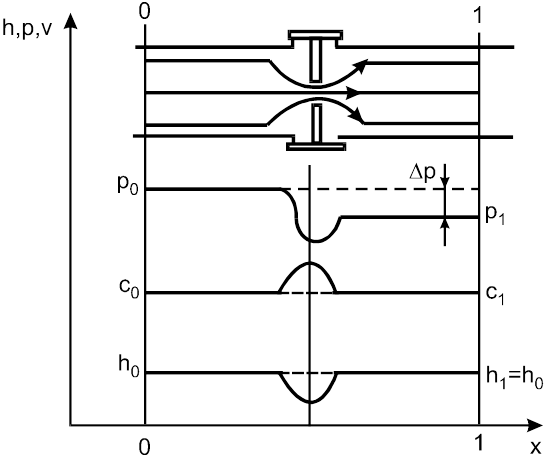 |
Рис.1.25. Изменение параметров h, p и скорости газа
в процессе дросселирования
х – направление оси канала
При одинаковом сечении канала до и после сужения потока изменение его кинетической энергии мало, поэтому можно принять, что с0=с1. Тогда из (1.79) следует, что
h0=h1 (∆h=0). (1.80)
Таким образом, при дросселировании рабочего тела его энтальпия остается постоянной, энтропия и объем увеличиваются, давление падает.
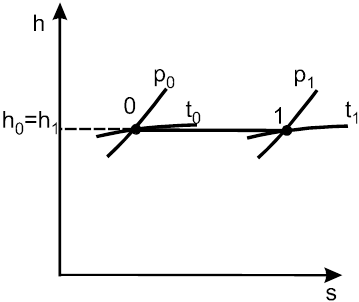
Температура в разных условиях меняется по-разному. Дросселирование — процесс изоэнтальпийный и на hs-диаграмме изображается прямой линией h=const, параллельной оси энтропии (рис. 1.26).
Данный вывод справедлив для идеального и реального газов, поскольку при выводе (1.80) не оговаривались свойства газа. Следствия из (1.80) для идеального и реального газов будут существенно различны.
Для идеального газа u=u(Т), h=h(T), и дросселирование означает, что Т0=Т1. Для реального газа, у которого внутренняя энергия зависит и от объема, u=u(v, T), несмотря на то, что в процессе дросселирования ∆h = 0, ∆u ≠ 0, а следовательно, и ∆T ≠ 0 (T0 ≠ T1) т. е. дросселирование реального газа сопровождается изменением его температуры вследствие изменения теплоемкости.
 |
У большинства газов при не очень высоких температурах при дросселировании наблюдается охлаждение. Изменение температуры при дросселировании называется эффектом Джоуля — Томсона и используется в технике для получения низких температур.
1.11. Реальные газы. Водяной пар
Реальный газ, в отличие от идеального, состоит из
молекул конечного объема, связанных между собой силами взаимодействия, имеющими
электромагнитную природу. Ван-дер-вальс (1873 г.), исходя из качественных физических
представлений, получил эмпирическое уравнение состояния реального газа, которое
носит его имя:  ,
(1.81)
,
(1.81)
здесь b-поправка на объем (предельный объем сжатия газа); a/v² - поправка на внутреннее давление (добавочное к внешнему) за счет сил молекулярного притяжения; a и b - физические константы, определяемые экспериментально для конкретного газа. Это уравнение можно получить также аналитически.
Водяной пар является реальным газом и широко используется в качестве рабочего тела в технике и, в особенности, в теплоэнергетике. Водяной пар получается в процессе парообразования при подводе теплоты к воде в теплообменных аппаратах и агрегатах, например в паровых котлах.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.