2. Азотсодержащие группы
|
Название |
Структура |
Название |
Структура |
|
|
NH2 |
Амидная |
|
|
Аминогруппа вторичная |
= NH |
Замещенная амидная |
|
|
|
N |
Лактамная |
С = О NH |
|
|
NO2 |
Гидразинная |
– NH – NH2 |
|
|
N = O |
Гидразидная |
|
3. Серосодержащие группы
|
Название |
Структура |
Название |
Структура |
|
Сульфгидрильная |
– SH |
Аминометилен-сульфонатная |
–NH – CH2 – SO3 – Na |
|
Сульфогруппа |
– SO3H |
Сульфамидная |
– SO2 – NH2 |
|
Тиокарбонильная |
>С=S |
Сульфамидная замещенная |
– SO2 – NH – R |
4. Кратные (ненасыщенные) углерод-углеродные связи
![]() - для алифатических и ароматических соединений
- для алифатических и ароматических соединений
![]() - для алифатических соединений
- для алифатических соединений
5. Прочие функциональные группы
![]() d+
d+
![]()
![]() С –
Н - активный атом водорода
С –
Н - активный атом водорода
d+
![]()
![]() СН2
СН2
- активная метиленовая группа
![]() С = О
С = О
![]()
![]() С – Hal - галоген-углеродная
функция
С – Hal - галоген-углеродная
функция
|
Гидроксил
1. Реакция этерификации SN
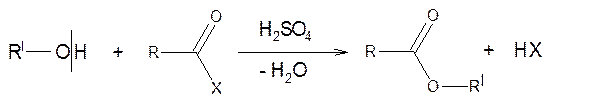
2. Реакция окисления
Первичные спирты окисляются до альдегидов:

вторичные спирты – до кетонов:

третичные спирты, у которых атом углерода не связан с атомами водорода, устойчивы к окислению.
В фармацевтическом анализе реакции окисления и этерификации (ацилирования) широко используются как для установления подлинности, так и для определения количественного содержания.
Подлинность многоатомных спиртов подтверждают реакцией комплексообразования с гидроксидами тяжелых металлов:
![]()
![]() CuSO4 + 2 NaOH Cu(OH)2
+ Na2SO4
CuSO4 + 2 NaOH Cu(OH)2
+ Na2SO4
Фенольный гидроксил
1. В отличие от спиртов, фенолы взаимодействуют не только со щелочными металлами, но и с водными растворами гидроксидов щелочных металлов, образуя соли – феноляты:
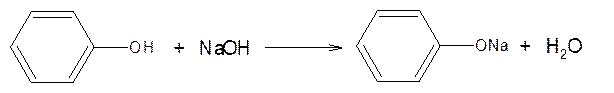
2. Реакция этерификации
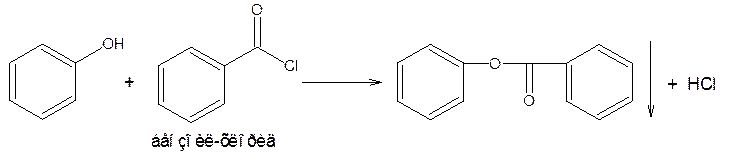
Тплавления
Сложные эфиры фенолов нельзя получить непосредственным взаимодействием с кислотами, их получают путем взаимодействия с ангидридами или хлорангидридами кислот (лучше в щелочной среде).
3. Реакция с FeCl3. Образуются комплексы различного состава.
|
|
Характер окраски зависит от наличия и расположения в молекуле фенольных гидроксилов и других функциональных групп.
4. Реакция образования азокрасителя при сочетании с солями диазония:
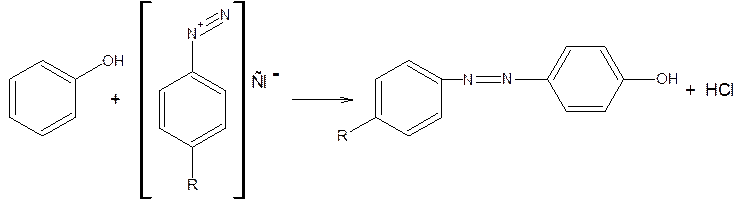
5. Реакции окисления и конденсации
а) образование индофенола

б) Нитрозореакция Либермана (разновидность индофенольной реакции)
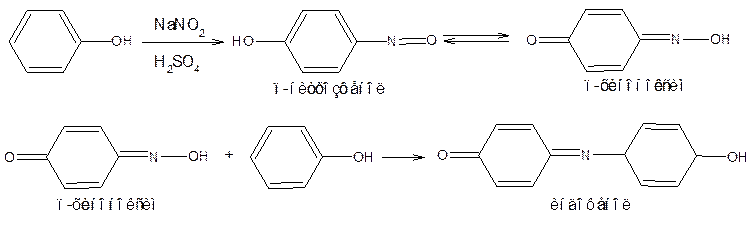
в) образование ауринового красителя с реактивом Марки (формальдегид и конц. H2SO4)
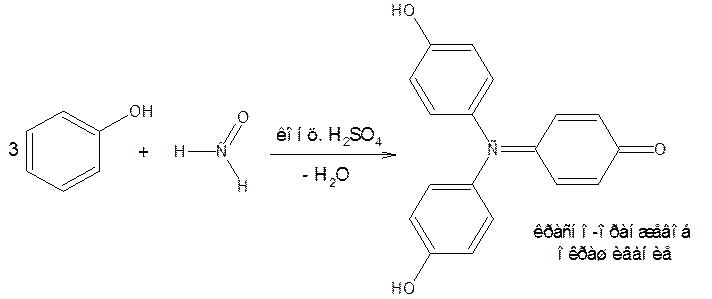
6. Реакции замещения SE (бромирование в о- и п-положения)
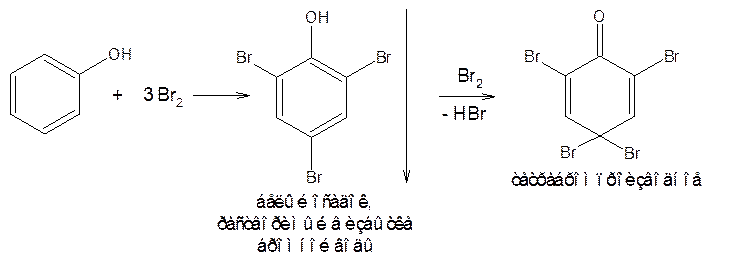
В основном эта реакция используется для количественного определения броматометрическим методом.
Например,
![]() 5 KBr + KBrO3 + 6 HCl 3 Br2 + 6 KCl + 3 H2O
5 KBr + KBrO3 + 6 HCl 3 Br2 + 6 KCl + 3 H2O
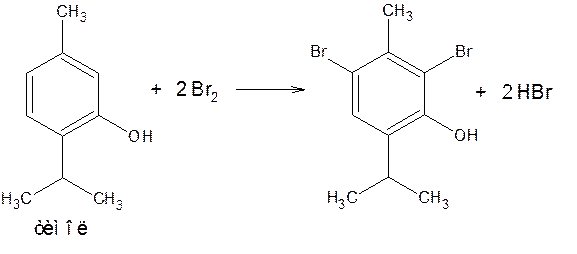
Индикатор – метиловый оранжевый
В фармацевтическом анализе чаще используются реакции комплексообразования с хлоридом железа (III), образования азокрасителя и ауринового красителя, а также реакции электрофильного замещения.
Карбонильная группа
1. Реакции окисления а) с реактивом Толленса (аммиачный раствор нитрата серебра)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.