Пользуясь уравнениями горения для составляющих газообразного топлива, можно написать, что объем трехатомных газов, м3/м3, будет равен:
VRO2 = 0,01⋅(CO2 + CO + H2S+ ∑(n⋅Cn mH ))Т .
Объем азота в продуктах сгорания
VN02 = 0,79⋅V0 + 0,01⋅ NТ2 и сухих газов
VСГ0 =VRO2 +VN02 . (6)
Теоретический объем водяных паров в продуктах сгорания газа
Т
⎛
0 ⎛ n ⎞ ⎞ 0
VH O2 = 0,01⋅⎜H2 + H2S+ ∑⎜ ![]() ⋅CnHm ⎟ + 0,124⋅dГТ ⎟ + 0,0161⋅V , (7)
⋅CnHm ⎟ + 0,124⋅dГТ ⎟ + 0,0161⋅V , (7)
⎝ ⎝ 2 ⎠ ⎠
где dГТ – влажность газообразного топлива, г/м3.
Суммарный теоретический объем продуктов сгорания топлива, м3/м3:
V VГ0 = СГ0 +VH O02 =VRO2 +VN02 +VH O02 . (8)
Полный (действительный) объем сухих газов, м3/м3, можно определить из выражения
VСГ ![]() V V0, (9)
V V0, (9)
а полный объем водяных паров, м3/м3, будет:
VH O2 =VH O02 + 0,0161⋅ α −( 1)⋅V0.
Наконец, действительный объем, м3/м3, дымовых газов составит:
V
VГ![]() V0. (10)
V0. (10)
Изложенные формулы позволяют определять количество воздуха, потребного для горения, и объемы дымовых газов при известном избытке воздуха. Избыток воздуха при расчете выбирается на основе опытных данных (табл. 1), в зависимости от типа горелок и топочного устройства, элементов котельного агрегата и установки.
Таблица 1. Значения коэффициента избытка воздуха в топке
|
Наименование |
Избытки воздуха в топке α т для топлива |
||||||||
|
антрацитов и полуантрацито в |
каменны х углей |
бурых углей |
сланцев |
торф а |
древесин ы |
жидкого |
газообразног о |
||
|
топочного устройства |
|||||||||
|
Неподвижная решетка с ручным забросом топлива |
1,30–1,35 |
1,3–1,4 |
1,3–1,5 |
1.3 |
|||||
|
Неподвижная решетка с пневмомеханическим забросом топлива |
1,6–1,7 |
1,4–1,5 |
1,4–1,5 |
||||||
|
Шахтная топка с наклонной решеткой |
1,4 |
1,4 |
|||||||
|
Топка с зажатым слоем топлива (скоростная топка В.В. Померанцева) |
1,2–1,3 |
||||||||
|
Топка с цепной решеткой |
1,5–1,6 |
||||||||
|
То же и шахтой для топлива |
1,3 |
||||||||
|
То же и пневматическим забрасывателем топлива |
1.3–1,4 |
1,3–1,4 |
|||||||
|
То же с пневмомеханическим забрасывателем и обратным ходом |
1,3–1,4 |
1,3–1,4 |
|||||||
|
Топка с наклонно переталкивающими колосниками |
1,4 |
||||||||
|
Камерные топки с твердым удалением шлака |
1,25 |
1,2 |
1,2 |
1,2 |
1,2 |
1,25 |
|||
|
То же с жидким удалением шлака |
1,2 |
1,2 |
1,2 |
||||||
|
Камерные топки для мазута и других жидких топлив |
1,02–1,1 |
||||||||
|
То же для природного и нефтепромыслового газа |
1,10 |
||||||||
Расчет горелочного устройства
Теоретическое количество воздуха, необходимое для сгорания:
Т
⎛
0 ⎛ m ⎞ ⎞
V = 0,0476⋅⎜⎝0,5⋅CO + 0,5⋅H2 +1,5⋅H2S+ ∑⎜⎝n + ![]() 4
⎟⎠⋅СnHm − O2 ⎟⎠ =
4
⎟⎠⋅СnHm − O2 ⎟⎠ =
= 0,0476⋅(2⋅CH4 + 3,5⋅C2 6H + 5⋅C3 8H + 6,5⋅C4 10H +8⋅C5 12H )T =
= 0,0476⋅(2⋅98,4 + 3,5⋅0,33+ 5⋅0,12 + 6,5⋅0,04 +8⋅0,01) = 9,5 м3/м3.
Теоретический объем продуктов сгорания: а) сухих трехатомных газов
VRO2 = 0,01⋅(CO2 + CO + H2S+ ∑(n⋅CnHm))Т =
= 0,01⋅(CO2 +1⋅CH4 + 2⋅C H2 6 + 3⋅C H3 8 + 4⋅C H4 10 + 5⋅C H5 12 )Т =
= 0,01⋅(0,1+1⋅98,7 + 2⋅0,33+ 3⋅0,12 + 4⋅0,04+ 5⋅0,01) =1,0 м3/м3. б) азота
VN02 = 0,79⋅V0 + 0,01⋅ NТ2 = 0,79⋅9,5+ 0,01⋅0,7 = 7,51 м3/м3. в) водяных паров
Т
VH O02 = 0,01⋅⎜⎛H2 + H2S+ ∑⎛⎜⎝
![]() m2 ⋅Cn mH ⎟⎠⎞
+ 0,124⋅dТ ⎟⎞⎠
+ 0,0161⋅V0 =
m2 ⋅Cn mH ⎟⎠⎞
+ 0,124⋅dТ ⎟⎞⎠
+ 0,0161⋅V0 =
⎝
= 0,01⋅(2⋅CH4 + 3⋅C2 6H + 4⋅C3 8H +5⋅C4 10H + 6⋅C5 12H )Т + 0,0161⋅V0 =
= 0,01⋅(2⋅98,7 + 3⋅0,33+ 4⋅0,12 + 5⋅0,04 + 6⋅0,01)Т + 0,0161⋅9,5 = 2,14 м3/м3, где dТ – влажность газообразного топлива, г/м3.
Определим коэффициент избытка после подмешивания к воздуху горячих продуктов сгорания до температуры смеси tсм = 45 °С. Воспользуемся формулой
![]() ⋅η
+ с ⋅t − V 2 c 2 2 2 V cВ tСМ
⋅η
+ с ⋅t − V 2 c 2 2 2 V cВ tСМ
α
= ![]() 0 , (11)
0 , (11)
V ⋅cВ ⋅(tСМ −tВ)
в которой ηТ = 0,96 – к.п.д. смесительного устройства; сТ – теплоемкость топлива, ккал/(м3⋅К); cRO2 – теплоемкость сухих трехатомных газов в продуктах сгорания, ккал/(м3⋅К); cH O2 – теплоемкость паров воды, ккал/(м3⋅К); сВ – теплоемкость воздуха, ккал/(м3⋅К).
Для индивидуальных веществ в состоянии идеального газа теплоемкость в кал/(моль⋅К) при любой температуре можно рассчитать по формуле cP = A+ B T⋅ +C T⋅ 2 + D T⋅ 3 , а для подсчета теплоемкости газовой смеси можно воспользоваться правилом аддитивности. Значение теплоемкости топлива при начальной температуре tТ = 20 °С приведено в табл. 2.
Теплоемкость сухих трехатомных газов, в которых в нашем случае находиться только оксид углерода (IV), найдем как:
cRO2 = A+ B T⋅ + C T⋅ 2 + D T⋅ 3,
cRO2 = 4,728+1,75⋅10-2 ⋅318,15−1,34⋅10-5 ⋅318,152 + 4,10⋅10-9 ⋅318,153 cRO2 = 8,8232 кал/(моль⋅К) или 8,8232/22,411383=0,3937 ккал/(м К3 ⋅ ).
Таблица 2. Теплоемкость газового топлива при tТ = 20 °С.

Теплоемкость водяных паров при tсм = 45 °С: cH O2 = A B T C T+ ⋅ + ⋅ 2 + D T⋅ 3,
cH O2 = 7,701+ 4,6⋅10-4 ⋅318,15+ 2,52⋅10-6 ⋅318,152 −8,59⋅10-10 ⋅318,153 cH O2 =8,0747 кал/(моль⋅К) или 8,0747/22,411383=0,3603 ккал/(м К3 ⋅ ).
Теплоемкость воздуха при tВ0 = –25 °С приведена в табл. 3, а при tсм = 45 °С – в табл. 4.
Таблица 3. Теплоемкость воздуха при tВ0 = –25 °С.

Таблица 4. Теплоемкость воздуха при tсм = 45 °С.

Подставив значения теплоемкостей в уравнение (11) найдем:

Расход топлива найдется из уравнения теплового баланса смесителя:
BТ ⋅(QНС ⋅η +Т сТ ⋅tТ +V0 ⋅α⋅cВ ⋅tВ) =VСМ ⋅cСМ ⋅tСМ.
Теплоемкость смеси воздуха с продуктами сгорания приведена в табл. 5.
Таблица 5. Теплоемкость смеси воздуха с продуктами сгорания при tТ = 45 °С.

![]() BТ = С СМ СМ СМ0 =
BТ = С СМ СМ СМ0 =
QН ⋅ηТ + сТ Т⋅t +V ⋅α⋅cВ В⋅t
 43,23 м3/ч или 0,012 м3/с.
43,23 м3/ч или 0,012 м3/с.
Количество воздуха, поступающего к горелке:
VВ = BТ ⋅V 0 ⋅α =Т 43,23⋅9,5⋅1,1= 451,73 м3/ч или 0,1255 м3/с.
Скорость истечения газа из отверстий определим по формуле
wГ = µГ ⋅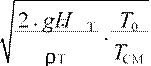 ,
,
где ρТ – плотность газового топлива, кг/м3; µГ – коэффициент расхода газа, µ =Г 0,96; HТ – избыточное давление газа перед соплами, мм вод. ст.,
TСМ – температура газа при истечении, К.
Избыточное давление газа перед соплами найдем из расчета, что
1 ат = 1 кг/см2 = 98066,5 Па, а 1 мм вод. ст. = 9,80665 Па. Тогда
98066,5 98066,5
HТ = pТ ⋅ ![]()
![]() 1800
мм вод. ст. и
1800
мм вод. ст. и
wГ
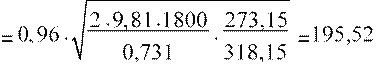 м/с.
м/с.
Скорость истечения воздуха, поступающего к горелке через отверстия:
wВ
= µВ ⋅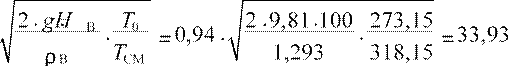 м/с. где µВ – коэффициент расхода воздуха,
µВ = 0,94; HВ
– избыточное давление воздуха перед соплами, мм вод. ст.
м/с. где µВ – коэффициент расхода воздуха,
µВ = 0,94; HВ
– избыточное давление воздуха перед соплами, мм вод. ст.
Суммарное сечение всех газовых отверстий
![]() fГ = BГс = 0,012 =
6,142⋅10−5 м2. wГ 195,52
fГ = BГс = 0,012 =
6,142⋅10−5 м2. wГ 195,52
Площадь одного отверстия для газа
f 6,142⋅10−5
0 Г −6 2
fГ = = ![]() = 3,84⋅10 м .
= 3,84⋅10 м .
16 16
Диаметр одного отверстия для газа составит
dГ
= 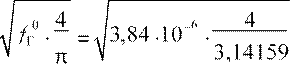 = 0,0022 м.
= 0,0022 м.
Суммарное сечение всех воздушных отверстий
VВ 0,1255 −3 2
fВ
= = ![]() = 3,698⋅10 м . wВ 33,93
= 3,698⋅10 м . wВ 33,93
Намечаем образующие на поверхности усеченного конуса в количестве 16 шт. по 10 отверстий для воздуха на каждой, итого 16×10 = 160 отверстий
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.