Министерство образования Российской Федерации
Санкт-Петербургский государственный горный институт
им. Г.В. Плеханова (технический университет)
Выполнил студент группы ОП-04:
Проверила: доцент
Санкт-Петербург
2007
Исследование поверхности раздела двух фаз: раствор ПАВ – воздух.
Цель работы: На основании изотермы поверхностного натяжения и изотермы адсорбции определить уравнения Шишковского, рассчитать предельное значение удельной адсорбции ПАВ, площадь, занимаемую одной молекулой и её длину.
1. Оборудование и реактивы.
2) колба круглая, объёмом 50 мл;
3) мерная пипетка, объёмом 15 или 20 мл;
4) резиновая груша;
5) раствор ПАВ для исследований.
2. Теоретические сведения.
Самопроизвольные процессы на границе раздела двух фаз в гетерогенных системах сопровождаются уменьшением избыточной энергии в поверхностном слое. К этому приводит уменьшение площади этой поверхности (частицы дисперсной фазы либо слипаются, коагулируют, либо приобретают сферическую форму) и поверхностного натяжения на границе раздела фаз. Также к изменению поверхностного натяжения приводит адсорбция, то есть самопроизвольное изменение концентрации веществ на поверхности по сравнению с концентрацией в объёмах фаз. Такой процесс характеризует удельная адсорбция:
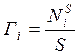 , где
, где ![]() - избыток
частиц i-го компонента,
- избыток
частиц i-го компонента,
S – поверхность.
Уравнение, которое описывает адсорбцию при постоянной температуре, называют уравнением изотермы адсорбции Гиббса:
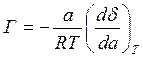 , в разбавленных
растворах активность вещества в растворе а заменяется на его концентрацию С.
, в разбавленных
растворах активность вещества в растворе а заменяется на его концентрацию С.
Вещества,
снижающие при растворении поверхностное натяжение растворителя ![]() ,
называют поверхностно – активными. К ним относятся органические вещества, менее
полярные, чем растворитель, например, карбоновые кислоты и их соли, амины и
аминокислоты, эфиры, а также спирты. Такие соединения, в которых содержится
неполярный радикал и полярная группа (карбоксильная, гидроксильная, и т. д.). С
ростом концентрации ПАВ в растворе, поверхностное натяжение растворителя
падает. Если же в растворитель добавлять более полярные вещества, поверхностное
натяжение растворителя будет увеличиваться. Такие вещества называют
инактивными. К ним относятся растворы электролитов (кислот, солей, щелочей) в
воде.
,
называют поверхностно – активными. К ним относятся органические вещества, менее
полярные, чем растворитель, например, карбоновые кислоты и их соли, амины и
аминокислоты, эфиры, а также спирты. Такие соединения, в которых содержится
неполярный радикал и полярная группа (карбоксильная, гидроксильная, и т. д.). С
ростом концентрации ПАВ в растворе, поверхностное натяжение растворителя
падает. Если же в растворитель добавлять более полярные вещества, поверхностное
натяжение растворителя будет увеличиваться. Такие вещества называют
инактивными. К ним относятся растворы электролитов (кислот, солей, щелочей) в
воде.
Из уравнения Гиббса следует, что поверхностно – активные вещества накапливаются на поверхности, а поверхностно – инактивные, наоборот, выводятся из неё.
![]() d Зависимость поверхностного натяжения от концентрации:
d Зависимость поверхностного натяжения от концентрации:

![]() 1 – ПАВ; 2
1 – ПАВ; 2
2 – ПИВ.

![]()

![]()
А
![]()
![]() В
В
1
![]()
![]()
![]() С
С
Для нахождения
производной 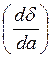 используют
уравнение Шишковского:
используют
уравнение Шишковского:
![]() , где
, где ![]() ,
, ![]() -
поверхностное натяжение соответственно чистого растворителя и раствора;
-
поверхностное натяжение соответственно чистого растворителя и раствора;
a и b – эмпирические коэффициенты.
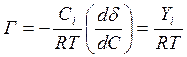 , где
, где ![]() =AB на оси ординат;
=AB на оси ординат;
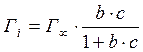 ,
,
![]() -
предельное значение удельной адсорбции,
-
предельное значение удельной адсорбции,
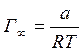 .
.
По величине ![]() можно
посчитать площадь поперечного сечения молекулы ПАВ
можно
посчитать площадь поперечного сечения молекулы ПАВ ![]() и её
длину
и её
длину ![]() по
формулам:
по
формулам:
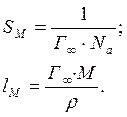
где ![]() - число
Авогадро;
- число
Авогадро;
М – молекулярная масса ПАВ;
r - плотность ПАВ.
Для определения поверхностного натяжения используют два метода: статический и динамический.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.