






теория, развитая в [З] в общем виде, не зависящем
от силы (и знака) проявления эффекта адсорбции вещества ядра на поверхности
капли, требует от термодинамики знания не только порогового значения
химического потенциала пара, но ![]() еще
и сведений о работе гетерогенного образования капли: положений и полуширин
потенциальной ямы и потенциального горба раб,эгы, энергии активации (перепада
высот потенциального горба и потенциальной ямы работы).
еще
и сведений о работе гетерогенного образования капли: положений и полуширин
потенциальной ямы и потенциального горба раб,эгы, энергии активации (перепада
высот потенциального горба и потенциальной ямы работы).
Нахождению ключевых термодинамических характеристик кинетики конденсации в сложном случае растворимых в каплях ядер ПАВ и посвящена данная статья. Эти характеристики позволяют легко найти уже и все остальные термодинамические характеристики, нужные для кинетики конденсации в предпороговой области значений химического потенциала пара и проявляемые в эксперименте.
Рассмотрение не будет ограничено конкретным видом изотер , ы адсорбции вещества ядра на
99
поверхности капли (и связанным с ним по уравнению адсорбции Гиббса видом двухмерного уравнения состояния адсорбционного слоя вещества ядра на поверхности капли). Опорой рассмотрения послужат идеи, высказанные в [4]. В случае ядер поверхностно-инактивных веществ аналогџчное рассмотрение было полностью (в нужном для кинетики конденсации объеме) проведено в [1]. В случае ядер ПАВ полученные ранее [5 - 7] термодинамические результаты относились лишь к одной, хотя и главнейшей, термодинамической характеристике кинетики конденсации — пороговому значению химического потенциала пара. Эти результаты, к тому же, были ограничены в [6] предположением о постоянстве величины адсорбции, а в [7] — предположением о применимости изотермы адсорбции Ленгмюра.
ПРЕДПОРОГОВАЯ ОБЛАСТЬ
МЕТАСТАБИЛЬНОСГИ ПАРА
В [6 - 9] было показано, что химический потенциал конденсата в капле как функция размера капли, зарождающейся на растворимом в ней ядре ПАВ, может иметь не один, а несколько максимумов, природа которых связана либо со свойствами монослоя ПАВ на поверхности капли, либо с образованием мицелл в объемной части раствора внутри капли, либо с влиянием поверхностных сил ядра при неполном его растворении в капле. Пороговое значение химического потенциала пара определяется наибольшим из этих максимумов.
Ограничимся в данной статье случаем, когда наибольший из максимумов попадает в область полного растворения ядра и когда это растворение приводит к образованию молекулярного (а не мицеллярного) раствора ПАВ внутри капли. Даже и в этом случае химический потенциал конденсата может обладать более чем одним максимумом.
Обозначим через bv химический потенциал конденсата в капле как функцию числа молекул v конденсата, а через Ь химический потенциал пара. Химические потенциалы bv и Ь выражаем в тепловых единицах энергии КТ (К — постоянная Больцмана, Т — температура пара и капли) и отсчитываем от значения, соответствующего равновесию пара с конденсирующейся жидкосгью при плоской поверхносги их соприкосновения,
Для порогового значения btr
химического потенциала пара Ь имеем btr =![]() (1)
(1)
![]()
![]()
![]()
![]() Здесь
индекс нуль характеризует экстремумы химического потенциала конденсата, а
символ тах выделяет наибольший из этих экстремумов. Им, естественно,
оказывается максимум. Величины, относящиеся к наибольшему из экстремумов,
помечаем в дальнейшем индексом tr. Включение в экстремумы не только максимумов,
но и минимумов позволит полностью раскрыть термодинамическую картину
гетерогенной конденсации.
Здесь
индекс нуль характеризует экстремумы химического потенциала конденсата, а
символ тах выделяет наибольший из этих экстремумов. Им, естественно,
оказывается максимум. Величины, относящиеся к наибольшему из экстремумов,
помечаем в дальнейшем индексом tr. Включение в экстремумы не только максимумов,
но и минимумов позволит полностью раскрыть термодинамическую картину
гетерогенной конденсации.
Будем интересоваться, как и в [1, З], лежащей лишь чуть снизу от и чрезвычайно узкой предпороговой областью значений химического потенциала пара, в которой
![]() (2)
(2)
где Е > 0 и Е 1. Для простоты предположим, что эта область, которую более кратко будем называть предпороговой областью метастабильносги пара, лежит выше всех остальных, помимо наибольшего (равного b,r), экстремумов химического потенциала конденсата bv. При достаточно малом Е это предположение не является жестким.
В согласии с общим термодинамическим соотношением [10]
DFlDv = bv — Ь (3)
для работы образования капли Е, выраженной, как bv и Ь, в тепловых единицах энергии КТ, сделанное предположение означает, что в интересующей нас предпороговой области метастабильности пара на кривой зависимости АР от v существуют только один минимум и только один максимум. Действительно, уравнение
(4)
определяющее
ввиду (3) экстремумы работы Е, успевает обрести в этой области только два
корня. Корень, соответствующий минимуму работы Е, обозначим через ve, а корень,
соответствующий максимуму работы F, обозначим через vc. Между этими корнями
располагается точка перегиба работы Е. Ею, как ясно из (3) и ![]() = О, является точка v = максимума
химического потенциала конденсата bv. Очевидно, vtr, в отличие от
= О, является точка v = максимума
химического потенциала конденсата bv. Очевидно, vtr, в отличие от ![]() и vc, не зависит, как и bv, от
химического потенциала пара Ь.
и vc, не зависит, как и bv, от
химического потенциала пара Ь.
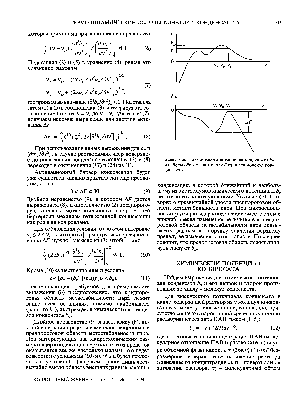
Зависимость bv от v и вытекающая из нее по термодинамическому соотношению (З) зависимость F от в предпороговой области метастабильности пара изображены на рисунке. Представлен сложный случай, когда bv обладает более чем одним экстремумом (двумя максимумами и расположенным между ними минимумом). Разность максимума и минимума работы F в точках
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.