4,66 Fe7S8 – х FeS
m(Fe в FeS) = 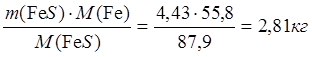 ;
;
m(S в FeS) = 1,62 кг.
m(S2) = 4,66–4,43 = 0,23 кг.
7. Fe3O4 + CO ® 3FeO + CO2
m(Fe3O4) = 9,96-0,15 = 9,81кг
m(Fe в Fe3O4) = 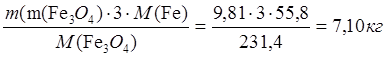 ;
;
m(O в Fe3O4) = 2,71 кг.
231,4 Fe3O4 – 3∙71,8 FeO
Þ х = m(FeO) = 9,13 кг
9,81 Fe3O4 – х FeO
m(Fe в FeO) = m(Fe в Fe3O4) = 7,10 кг;
m(O в FeO) = 2,03 кг.
3∙71,8 FeO – 28 CO
Þ х = m(CO) = 1,19 кг
9,13 FeO – х CO
m(C в CO) = 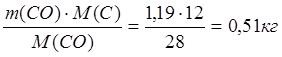 ;
;
m(O в CO) = 0,68 кг.
m(CO2) = 9,81+1,19-9,13 = 1,87 кг
m(C в CO2) = 0,51 кг;
m(O в CO2) = 1,36 кг.
8. FeO + CO ® Feмет + CO2
m(FeO) = 9,13 кг
m(Feмет) = m(Fe в FeO) = 7,10 кг;
m(O в FeO) = 2,03 кг.
71,8 FeO – 28 CO
Þ х = m(CO) = 3,56 кг
9,13 FeO – х CO
m(C в CO) = 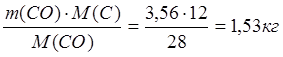 ;
;
m(O в CO) = 2,03 кг.
m(CO2) = 9,13+3,56-7,10 = 5,59 кг
m(C в CO2) = 1,53 кг;
m(O в CO2) = 4,06 кг.
9. Fe2O3 + CO ® 2FeO + CO2
m(Fe2O3) = 10,63-0,16 = 10,47кг
159,6 Fe2O3 – 2∙71,8 FeO
Þ х = m(FeO) = 9,42 кг
10,47 Fe2O3 – х FeO
m(Fe в FeO) = 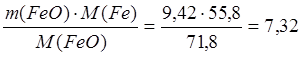 кг;
кг;
m(O в FeO) = 2,10 кг.
159,6 Fe2O3 – 28 СO
Þ х = m(СO) = 1,84 кг
10,47 Fe2O3 – х СO
m(C в CO) = 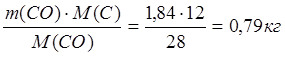 ;
;
m(O в CO) = 1,05 кг.
m(CO2) = 10,47+1,84-9,42 = 2,89 кг
m(C в CO2) = 0,79 кг;
m(O в CO2) = 2,1 кг.
Feмет образуется по реакции восстановления FeO, и расходуется на восстановление металлического Ni и Сo:
mшт(Feмет) = 7,10-0,11-0,4 = 6,59 кг
mшт(FeS) = 11,42-0,17+0,47+0,89-0,64+4,43 = 16,40 кг
mшт(Fe в FeS)
= 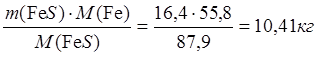 ;
;
mшт(S в FeS) = 5,99 кг.
![]() = mшт(Feмет)+ mшт(Fe в FeS) = 6,59+10,41 = 17,00 кг;
= mшт(Feмет)+ mшт(Fe в FeS) = 6,59+10,41 = 17,00 кг;
![]() = 0,61+1,56+5,99 = 8,16 кг.
= 0,61+1,56+5,99 = 8,16 кг.
Таблица 8
Состав штейна
|
Соединение |
Количество |
Элемент |
Количество |
||
|
кг |
% |
кг |
% |
||
|
Cu2S |
3,05 |
9 |
Cu |
2,44 |
7,5 |
|
Coмет |
0,12 |
0,4 |
Co |
0,12 |
0,4 |
|
Niмет |
0,43 |
1,4 |
Ni |
4,68 |
14,4 |
|
Ni3S2 |
5,81 |
18 |
Fe |
17,00 |
52,4 |
|
Feмет |
6,59 |
20 |
S |
8,16 |
25,1 |
|
FeS |
16,4 |
51 |
Прочие |
0,07 |
0,2 |
|
Прочие |
0,07 |
0,2 |
|||
|
Всего в штейне |
32,47 |
100 |
Всего в штейне |
32,47 |
100 |
Расчет компонентов шлака
Компоненты шихты, которые не полностью перешли в штейн и пыль, уходят в шлак.
В шлак переходит:
- оставшаяся масса Cu2S:
mшл(Cu2S) = 2,77-0,04-2,63 = 0,1 кг
m(Cu в Cu2S) = 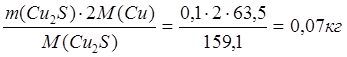 ;
;
m(S в Cu2S) = 0,03 кг.
- не до конца прореагировавший CoO:
mшл(CoO) = 0,17-0,00(в пыль уходит очень малое количество)-0,15 = 0,02 кг
m(Со в CoO) = 0,01 кг; m(O в CoO) = 0,01 кг.
- весь СоS:
mшл(CoS) = 0,02 кг
m(Со в CoS) = 0,01 кг; m(S в CoS) = 0,01 кг.
![]() .
.
- оставшийся NiO:
mшл(NiO) = 1,18-0,02-1,08 = 0,08 кг.
m(Ni в NiO) = 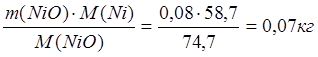 ;
;
m(О в NiO) = 0,01.
Шлак представлен силикатным расплавом; в него входит в основном фаялит, а также силикаты магния, кальция и алюминия.
1. 2FeO + SiO2 → Fe2SiO4
На образование фаялита идет вся суммарная масса FeO, образующаяся по реакциям:
m(FeO) = 0,14+0,52+0,53+9,42 = 10,61 кг
2·71,8 FeO – 60,1 SiO2
Þ х = m(SiO2) = 4,44 кг
10,61 FeO – х SiO2
m(Fe2SiO4) = m(FeO)+ m(SiO2) = 10,61+4,44 = 15,05 кг.
2. MgO + SiO2 → MgO·SiO2
Оксид магния из исходной шихты уходит в пыль; остальное количество MgO идет на реакцию образования силиката магния:
m(MgO) = 14,34-0,22 = 14,12 кг
40,3 MgO – 60,1 SiO2
Þ х = m(SiO2) = 21,06 кг
14,12 MgO – х SiO2
m(MgO·SiO2) = m(MgO)+ m(SiO2) = 14,12+21,06 = 35,18 кг.
3. СaO + SiO2 → CaO·SiO2
Оксид кальция из исходной шихты уходит в пыль; остальное количество СaO идет на реакцию образования силиката кальция:
m(СaO) = 1,97-0,03 = 1,94 кг
56,1 СaO – 60,1 SiO2
Þ х = m(SiO2) = 2,08 кг
1,94 СaO – х SiO2
m(СaO·SiO2) = m(СaO)+ m(SiO2) = 1,94+2,08 = 4,02 кг.
4. Al2O3 + SiO2 → Al2O3·SiO2
Оксид алюминия из исходной шихты уходит в пыль; остальное количество Al2O3 идет на реакцию образования силиката алюминия:
m(Al2O3) = 5,23-0,08 = 5,15 кг
102 Al2O3 – 60,1 SiO2
Þ х = m(SiO2) = 3,03 кг
5,15 Al2O3 – х SiO2
m(Al2O3·SiO2) = m(Al2O3)+ m(SiO2) = 5,15+3,03 = 8,18 кг.
Расчет массы флюса
Кремнезем из исходной шихты (27,52 кг) уходит в пыль (0,41 кг), идет на образование фаялита (4,44 кг), на реакции образования силикатов магния (21,06 кг), кальция (2,08 кг) и алюминия (3,03 кг). Масса расходуемого кремнезема:
m(SiO2) = 0,41+4,44+21,06+2,08+3,03 = 31,02 кг
Масса расходуемого кремнезема больше массы исходного оксида кремния. Это означает, что в исходном материале недостаток кремнезема. Следовательно, в шихту электропечи необходимо ввести кварцевый флюс. Состав принимаемого кварцевого флюса:
SiO2 – 78%, FeO – 8%, MgO – 4%, СaO – 6%, прочие – 4%.
Определим флюсующую способность кварцевой руды, исходя из того, что оксиды железа, магния и кальция будут расходовать оксид кремния на образование своих силикатов.
2·71,8 FeO – 60,1 SiO2
Þ х = 3,35% SiO2 на 2FeO·SiO2;
8% FeO – х SiO2
40,3 MgO – 60,1 SiO2
Þ х = 5,96% SiO2 на MgO·SiO2;
4% MgO – х SiO2
56,1 СaO – 60,1 SiO2
Þ х = 6,43% SiO2 на СaO·SiO2.
6% СaO – х SiO2
Суммарная флюсующая способность:
78 -![]() SiO2
(%) = 78-(3,35+5,96+6,43) = 62,26%
SiO2
(%) = 78-(3,35+5,96+6,43) = 62,26%
Недостаток массы флюса составляет:
mнед(SiO2) = 31,02-27,52 = 3,5 кг
Значит, масса флюса равна:
mфл = 3,5 / 0,6226 = 5,62 кг
mфл(SiO2) = 5,62·0,78 = 4,39 кг;
mфл(FeO) = 5,62·0,08 = 0,45 кг;
m(Fe в FeO) =
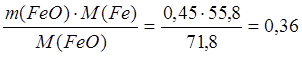 кг; m(O в FeO) = 0,09 кг.
кг; m(O в FeO) = 0,09 кг.
mфл(MgO) = 5,62·0,04 = 0,22 кг;
mфл(СaO) = 5,62·0,06 = 0,34 кг;
mфл(прочих) = 5,62·0,00 = 0,22 кг.
Дальнейший расчет шлака с учетом компонентов флюса
При введении в исходную шихту флюса изменяется состав шлака, т. к. в него переходят FeO, СaO, MgO в виде 2FeO·SiO2,, СaO·SiO2, MgO·SiO2 соответственно.
mфл(SiO2 в 2FeO·SiO2) = 4,39·0,0335 = 0,15 кг
m(Fe2SiO4) = 0,45+0,15 = 0,60 кг
![]() mшл(Fe2SiO4) = 15,05+0,60 = 15,65 кг.
mшл(Fe2SiO4) = 15,05+0,60 = 15,65 кг.
mфл(SiO2 в СaO·SiO2) = 4,39·0,0643 = 0,28 кг
m(СaO·SiO2) = 0,34+0,28 = 0,62 кг
![]() mшл(СaO·SiO2) = 4,02+0,62 = 4,64 кг.
mшл(СaO·SiO2) = 4,02+0,62 = 4,64 кг.
mфл(SiO2 в MgO·SiO2) = 4,39·0,0596 = 0,26 кг
m(MgO·SiO2) = 0,22+0,26 = 0,48 кг
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.