При взаимодействии солей олова (II) с щелочами получается гидроксид олова (II) Sn(OH)2.
ж) Ход эксперимента.
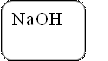
После этого к одной капле добавим 2 капли раствора соляной кислоты HCl, а ко второй еще 2 капли раствора гидроксида натрия NaOH.
з) Наблюдения.
В обеих ячейках осадок растворяется.
и) Уравнения реакции.
Sn(OH)2 + 2HCl = SnCl2 + 2H2O
Sn(OH)2 + NaOH = Na2[Sn(OH)4
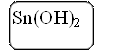 |
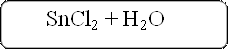 |
||||||
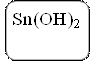 |
 |
![Na2[Sn(OH)4]](http://files3.vunivere.ru/workbase/00/05/94/22/images/image048.gif) |
|||||||
л) Вывод.
Так как гидроксид олова (II) Sn(OH)2 растворяется и в кислоте HCl и в щелочи NaOH, то он является амфотерным.
Опыт 7.
а) Название эксперимента.
Восстановительные свойства олова (II).
б) Ход эксперимента.
В 2 ячейки капельного планшета поместим по 1 капле раствора хлорида олова (II) SnCl2. К обеим добавим по капле соляной кислоты HCl. Затем, к первой капле добавим 2 капле перманганата калия KMnO4, ко второй добавим 2 капли раствора дихромата калия K2Cr2O7.
в) Наблюдения.
Цвет раствора в ячейке с перманганатом калия меняется с фиолетового на бесцветный, а в ячейке с дихроматом меняется с оранжевого на желто - синий.
г) Уравнения реакции.
5SnCl2 + 16HCl + 2KMnO4 = 5SnCl4 + 2MnCl2 + 8H2O + 2KCl
Sn+2 - 2ē = Sn+4 5 восстановитель
Mn+7 + 5ē = Mn+2 2 окислитель
3SnCl2 + 28HCl + 2K2Cr2O7 = 2CrCl3 + 3SnCl4 + 4KCl + 14H2O
Sn+2 - 2ē = Sn+4 3 восстановитель
Cr+6 + 3ē = Cr+3 2 окислитель
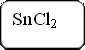 |
|||||||
 |
|||||||
Олово (II) является активным восстановителем.
Опыт 8.
а) Название эксперимента.
Получение гидроксида свинца (II) и изучение его свойств.
б) Ход эксперимента.
В две ячейки капельного планшета поместим по капле ацетата свинца (II) Pb(CH3COO)2. К каждой капле добавим по 1 капле раствора гидроксида натрия NaOH.
в) Наблюдения.
Выпадает белый осадок.
г) Уравнения реакции.
Pb(CH3COO)2 + 2NaOH = Pb(OH)2 ↓+ 2NaCH3COO
 |
е) Вывод.
При взаимодействии ацетата свинца (II) Pb(CH3COO)2 с щелочами получается гидроксид свинца (II) Pb(OH)2.
ж) Ход эксперимента.
После этого к одной капле добавим 2 капли раствора уксусной кислоты CH3COOH, а ко второй еще 3 капли раствора гидроксида натрия NaOH.
з) Наблюдения.
В обеих ячейках осадок растворяется.
и) Уравнения реакции.
Pb(OH)2 + 2CH3COOH = Pb(CH3COO)2 + 2H2O
Pb(OH)2 + 2NaOH = Na2[Pb(OH)4]
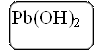 |
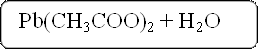 |
||||||
 |
|||||
 |
 |
||||||||
л) Вывод.
Так как гидроксид свинца (II) Pb(OH)2 растворяется и в кислоте CH3COOH и в щелочи NaOH, то он является амфотерным.
Опыт 9.
а) Название эксперимента.
Характерная реакция на ион свинца (II).
б) Ход эксперимента.
В ячейку капельного планшета внесем 1 каплю раствора уксуснокислого Pb(CH3COO)2 свинца и добавим 1 каплю раствора йодистого калия KJ.
в) Наблюдения.
Выпадает ярко желтый осадок.
г) Уравнения реакции.
Pb(CH3COO)2 + KJ = PbJ2↓ + 2KCH3COO
д) Иллюстрационный материал.
Для того, чтобы обнаружить ион свинца Pb+2 надо провести реакцию с йодидом калия KJ. На ион свинца будет указывать ярко желтое окрашивание раствора.
4. Контрольные вопросы.
1. Какие вам известны комплексные соединения бора и алюминия? Какие координационные числа характерны для бора и алюминия?
Комплексные соединения:
- для бора
[B(OH)4]Cl, [BF3H]OH, [BF4]Cl
- для алюминия
Na[Al(OH)4], [Al(OH)6]Cl.
Координационные числа:
- для алюминия
4 и 6
- для бора
3 и 4
2. В растворе находятся ионы Pb2+ и Sn2+. Как их можно разделить?
Нужно провести качественную реакцию на ион свинца. Для этого нужно добавить в раствор йодид калия. При реакции со винцом выпадет ярко желтый осадок PbJ2.
3. Приведите примеры комплексных соединений олова и свинца. Какие координационные числа для них характерны?
Комплексные соединения:
- для олова
Na2[Sn(OH)6], Na2Sn(OH)4
- для свинца
Na2[Pb(OH)4]
Координационные числа :
- для свинца
4
- для олова
4 и 6
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.