При реагировании алюминия Al с щелочами реакция протекает очень бурно с выделением огромного количества водорода H2. Алюминий Al проявляет кислотные свойства.
Опыт 2.
а) Название эксперимента.
Взаимодействие алюминия с солями меди (II).
б) Ход эксперимента.
Поместим в три пробирки алюминий Al. В первую добавим 6 – 7 капель голубого раствора хлорида меди CuCl2, во вторую – 6 – 7 капель голубого раствора сульфата меди CuSO4, в третью – 6 – 7 капель голубого раствора нитрата меди Cu(NO3)2.
в) Наблюдения.
В пробирке с хлоридом меди CuCl2 и сульфатом меди реакция идет очень интенсивно, выделяется газ, образуется медная пленка. В последней нет никаких изменений.
г) Уравнения реакции.
2Al + 3CuCl2 = 2AlCl3 + 3Cu
Al0 - 3ē = Al+3 2 восстановитель
Cu+2 + 2ē = Cu0 3 окислитель
2Al + 3CuSO4 = Al2(SO4)3 + 3Cu
2Al0 - 6ē = Al2+3 1 восстановитель
Cu+2 + 2ē = Cu0 3 окислитель
2Al + 3Cu(NO3)2 = реакция не идет д) Иллюстрационный материал.
 |
|||||||
 |
|||||||
 |
|||||
е) Вывод.
Алюминий восстанавливает медь из растворов солей – хлоридов и сульфатов.
Опыт 3. Часть первая.
а) Название эксперимента.
Получение гидроксида алюминия и изучение его свойств.
б) Ход эксперимента.
В две ячейки капельного планшета поместим по капле бесцветного раствора хлорида алюминия (III) AlCl3. К каждой капле добавим по 1 капле бесцветного раствора гидроксида натрия NaOH.
в) Наблюдения.
Выпадает гелеобразный белый осадок.
г) Уравнения реакции.
AlCl3 + 3NaOH = Al(OH)3 ↓+ 3NaCl
При взаимодействии солей алюминия (III) с щелочами получается гидроксид алюминия (III) Al(OH)3.
ж) Ход эксперимента.
После этого к одной капле добавим 2 капли раствора соляной кислоты HCl, а ко второй еще 2 капли раствора гидроксида натрия NaOH.
з) Наблюдения.
В обеих ячейках осадок Al(OH)3 растворяется.
и) Уравнения реакции.
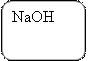
Al(OH)3 + 3HCl = AlCl3 + 3H2O
Al(OH)3 + NaOH = Na[Al(OH)4] → NaAlO2 + 2H2O
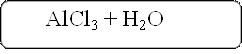 |
|||||||
 |
 |
 |
||||||||
л) Вывод.
Так как гидроксид алюминия (III) Al(OH)3 растворяется и в кислоте HCl и в щелочи NaOH, то он является амфотерным.
Опыт 3. Часть 2.
м) Ход эксперимента.
К полученному раствору алюмината натрия NaAlO2 добавим несколько кристалликов хлорида аммония NH4Cl.
н) Наблюдения.
Выпадает мутный осадок.
о) Уравнения реакции.
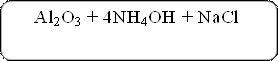
4Na[Al(OH)4] + 4NH4Cl + H2O ↔ 2Al2O3 + 4NH4OH + 4NaCl
![Na[Al(OH)4]](http://files3.vunivere.ru/workbase/00/05/94/22/images/image029.gif) |
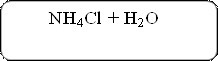 |
 |
|||||||
При взаимодействии алюмината натрия NaAlO2 и хлорида аммония NH4Cl происходит совместный гидролиз этих солей.
Опыт 4.
а) Название эксперимента.
Гидролиз соли алюминия.
б) Ход эксперимента.
В ячейку капельного планшета поместим 1 каплю раствора нейтрального лакмуса, добавим к ней несколько кристалликов сульфата алюминия Al2(SO4)3.
в) Наблюдения.
Цвет раствора меняется с фиолетового на розовый. г) Уравнения реакции.
Al2(SO4)3 + H2O = [Al(OH)2]SO4 + H2SO4
 |
|||||||
Гидролиз соли алюминия идет по катиону, по первой ступени. Реакция среды кислая.
Опыт 5.
а) Название эксперимента.
Влияние карбоната натрия на гидролиз соли алюминия.
б) Ход эксперимента.
В ячейку капельного планшета внесем 1 каплю хлорида алюминия AlCl3 и добавим 2 капле карбоната натрия Na2CO3.
в) Наблюдения.
Выпадает гелеобразный белый осадок.
г) Уравнения реакции.
2AlCl3 + 3Na2CO3 + 3H2O → 2Al(OH)3↓ + 3CO2↑ + 6NaCl
Карбонат натрия Na2CO3 усиливает гидролиз солей алюминия. Реакция среды щелочная.
Опыт 6.
а) Название эксперимента.
Получение гидроксида олова (II) и изучение его свойств.
б) Ход эксперимента.
В две ячейки капельного планшета поместим по капле хлорида олова (II) SnCl2. К каждой капле добавим по 1 капле раствора гидроксида натрия NaOH.
в) Наблюдения.
Выпадает белый осадок.
г) Уравнения реакции.
SnCl2 + 2NaOH = Sn(OH)2 ↓+ 2NaCl
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.