МИНИСТЕРСТВО ОБРАЗОВАНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
Учреждение образования
«Гомельский государственный университет имени Франциска Скорины»
Изучение электронного строения и
спектров
атомов щелочных металлов
Отчет о лабораторной работе
Выполнил:
студент группы ФТТ-32 Гордунов Д.С.
Гомель 2012
Цель работы: изучение основных закономерностей электронного строения и спектров щелочных металлов; определение величины дублетного расщепления спектральных термов, эффективного заряда и постоянной экранирования для атома щелочного металла.
Приборы и оборудование: спектрограф ИСП -30, микрофотометр МФ-4, атлас спектральных линий железа, спектропроектор ПС-18, набор электродов, соль натрия, фотопластинки и фотореактивы для их обработки.
Рабочие формулы:
![]() - разность частот;
- разность частот;
![]() – постоянная расщепления;
– постоянная расщепления;
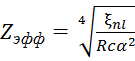 - эффективный заряд ядра;
- эффективный заряд ядра;
![]() - постоянная экранирования;
- постоянная экранирования;
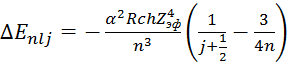 – величина расщепления;
– величина расщепления;
Выполнение работы:
1). Определим положение дублетной линии в спектре натрия относительно шкалы спектрографа. Найдем соответствующие длины волн λ1 и λ2:
3p ![]() 3s
λ1 = 588,99
3s
λ1 = 588,99 ![]() 10-9
м;
λ2 = 589,59
10-9
м;
λ2 = 589,59 ![]() 10-9
м;
10-9
м;
5s![]() 3p λ1 = 615,42
3p λ1 = 615,42![]() 10-9 м; λ2
= 616,07
10-9 м; λ2
= 616,07 ![]() 10-9
м;
10-9
м;
4d![]() 3p λ1 = 568,27
3p λ1 = 568,27![]() 10-9 м;
λ2 = 568,82
10-9 м;
λ2 = 568,82![]() 10-9
м;
10-9
м;
2). Рассчитаем
разность частот Δν наблюдаемых дублетов по формуле ![]() :
:
Δν1 = 518,34
![]() 109
с-1
109
с-1
Δν2 = 515,91
![]() 109с-1
109с-1
Δν3 = 515,09
![]() 109
с-1
109
с-1
3). На основании
результатов, полученных в пункте (2), найдем значение постоянной расщепления по
формуле ![]() :
:
![]() с-1
с-1
4). Пользуясь
формулой ![]() найдем значение эффективного заряда ядра Zэфф:
найдем значение эффективного заряда ядра Zэфф:
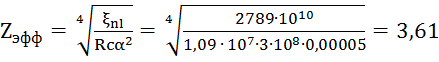
5). Зная значение эффективного заряда Zэфф найдем значение постоянной экранирования для атома натрия 11Na:
![]()
![]()
![]()
6). Рассчитаем величину расщепления 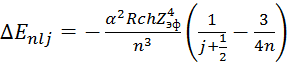
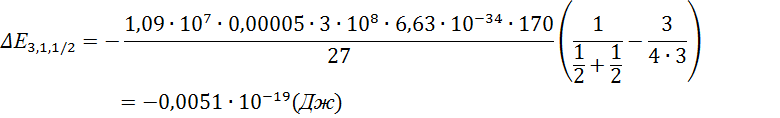
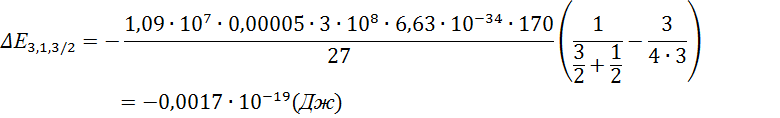
7).
Из формулы 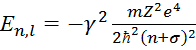 найдем величину квантового дефекта
σ:
найдем величину квантового дефекта
σ:
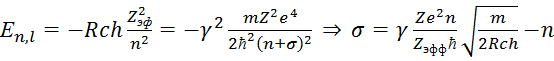
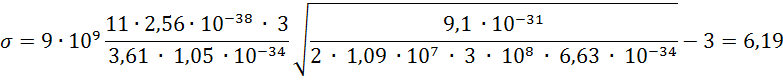
8). Зная
величину квантового дефекта и используя формулу ![]() определим численное значение коэффициента С1:
определим численное значение коэффициента С1:
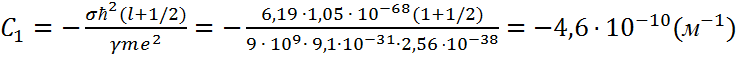
9). С учетом полученных результатов в пункте (8) запишем значение потенциальной энергии в дипольном приближении:
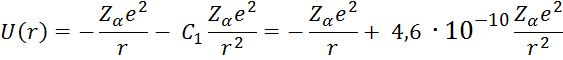
Вывод: Изучены
основные закономерности электронного строения и спектров щелочных металлов.
Каждая спектральная линия расщепляется на две – дублетное расщепление. Его
причиной является спин-орбитальное взаимодействие. Спектральная серия –
совокупность линий. С ростом частоты излучения линии сгущаются, а из
интенсивность уменьшается. Определены величины: постоянная расщепления ξ31=2789
![]() 1010;
эффективный заряд Zэфф=3,61
и постоянная экранирования а =
7,39;
квантовый дефект σ=6,19.
1010;
эффективный заряд Zэфф=3,61
и постоянная экранирования а =
7,39;
квантовый дефект σ=6,19.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.