 |
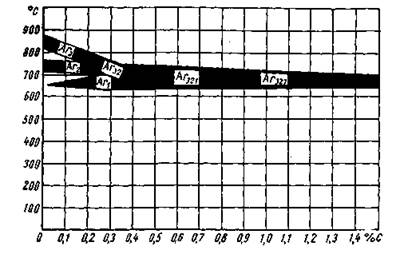
Рис. 10.
Однако первые попытки построения полной диаграммы железо—углерод предпринял только Робертс-Аустен [241, 2551 в 1897— 1899гг,
Диаграмму Робертса-Аустена 1897 г. многие позднейшие авторы считали фактически первой диаграммой железо — углерод.
VII. ДАЛЬНЕЙШИЕ ИССЛЕДОВАНИЯ
КОЛИЧЕСТВЕННОЙ СТОРОНЫ СОСУЩЕСТВОВАНИЯ ЖЕЛЕЗА С УГЛЕРОДОМ В СПЛАВАХ Fe — С
И ОПРЕДЕЛЕНИЕ ФОРМУЛЫ КАРБИДА ЖЕЛЕЗА
Начатые Карстеном [41, 47] в двадцатых годах 19 в. исследования видов углерода в сплавах Fe —С, продолженные в дальнейшем многими учеными, главным образом Бертье [54], Каро-ном [77] и Ринманом [89], не привели еще к определению вида связанного углерода. Формулы, приписываемые некоторыми исследователями, например Карстеном [47] и Бертье [54], якобы выделенному карбиду, были позднее ими же самими поставлены под сомнение [61, 55]. Через некоторое время было принято, что существуют карбиды Fe4C и Fe8C; Гурлит [65] считал, что серый чугун содержит карбид Fe8C и графит, а белый чугун — только карбид Fe4C, который при повышенных температурах может превращаться в карбид Fe8C и графит. По мнению Таннера [90], в сплавах с низким содержанием углерода должен присутствовать карбид Fe4C, смешанный с чистым железом. В 1875 г. Буссинголт [97] на основе своих химических опытов над белыми чугунами, полученными из шведского железа и древесного угля, приписал карбиду, заключенному в этих сплавах, формулу Fe5C.
Насколько неуверенными были вышеуказанные формулы, свидетельствует лучше всего тот факт, что Труст и Хаутефюиль [99], проводя в 1875 г. калориметрические исследования по определению теплоты образования карбида железа и карбида марганца, не приписывали карбиду железа никакой формулы, в то время как карбид марганца представляли формулой Мп3С.
С 1860 г. исследователи всесторонне занимались проблемой растворимости углерода в жидком железе, при этом было замечено, что растворимость углерода не является неограниченной, т. е. железо и углерод не могут давать непрерывного ряда растворов от чистого железа до чистого углерода. Содержание 5,95% С, данное в 1844 г. Карстеном, известный английский металлург Перси считал слишком высоким [81]. Дик [83] обнаружил углерод в количестве 4,56%, Райли [104] — 4,75%, Хохстэттер [82] и Перси [81] —4,63%, Маннесман [ПО] — 4,76%, а Санитер [243] — 4,81%. Эти ученые, однако, не указывали температур, при которых наблюдалась такая растворимость, в результате чего их данные не представляли для диаграммы железо — углерод особой ценности, так как, по утверждению Муасанна [271], растворимость углерода в железе зависит от температуры. Проводя плавки при высоких температурах в электропечи, Муасанн пришел к выводу, что при температуре вольтовой дуги (около 3500° С) в железе может раствориться до 40% углерода. Кроме того, эти исследователи, за исключением Санитера [243], не учитывали влияния кремния и марганца на растворимость углерода в железе.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.