




1. Универсальной мерой для любых веществ (не зависимо от их вида) является масса m, измеряемая [ кг ]; [ г ]; [ т ]; [ мг ] и т.д.
2. Количество жидкости может быть измерено величинами массы (m ) и объема (V). Единицы измерения объема – [м3]; [л]; [мл] (“литр” – специальное название кубического дециметра.)
[см3]=[мл]. Переход от массы к объёму (или от объёма к массе) осуществляется через плотность r - массу единицы объёма раствора:
r = m/V [г/мл]; m = r ·V; V = m/r.
Моль – Авогадрово число (6,02×1023) частиц данного вида;
количество граммов вещества, численно равное атомной или молекулярной массе данного вещества.
Обозначается М(В), где В – вид вещества, о количестве которого идет речь.
Молекулярные массы (Мr) сложных веществ вычисляются с использованием округленных целочисленных значений атомных масс элементов (Аr) из Таблицы Д.И. Менделеева, где они приведены в [а.е.м.] – в атомных единицах массы (1/12 массы атома изотопа 126С).
Термин “моль “ – не склоняется: 2 моль; 5 моль; 0,1 моль и т.д.
3.2.1. Специфически химический способ измерения количества вещества – числом моль n(в) = m(в) /М(в).
Соответствующие пересчёты осуществляются по формулам:
m(в) =n(в)× M(в); M(в) = m(в) / n(в).
3.2.1. Для газов используется измерение их количества числом мольных объёмов (при н.у. 22,4 л/моль – следствие закона А. Авогадро).
n(газа)=V0(газа) / 22,4; V(газа)= n(газа)·22,4;
(Здесь V0 –объём газа, измеренный при нормальных условиях – 00С и 1 атм).
3.2.2.Количество вещества может быть измерено:
(а) числом частиц (атомов, молекул);
(б) числом моль этого вещества;
(в) числом граммов ([кг] и т. д.);
(г) числом мольных объёмов газа (см. табл.3).
Подстрочный индекс “r” в символах Аr и Мr – первая буква лат. relative - относительный, - соответственно, относительные атомная и молекулярная массы. Следует подчеркнуть, что при измерении количества вещества числом моль обязательно указывается вид вещества, о количестве которого идет речь, т.к. молярная масса у каждого вещества – своя.
Мольный объём газа – универсальная мера количества любого газа.
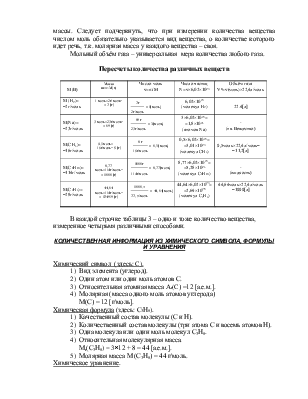
Пересчеты количества различных веществ
|
М(В) |
Масса m=n×M(в) |
Число моль n=m/M |
Число частиц N=n´6,02´1023 |
Объём газа V0=n(моль)´22,4л/моль |
|
М (Н2)= =2г/моль |
1 моль´2г/моль= = 2 [г] |
|
6,02´1023 (молекул Н2) |
22.4[л] |
|
М(Na)= =23г/моль |
3 моль´23г/моль= = 69 [г] |
|
3´6,02´1023= =1,8´1024 (атомов Na) |
- (тв. Вещество) |
|
М(СН4)= =16г/моль |
0,5 моль´ 16г/моль= 8 [г] |
|
0,5´6,02´1023= =3,01´1023 (молекул СН4) |
0,5моль´22,4л/моль= =11,2[л] |
|
М(С8Н18)= =114г/моль |
8,77 моль´114г/моль= = 1000 [г] |
|
8,77´6,02´1023= =5,28´1024 (молекул С8Н18) |
- (жидкость) |
|
М(С2Н4)= =28г/моль |
44,64 моль´114г/моль= = 1249/9 [г] |
|
44,64´6,02´1023= =2,69´1025 (молекул С2Н4) |
44,64моль´22,4л/моль=1000[л] |
В каждой строчке таблицы 3 – одно и тоже количество вещества, измеренное четырьмя различными способами.
Химический символ (здесь: C).
1) Вид элемента (углерод).
2) Один атом или один моль атомов С.
3) Относительная атомная масса Аr(C) =12 [а.е.м.].
4) Молярная (масса одного моль атомов углерода)
М(С) = 12 [г/моль].
Химическая формула (здесь: С3Н8).
1) Качественный состав молекулы (С и Н).
2) Количественный состав молекулы (три атома С и восемь атомов Н).
3) Одна молекула или один моль молекул С3Н8.
4) Относительная молекулярная масса.
Мr(С3Н8) = 3´12 + 8 = 44 [а.е.м.].
5) Молярная масса М (С3Н8) = 44 г/моль.
Химическое уравнение.
С3Н8 + 5 О2 = 3СО2 + 4Н2О(ж).
1) Вид реагентов (С3Н8 и О2) и вид продуктов (СО2 и Н2О) реакции.
2) Количественное их соотношение по числу молекул и по числу моль ( один С3Н8 и пять О2; три СО2 и четыре Н2О).
3) Демонстрация закона сохранения массы:
44 г (С3Н8) + 5´32г (О2) = 3´44г (СО2) + 4´18г (Н2О)
204г реагентов = 204г продуктов
Эти расчеты проводятся путем составления и последующего решения х и м и ч е с к о й п р о п о р ц и и:
1я строка - сведения из химической формулы или уравнения.
2я строка - искомая величина (х) и цифра из условия задачи.
При составлении пропорции соблюдаются два условия:
а) Друг под другом в пропорции должны стоять цифры, относящиеся к одному и тому же веществу;
б) У этих цифр (стоящих в пропорции друг под другом) должны быть одинаковые размерности.
Желательно перед решением задачи сделать компактную запись условия, включив в перечень данных величин молярные массы тех участников реакции, о массах которых идет речь в условии. Ответы удобно показать в компактной записи условия.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.