УДК 621.383.1.
ФОТОКОЛОРИМЕТРЫ
Нефёдова А.А., Королёва О.Г., Концелярчик А.И., Тамилович Т.М.
Научный руководитель – МИХАЛЬЦЕВИЧ Г.А.
Фотоколориметрический метод анализа – один из самых распространенных методов физико-химического анализа, основан на измерении поглощения электромагнитного излучения видимого диапазона (400-750 нм) прозрачными растворами веществ. Он также характеризуется сравнительной простотой средств измерения и наличием большого количества реагентов, образующих окрашенные соединения с неорганическими и органическими веществами.
Количественно поглощение электромагнитного излучения веществом описывается уравнением основного закона светопоглощения (уравнением закона Бугера-Ламберта-Бэра) и уравнением закона аддитивности оптических плотностей [1]. Согласно основному закону светопоглощения, интесивность света, прошедшего через вещество, выражается уравнением
Iпр = Io* 10 -kcl
где Iпр – интенсивность светового потока, прошедшего через раствор;
I0– интенсивность падающего светового потока;
k– коэффициент поглощения света;
с – концентрация вещества в растворе;
l – толщина слоя светопоглощающего раствора (ширина кюветы).
Коэффициент поглощения света k зависит от природы вещества, температуры и рН-раствора, значит, это величина непостоянная.
Для характеристики поглощения света веществами используют величину пропускания Т [1], которая показывает, какая часть света прошла через раствор, и определяется как:
T = Iпр/ Io,
а также величину, которую называют оптической плотностью раствора, обозначают буквой А (логарифмированное уравнение закона Бугера-Ламберта-Бера) и определяют как:
A = k*l*c = –lgT
Если концентрация поглощающих частиц выражена в моль/дм3, а толщина слоя – в сантиметрах, то коэффициент поглощения обозначается буквой ε и называется молярным коэффициентом поглощения. Он характеризует способность вещества поглощать свет. Его размерность – дм3 • моль-1 • см-1, а численное значение равно оптической плотности раствора с концентрацией 1 моль/дм3 при толщине поглощающего слоя 1 см. Тогда общепринятая форма записи уравнения основного закона светопоглощения выглядит, как:
A = ε *l*c.
Графически зависимость оптической плотности от концентрации выражается прямой, проходящей через начало координат, если соблюдаются ряд условий:
1. Раствор поглощающего вещества – гомогенная нерассеивающая среда.
2. Монохроматичность падающего света.
3. При данной длине волны поглощает только один тип частиц.
4. Растворитель оптически прозрачен, т.е. не поглощает.
5. В растворе не протекают побочные реакции, изменяющие концентрацию поглощающих частиц.
6. На поглощающие частицы не оказывают влияние ни растворитель, ни ионные силы раствора.
Важным дополнением к основному закона светопоглощения является закон аддитивности оптических плотностей. Если в растворе присутствуют несколько поглощающих веществ, то оптическая плотность раствора равна сумме вкладов каждого из компонентов:
A = ε 1*11*c1 + ε 2*l2*c2 + … + ε n*ln*cn
Измерение оптической плотности производят на приборах - фотоколориметрах. Принципиальную схему фотоколориметра можно представить как на рисунке 1 [2].
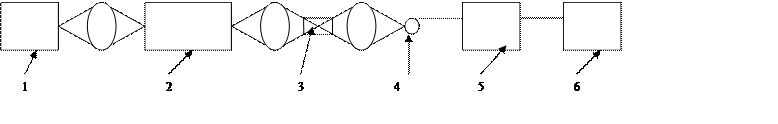
Рисунок 1. Схема однолучевого фотоколориметра:
1 - источник света; 2 - светофильтр; 3 - кюветное отделение; 4 - фотоприемник; 5- усилитель; 6 - индикатор выходного сигнала.
В качестве источника излучения применяют обычные лампы накаливания с вольфрамовой нитью или галогенокварцевые. Эти источники излучают в широкой области спектра, поэтому излучение нужно монохроматизировать. Для выделения определенного интерн вала длин волн в фотоколориметрах используют
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.