






окислительному обжигу относится и агломерирующий обжиг (обжиг со спеканием), при котором сульфидный материал одновременно окисляется и превращается в прочный кусковый продукт – агломерат. Применяются и некоторые другие виды обжига.
2.2.1.2. плавка
Пирометаллургический процесс, проводимый в плавильных печах при температурах, обеспечивающих получение продуктов плавки в расплавленном состоянии. Различают две разновидности плавки, рудную и рафинировочную.
2.2.1.2.1. рудная плавка
Рудная плавка подразделяется на следующие виды:
1. Восстановительная плавка – процесс получение металлов за счет восстановления его оксидов углеродистыми восстановителями или водородом и перевода пустой породы в шлак. Этим способом получают многие металлы – свинец, олово и. т. д. Реакцию восстановления оксидов металла углеродом, например, оксида свинца, можно записать следующим уравнением:
PbО + С = Рb + СО.
Подобные реакции идут вправо – в сторону восстановления металла, если прочность химической связи кислорода с углеродом в оксиде углерода больше прочности связи кислорода с металлом. Прочность химических связей называют сродством и характеризуют в химической термодинамике величиной изобарно–изотермического потенциала, обозначаемого символом ∆Z. Изобарный потенциал измеряют в джоулях. Физический смысл его – максимальная работа, которую может совершить реакция. Эту работу условно считают отрицательной, поэтому отрицательная величина ∆Z указывает на работоспособность реакции – возможность самопроизвольного ее протекания.
Сродство какого-либо элемента к кислороду или сере (изобарный потенциал образования оксида или сульфида) зависит от температуры. Эта зависимость выражается уравнением вида:
∆Z = A + BТ lgT+CT+…,
где А, В, С – коэффициенты, определяемые из опыта; Т – абсолютная температура, °К.
Зависимость сродства от температуры по этим уравнениям можно представить графически, как это сделано на (рис. 4), где величина ∆Z дана на один моль кислорода, участвующего в реакции образования оксида. Воспользовавшись графиком, вычислим изобарный потенциал реакции восстановления оксида свинца углеродом при 800° С.
Восстановление PbО можно представить разностью двух реакций – II и I:
I. 2С + О2 = 2СО • • • ∆ZCO
II. 2Рb + О2 = 2РbО • • • ∆Z РbО
![]()
2РbО + 2C = 2Pb + 2CO
∆Z = ∆ZСО – ∆ZРbО.
По графику рис. 4 находим:
∆Z PbО = – 250 кДж; ∆ZCO = – 400 кДж; ∆Z = – 400 + 250 = – 150 кДж.
Разность получилась отрицательной, следовательно, реакция пойдет вправо, свинец будет восстанавливаться. Линии РbО и СО на рис. 4 пересекаются при температуре около 320 °С. За точкой пересечения влево разность сродства окажется положительной, эта точка определяет температуру начала восстановления свинца углеродом.
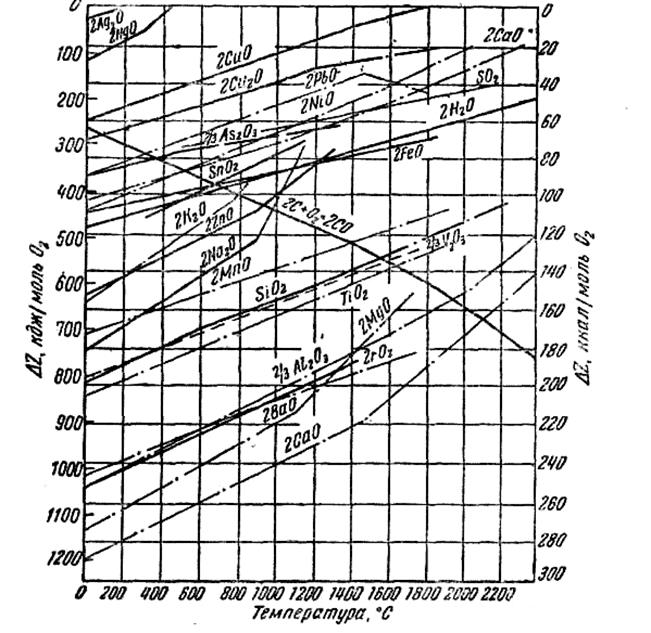
Рис. 4. Стандартные изобарные потенциалы образования окислов
Так же по точкам пересечения соответствующих линии можно определить температуры начала восстановления углеродом других оксидов. Для SiO2, Al2O3, CaO, MgO они выше 1500 °С.
Следовательно, можно выбрать такие температуры, при которых одни оксиды восстанавливаются до металла, а другие остаются неизменными. На этом основана, например, выплавка свинца из руд, содержащих SiO2, FeO, CaO и Аl2О3. При плавке руды с коксом восстанавливается только свинец, имеющий сравнительно малое сродство к кислороду. Другие оксиды сплавляются в жидкий шлак. Шлак с плотностью 3000–3500 кг/м3 всплывает над жидким свинцом (γ 10000 кг/м3) подобно тому, как слой масла всплывает над водой. Очень важна скорость восстановления: металлургические переделы должны быть производительными, а для этого
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.