







Определить расходы топлива В, кг/с (м3/с), окислителя Vок, м3/с, и воздуха, идущего на разбавление продуктов сгорания топлива Vв, м3/с, необходимые для получения заданного количества энергоносителя Vэ = 4,5 м3/с, имеющего температуру Тэ = 1150 К. Определить составы газов за камерой смешения, а также температуру газа после камеры сгорания Тксг, К.
В качестве окислителя и воздуха, подаваемого для разбавления продуктов сгорания, принять воздух О2 = 21%, N2 = 79% с температурой Тв = Ток = 300 К и влагосодержанием dв = dок =15 г/м3.
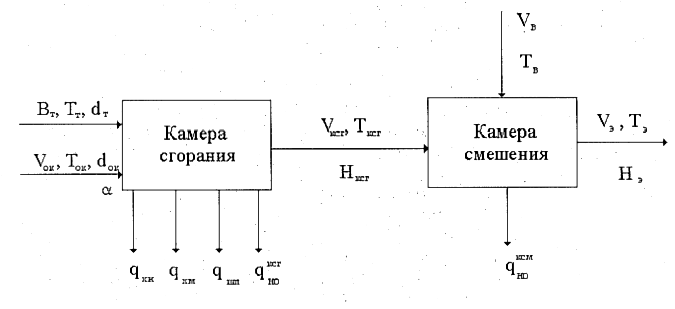
Схема движения теплоносителей.
Исходные данные:
- топливо – Газ генераторный водяной: (об. %) CO — 44, N2 — 6, CO2 — 5, H2 — 45.
- тепловые потери:
с химическим недожогом qхн = 0,5%;
а) через наружные ограждения камеры сгорания qноксг = 5%;
б) через наружные ограждения камеры смешения qноксм = 8%;
- коэффициент расхода окислителя α = 1,15.
Решение:
1.Определение низшей теплота сгорания 1 м3 топлива (генераторного водяного газа).
QHC=0,01*(CO*QCO+H2*QH2) = 0,01*(44*12,636 + 45*10,743) = 10,403 МДж/м3
где QCO, QH2 – теплота сгорания оксида углерода и водорода МДж/м3;
CO, H2 - содержание оксида углерода и водорода в генераторном газе, %об.
2. Расчёт теоретического расхода окислителя и теоретического выхода продуктов полного сгорания топлива.
Теоретический расход окислителя:
VOK0 = VO20*100/O2OK,
где O2OK – концентрация кислорода в окислителе, O2OK = 21% об;
VO20- теоретический расход кислорода, необходимый для полного сгорания 1 м3 газообразного топлива, м3/м3.
Для генераторного газа:
VO20 = 0,5*(H2 + CO)/100 = 0,5*(45 + 44)/100 = 0,445 м3/м3.
где CO, H2 - концентрация составляющих газового топлива, % об.
VOK0 = 0,445*100/21 = 2,12 м3/м3.
Суммарный теоретический выход продуктов полного сгорания:
Vксг0 = VRO20 + VN20 + VH2O0;
где VRO20 – теоретический выход сухих трёхатомных газов с учётом СО2, содержащегося в топливе;
VN20 - теоретический выход азота, определяемый в зависимости от содержания азота в газовом топливе и окислителе;
VH2O0 – теоретический выход водяных паров с учётом влагосодержания окислителя..
VRO20 = VCO2 = 0,01*(CO + CO2) = 0,01*(44+5) = 0,49 м3/м3;
VN20 = 0,01*(N2 + VOK0*N2OK) = 0,01*(6 + 2,12*79) = 1,74 м3/м3;
VH2O0 = 0,01*H2 + 0,00124* VOK0*dOK = 0,01*45+0,00124*2,12*15=0,489 м3/м3;
Vксг0 = 0,49 + 1,74 + 0,489 = 2,719 м3/м3.
3. Расчёт действительного расхода окислителя и действительного выхода продуктов полного сгорания топлива.
Действительный расход окислителя:
VOK = α* VOK0 = 1,15*2,12 = 2,438 м3/м3,
где α – коэффициент расхода окислителя.
Суммарный действительный выход продуктов полного сгорания:
Vксг = VRO2 + VN2 + VH2O + VО2,
где VRO2 = VRO20 - действительный выход сухих трёхатомных газов;
VN2 - действительный выход азота;
VH2O – действительный выход водяных паров;
VО2 – содержание кислорода в продуктах сгорания.
VN2 = 0,01*(N2 + α*VOK0*N2OK) = 0,01*(6 + 1,15*2,12*79) = 1,99 м3/м3;
VH2O = 0,01*H2 + 0,00124* α*VOK0*dOK = 0,01*45+0,00124*1,15*2,12*15=0,496 м3/м3;
VО2 = (α – 1)* VOK0*О2ОК/100 = (1,15 – 1)*2,12*21/100 = 0,067 м3/м3;
Vксг0 = 0,49 + 1,99 + 0,067 + 0,496 = 3,043 м3/м3.
4. Определение температуры газов после камеры сгорания.
Воспользуемся уравнением теплового баланса камеры сгорания:
(QHC + QOK)*[(100 – (qхн + qноксг)]/100 = Hксг,
где QHC – низшая теплота сгорания топлива;
QOK – тепло подогретого окислителя;
qхн – потери тепла с химическим недожогом, %;
qноксг – потери тепла через наружные ограждения камеры горения %;
Hксг – энтальпия продуктов сгорания.
QOK = VOK *СОК*tOK = 2,438*1,307*27 = 86,035 кДж/м3,
где СОК – объёмная теплоёмкость окислителя при tOK = 270С.
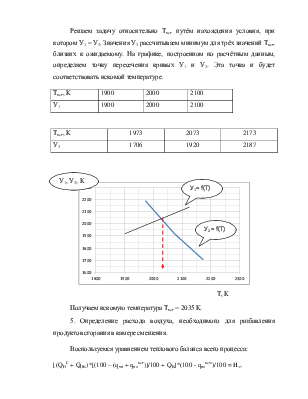
В явном виде уравнение баланса камеры сгорания не решается, так как входящие в это уравнение теплоёмкости продуктов сгорания сами являются функцией температуры Тксг. Определим Тксг, используя графоаналитический метод. Для этого выразим из уравнения баланса Тксг:
Тксг = {[(QHC + QOK)*[(100 – (qхн + qноксг)]/100]/[ VRO2*CRO2 + VN2*CN2 + +VH2O*CH2O + VО2* CO2} + 273,
где Сi – объёмная теплоёмкость i-го компонента продуктов сгорания
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.