











Охтирський технікум СНАУ
ЛЕКЦІЯ № 3
(Тематична)
Навчальна дисципліна – ГКА.
Тема лекції: Водяна пара, витікання та дроселювання
газів і пари. Способи розповсюдження тепла.
Для студентів ІІІ курсу, спеціальність 5. 092123.
Тривалість – 65 хв.
План
викладення лекційного матеріалу
1. Процес пароутворення. Насичена та суха пара.
2. І-sдіаграма водяної пари.
3. Поняття про витікання газів і пари. Критична швидкість. Сопло Лаваля. Процес дроселювання газів і пари.
4.Способи розповсюдження тепла :теплопровідність, конвективний теплообмін, теплообмін випромінюванням.
Викладач: Пугачов О.О.
Розглянуто і схвалено на засіданні предметної циклової
комісії спеціальних дисциплін (спеціальність 5. 092123)
протокол №від „ „ 2004 р.
Голова циклової комісії Пугачов О.О.
1. Процес пароутворення. Насичена та суха пара.
В якості робочого тіла в багатьох теплотехнічних апаратах застосовується водяна пара. А чому? Та тому, що, по своїм властивостям вона наближається до реальних газів і до неї можливо застосування газових законів. А по-друге її легко видобувати і вона не шкідлива для оточуючого середовища.
Пару отримують з води в спеціальних теплотехнічних апаратах, які називають паровими котлами. Процес утворення пари з води називають пароутворенням. Він відбувається при постійному тиску.
Розглянемо його більш детальніше. Якщо взяти циліндр, який закрито з одного боку (з низу) і налити в нього 1 кг води при температурі 0˚С, а зверху вставити поршень з постійним навантаженням (тиск на воду постійний –Р1).
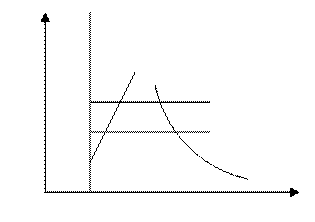 Почнімо його підігрівати . Як і любе тіло, так і вода
при нагріванні розширяється, тобто об’єм води незначно збільшиться.
Почнімо його підігрівати . Як і любе тіло, так і вода
при нагріванні розширяється, тобто об’єм води незначно збільшиться.
Розглядаючи стан цієї води в Р-V діаграмі відмітимо це збільшення крапкою аІ. Якщо продовжувати підводити тепло то вода через деякий час закипить (тобто частина її перейди в газоподібний стан). Такий процес буде продовжуватися до точки аІІ. Об’єм збільшиться значно. Від крапки аІ до крапки аІІ в циліндрі буде суміш води і пари. Якщо продовжувати підводити тепло і далі, то об’єм зростатиме значно і в циліндрі, після крапки аІІ відбувається динамічна рівновага – кількість пари яка утворюється, дорівнює кількості пари яка конденсується. Цей стан , є станом насиченої пари.
Якщо збільшити навантаження на поршень до Р2 і повторити процес нагрівання цієї ж води, то на діаграмі він буде відображений прямою в - вІІ. Таким чином, змінюючи величину тиску, можливо побудувати ряд крапок, і якщо їх з’єднати (з однаковими показниками) отримаємо криві. При підвищенні тиску криві зближуються, і з’єднаються в точці К. Це вказує на те що, при досягненні якогось значення тиску, вода перетворюється повністю на пару, не утворюючи насиченої пари. Точку К називають критичною, а параметри води і пари критичними. Пара, яка знаходиться на кривій аІІ - вІІ, не має зовсім крапель вологи і тому вона називається сухою. Масова доля сухої пари в вологому називають ступінню сухості і позначають – Х. Доля води в вологі парі називається ступеню вологості і дорівнює 1 – Х.
А пара, у якої температура і питомий об’єм більші ніж у сухої, називається перегрітою. Перегріта пара не може знаходитись в рівноважному стані з водою, з якої вона утворилася, і при ізотермічному змінені її об’єму призводить до змінення тиску. Вона не насичує простір в якому вона знаходиться. Тому її називають ненасиченою.
Аналогічно можливо побудувати і Т-s діаграму. Вона має ідентичний вигляд. Користуючись Т-s діаграмою, можливо визначати кількість теплоти, яка підводилась або відводилась при відповідному процесі.
2. І-sдіаграма водяної пари.
Значення ентальпії та температури для ідеального газу - пропорційні, і тому для розрахунків використовується не Т- s, а І – s діаграма водяної пари. В діаграмі по вісі абсцис відкладено значення ентропії s, а по вісі ординат – значення ентальпії І. Ентропія вимірюється в кДж/(кг·˚К), а ентальпії в кДж/кг. ( Запропонувати звернути увагу на плакат!)
На діаграмі в області насичення ізобари і ізотерми співпадають і мають вигляд прямої лінії. В області перегрітої пари ізобари і ізотерми розходяться і представляють собою криві лінії. По мірі віддалення від області насичення до області перегріву ізотерми асимптотично приближаються до горизонталі, а ізобари по своєму вигляду наближуються до логарифмічних кривих. Такий характер ізобар та ізотерм в області перегріву об’яснюється тим, що по мірі віддалення від області насичення властивості водяної пари наближаються до властивостей ідеального газу.
На діаграмі І – s зворотній адіабатний процес відображено відрізком вертикальної прямої (s =const), а кількість теплоти в ізобарному процесі відображається на ній проекцією відрізку ізобари на вісь ординат. На діаграмі також нанесені криві однакової сухості.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.