Перекристаллизовать препарат из ацетона и определить температуру плавления комплекса.
В мерных колбах емкостью 50 мл каждая приготовить 10-2 М и 5•10-2 М спиртовые растворы комплекса. Снять электронный спектр поглощения растворов в области 350-800 нм и рассчитать молярный коэффициент экстинции максимумов полос поглощения.
Снять ИК – спектр соединения в интервале 400-3600 см -1. Найти характеристические полосы поглощения.
Приборы и реактивы
o оксид ванадия (V) – 2,5 г;
o 96 %-ый раствор серной кислоты – 6 мл;
o этанол – 25 мл;
o ацетилацетон – 6 мл;
o безводный карбонат натрия – 10 г;
o дистиллированная вода;
o ледяная вода.
Экспериментальная часть
1. Поместила в стакан V2O5 m=2,5 г (оранжевого цвета), добавила 12,5 мл воды, 6 мл 96%-го раствора H2SO4 и 25 мл этанола.
Реакция:
2V2O5 + 4H2SO4 = 4VOSO4 + O2 + 4H2O
2. Поставила стакан на электроплитку и нагрела смесь до кипения при постоянном перемешивании. Далее продолжала нагревание в течение 30 минут. При этом цвет раствора от оранжевого становился светло-зеленым, а по окончании восстановления - темно-синим. В процессе нагревания поддерживала постоянный объем реакционной смеси, добавляя дистиллированную воду. Затем раствор профильтровала через бумажный фильтр «красная лента». К фильтрату добавила 6 мл ацетилацетона.
Реакция:
VOSO4 + 2HAcac = [VO(acac)2] + H2SO4
3. Поместила стакан со смесью на магнитную мешалку. Приготовила раствор: 10 г Na2CO3 на 63 мл воды. При постоянном перемешивании добавляла из капельной воронки приготовленный раствор соли, для нейтрализации серной кислоты, избегая вспенивания.
Реакция:
Na2CO3 + H2SO4 = Na2SO4 + CO2↑ + H2O
Получила бирюзовый осадок, профильтровала его на воронке Бюхнера, промыла не большим количеством ледяной воды и высушила на воздухе.
Структурная формула вещества:
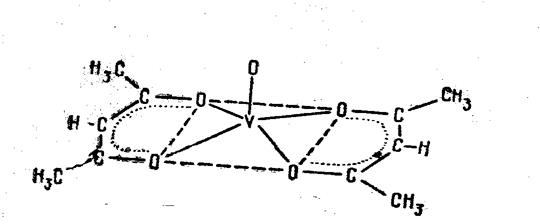
Бис – (ацетилацетонато) ванадил имеет форму квадратной пирамиды. К.Ч.=5.
4. Взвесила полученное вещество: m=5,06 г
5. Рассчитала выход продукта в процентах по отношению к теоретическому:
Теоретический выход: М ([VO(acac)2])=265 г/моль
ν ([VO(acac)2])= 0,02 моль
=>m (теор.)=5,3 г
Выход продукта составил: m (реал.)/m (теор.)*100 %=5,06 г/5,3 г *100 %=95,5 %
6. Провела исследование полученного вещества
Методы исследования
1. Для идентификации вещества и определения его строения сняла ИК – спектр 400-3600 см-1 (см. приложение). Из полученного спектра можно выделить следующие характеристические полосы поглощения:
Экспериментальные данные практически совпадают с данными из атласа. Следовательно, было получено искомое вещество: [VO(acac)2].
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.