В плоскости XY проекции дипольных моментов равномерно распределены по кругу, поэтому
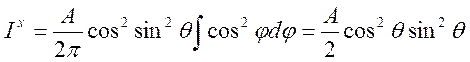 .
.
Таким образом,
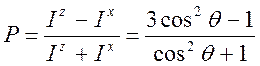 . При cos2q = 1/3 P = 0. Угол q = 54.740 – угол
Брюстера.
. При cos2q = 1/3 P = 0. Угол q = 54.740 – угол
Брюстера.
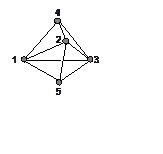
5. (400) Определить основной терм, энергии и поляризацию переходов для радикала H5, имеющего строение D3h. На рисунке указаны связи. Все резонансные интегралы считать одинаковыми.
Решение: Можно показать, что в группе D3h атомные орбитали водородов реализуют НП 2а1', a2'' и e'. Комбинации, преобразующиеся по этим представлениям имеют вид
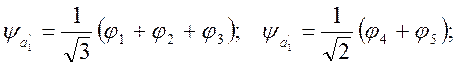
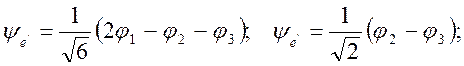
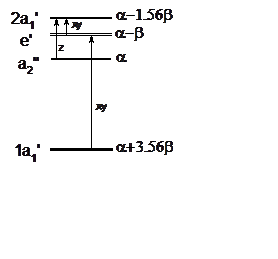
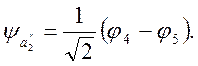 Детерминант для НП а1'
имеет вид
Детерминант для НП а1'
имеет вид 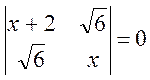 , корни которого равны
, корни которого равны ![]() Энергии орбиталей e' и a2''
равны a-b и a. На рисунке показано расположение и энергии МО, а также поляризация и
положение линий поглощения, которые определяются правилами отбора. Основной
терм радикала – 2E'.
Энергии орбиталей e' и a2''
равны a-b и a. На рисунке показано расположение и энергии МО, а также поляризация и
положение линий поглощения, которые определяются правилами отбора. Основной
терм радикала – 2E'.
Задачи на контрольную 7 апреля 2002. Группы 941-942-943-843
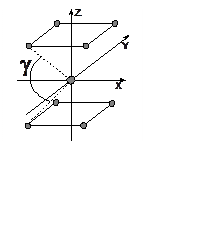
1. (600) Для комплекса MX8 (ион с 3d1 электронной конфигурацией, группа симметрии D4h) найти зависимость расстояния между dxy и dx2-y2 орбиталями от угла (см. рисунок).
Решение:
В группе D4h в потенциал кристаллического поля войдут гармоники Y00, Y20, Y40, (Y44+Y4-4). После определения угловых координат лигандов и замены гармоник на эквивалентные операторы оператор кристаллического поля приобретает вид (член V00 = 8eq/a от гармоники Y00 опускаем)
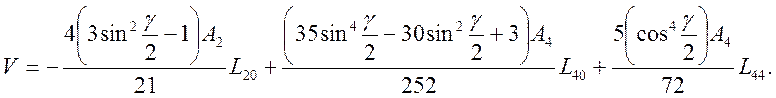
где
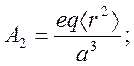
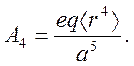
Расстояние между орбиталями dxy и dx2-y2 определяется недиагональным матричным элементом между гармоникам Y22 и Y2-2 , определяемым оператором L44.
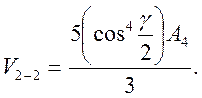
Расщепление между орбиталями dxy и dx2-y2 равно 2V2-2
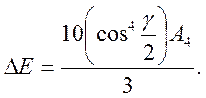
При
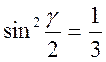 комплекс имеет строение куба, который
можно рассматривать как два вложенных друг в друга тетраэдра. В этом случае
расстояние между орбиталями dxy и dx2-y2
комплекс имеет строение куба, который
можно рассматривать как два вложенных друг в друга тетраэдра. В этом случае
расстояние между орбиталями dxy и dx2-y2
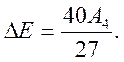
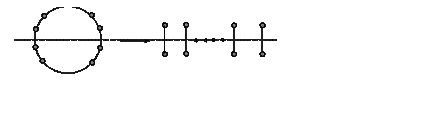
2. (300) Определить разрешенность по симметрии реакции распада плоской циклической молекулы на n молекул водорода (H2n ® nH2, см. рисунок).
 Решение: Если
выбрать в качестве элемента симметрии плоскость, перпендикулярную плоскости
исходной циклической молекулы, среди ее связывающих орбиталей будут и
антисимметричные. Для конечного состояния молекул водорода антисимметричные
орбитали будут только среди разрыхляющих. Таким образом, реакция запрещена для
реализации термическим способом.
Решение: Если
выбрать в качестве элемента симметрии плоскость, перпендикулярную плоскости
исходной циклической молекулы, среди ее связывающих орбиталей будут и
антисимметричные. Для конечного состояния молекул водорода антисимметричные
орбитали будут только среди разрыхляющих. Таким образом, реакция запрещена для
реализации термическим способом.
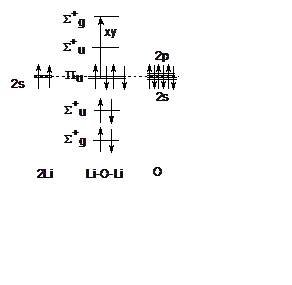
3. (400) Для линейной молекулы Li-O-Li указать поляризацию и энергию перехода S0 ® S1. Считать, что ось молекулы является осью Z. Кулоновские интегралы орбиталей 2s, 2p кислорода и 2s лития считать одинаковыми. Резонансный интеграл 2sLi-2sO в два раза больше резонансного интеграла 2sLi-2pO. Указать термы, между которыми происходит переход.
Решение: На рисунке изображены орбитали молекулы и приведена их симметрия. Основной терм S0 - 1Sg+ ввиду заполнения электронами орбиталей. Возбужденный, нижний по энергии, терм S1 1u типа. Так как в группе D¥h компоненты дипольного момента dx и dy преобразуются также по u представлению, переход поляризован вдоль осей XY. Энергия перехода равна DE = b2sLi-2sO.
4. (300) Шарообразные молекулы радиусом 10 А плотноупакованным мономолекулярным слоем находятся на поверхности кварцевой пластинки. Молекулы имеют полосу поглощения с коэффициентом экстинкции в ее максимуме e = 6´105 л/моль´см. Определить оптическую плотность такой пластинки в на длине волны максимума полосы поглощения. Считать, что кварц не поглощает и не отражает свет.
Решение: Сечение поглощения молекулой равно s = e/N0 = 10-15 см2. Площадь, занимаемая молекулой на пластинке, равна S = (2R)2 = 4´10-14 см2. Доля поглощенного света
Iпогл/I0 = (1 – 10-D) = (1 - exp(-2.3´D)) = s/S = 1/40.
Оптическая плотность будет небольшой (D << 1), поэтому экспоненту можно разложить в ряд и получить
D = 1/(2.3´40) = 0.0108
5. (400) Определить энергии и поляризацию переходов для комплекса TiH43+ (ион Ti3+ - 3d1 электронная конфигурация), имеющего строение D4h. Резонансные интегралы 3dz2 – 1s и 3dxz – 1s считать в два раза меньше резонансных интегралов 3dxy – 1s и 3dx2-y2 – 1s (если понадобятся какие-то из этих интегралов). Кулоновские интегралы для 3d орбиталей иона титана и 1s атомов водорода считать одинаковыми.
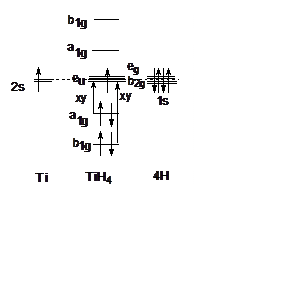 Решение: Можно
показать, что в группе D4h 3d орбитали титана преобразуются по
представлениям а1g, b1g, b2g и eg,
а атомные орбитали водородов реализуют НП а1g, b1g и eu.
Комбинации орбиталей водорода, преобразующиеся по этим представлениям имеют вид
Решение: Можно
показать, что в группе D4h 3d орбитали титана преобразуются по
представлениям а1g, b1g, b2g и eg,
а атомные орбитали водородов реализуют НП а1g, b1g и eu.
Комбинации орбиталей водорода, преобразующиеся по этим представлениям имеют вид
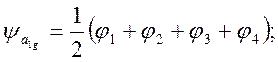
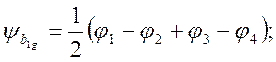
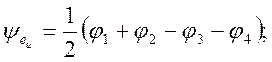
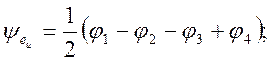
МО а1g (3dz2) равны a ± b(3dz2 – 1s), МО b1g (3dx2-y2) равны a ± b(3dx2-y2 – 1s). Остальные орбитали остаются несвязывающими. На рисунке показано расположение МО, а также положение переходов для двух линий поглощения с XY поляризация, отличающихся по энергии в два раза.
Решение задач на контрольную 6 апреля 2003 г. Группы 041-043
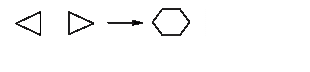 1. (400) Определить разрешенность реакции H3 + H3®H6. Построить коррелляционную диаграмму для этой реакции
и определить изменение полной электронной энергии. Кулоновские интегралы
одинаковы для обоих типов молекул.
1. (400) Определить разрешенность реакции H3 + H3®H6. Построить коррелляционную диаграмму для этой реакции
и определить изменение полной электронной энергии. Кулоновские интегралы
одинаковы для обоих типов молекул.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.