Исходя из полученных данных, была построена зависимость электропроводности от времени:
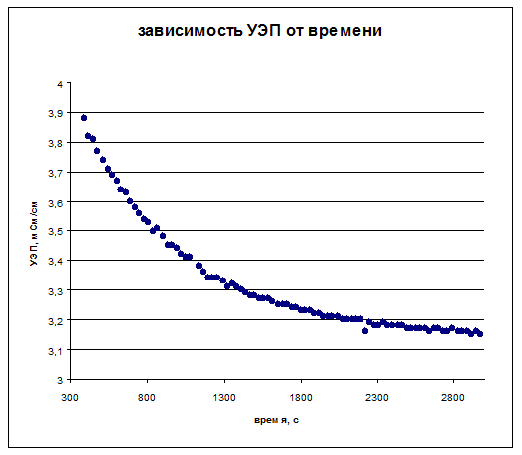
Полученная зависимость была аппроксимирована функцией y=y0+A1*exp(-x/t1), были определены независимые параметры (впоследствии в расчетах не использовались):
|
Параметр |
Значение |
Стандартное отклонение |
|
y0 |
3,161 |
0,004 |
|
A1 |
1,46 |
0,01 |
|
t1 |
569 |
9 |
Остаток раствора в
колбе №3 был оставлен в термостате на 2 часа, после чего была измерена удельная
электропроводность ![]() раствора,
данные занесены в таблицу 3:
раствора,
данные занесены в таблицу 3:
|
№ |
УЭП(мСм/см) |
T, oC |
|
1 |
3,050 |
24,9 |
|
2 |
3,040 |
25,0 |
|
3 |
3,040 |
25,0 |
|
4 |
3,040 |
25,0 |
|
5 |
3,040 |
25,0 |
|
6 |
3,040 |
25,1 |
Определение константы реакции:
Для
построения анаморфозы, соответствующей кинетике второго порядка, сначала
вычислили средние значения![]() ,
,
![]() ,
,![]() :
:
![]() =1,642,
=1,642,
![]() =3,040,
=3,040,
![]() =4,620.
Затем из среднего значения минерализации для раствора чистой щелочи определили b (начальную концентрацию щелочи):
С=0,7986(г/л)/39,9967(г/моль)=0,01996 (моль/л). Также вычислили точное значение
концентрации этилацетата (а) из кондуктометрических данных, воспользовавшись
уравнением 11 и соотношением
=4,620.
Затем из среднего значения минерализации для раствора чистой щелочи определили b (начальную концентрацию щелочи):
С=0,7986(г/л)/39,9967(г/моль)=0,01996 (моль/л). Также вычислили точное значение
концентрации этилацетата (а) из кондуктометрических данных, воспользовавшись
уравнением 11 и соотношением ![]() :
:
С0Ac-=0,01059 (моль/л).
Используя
выражения 5,10, вычислили значение концентрации ![]() и глубину протекания реакции y в каждой точке. Затем,
воспользовавшись уравнением 4, вычислили значения k*t в каждой точке, построили
анаморфозу, соответствующую кинетике второго порядка:
и глубину протекания реакции y в каждой точке. Затем,
воспользовавшись уравнением 4, вычислили значения k*t в каждой точке, построили
анаморфозу, соответствующую кинетике второго порядка:
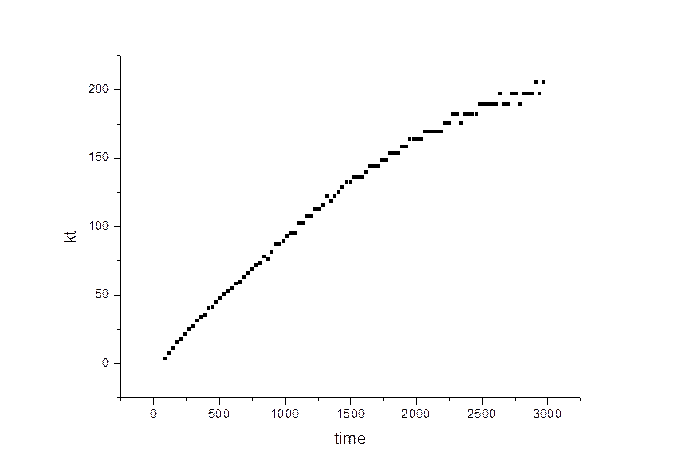
Для определения константы реакции провели прямую методом наименьших квадратов по первым 30 точкам, поскольку при больших значениях t анаморфоза достаточно сильно отклоняется от прямой зависимости:
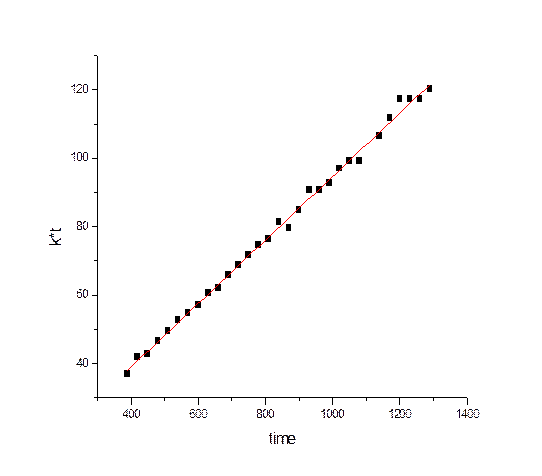
|
Параметр |
Значение |
Стандартное отклонение |
|
k |
0,093 |
0,001 |
Параметр k=0,093±0,001 (л/моль*с) является искомой константой реакции омыления этилацетата щелочью. Полученное значение сравнили с табличной константой:
|
T, oC |
k, л/моль*мин |
k, л/моль*с |
|
0 |
1,17 |
0,020 |
|
20 |
5,08 |
0,085 |
|
25 |
6,56 |
0,109 |
Ошибка измерения константы составила 9,4%.
Вывод
В ходе работы были проведены кинетические измерения, основанные на изменении удельной электропроводности от времени. Исходя из полученных данных, построена анаморфоза для кинетики второго порядка и при помощи метода наименьших квадратов определена константа реакции омыления этилацетата гидроксидом натрия:
k=0,093±0,001 (л/моль*с).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.