|
Номер опыта |
Объём пробы, мкл |
Концентрация субстрата, [S], моль/л |
Время, мин |
Изм опт плотн |
Изм конц, мкмоль/мл |
Скорость, мкмоль/(мл*мин) |
Средняя скорость, мкмоль/(мл*мин) |
|
1 |
10 |
0,0028 |
0,96 |
0,12 |
0,0048 |
0,00050 |
0,00053 |
|
1 |
0,86 |
0,12 |
0,0048 |
0,00056 |
|||
|
2 |
20 |
0,0055 |
0,61 |
0,12 |
0,0048 |
0,00079 |
0,00079 |
|
2 |
0,61 |
0,12 |
0,0048 |
0,00079 |
|||
|
3 |
50 |
0,0138 |
0,56 |
0,22 |
0,0088 |
0,00157 |
0,00168 |
|
3 |
0,45 |
0,20 |
0,0080 |
0,00179 |
|||
|
4 |
100 |
0,0276 |
0,38 |
0,26 |
0,0104 |
0,00271 |
0,00280 |
|
4 |
0,40 |
0,29 |
0,0116 |
0,00290 |
|||
|
5 |
200 |
0,0553 |
0,34 |
0,32 |
0,0128 |
0,00381 |
0,00380 |
|
5 |
0,40 |
0,38 |
0,0152 |
0,00380 |
|||
|
6 |
400 |
0,1106 |
0,35 |
0,42 |
0,0168 |
0,00477 |
0,00483 |
|
6 |
0,35 |
0,43 |
0,0172 |
0,00489 |
|||
|
7 |
1000 |
0,2764 |
0,37 |
0,49 |
0,0196 |
0,00533 |
0,00502 |
|
7 |
0,42 |
0,49 |
0,0196 |
0,00471 |
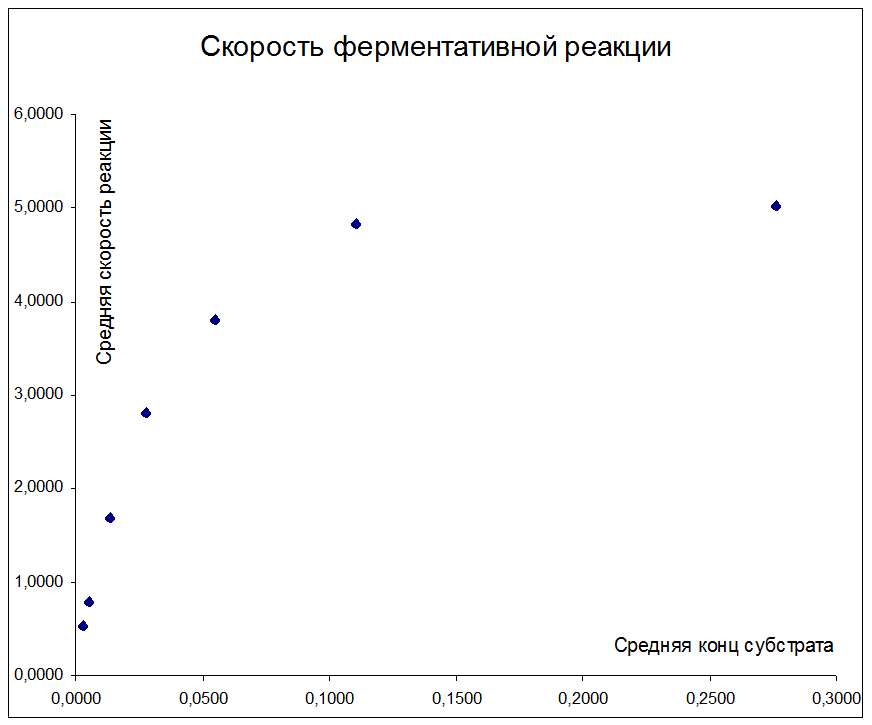
График 1 иллюстрирует, что скорость ферментативной возрастает при росте концентрации субстрата. Постепенно скорость роста падает (см. Приложение) и кривая выходит на плато, асимптотически приближаясь к уровню максимальной скорости реакции.
График Лайнуивера-Берка
Таблица 2
|
Обратная концентрация |
363,57 |
181,79 |
72,35 |
36,18 |
18,09 |
9,04 |
3,62 |
|
Обратная скорость |
1894,74 |
1266,67 |
595,74 |
356,61 |
262,83 |
207,06 |
199,25 |
|
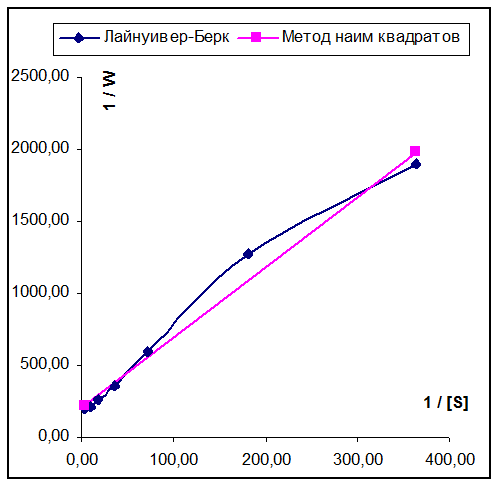
Определена константа Михаэлиса 0,02моль/л [0,01-0,03 моль/л] и максимальная скорость 0,0050мкмоль/(мл*мин). [0,0025-0,0075 мкмоль/(мл*мин)].
График Эйзеншталя-Корниш-Боудена
Определение константы Михаэлиса графическим методом Эйзеншталя-Корниш-Боудена (см. Приложение, график 3). Способ получения графика описан в теоретической части. Из графика видно, что идеального совпадения с теорией нет, так как наблюдается “плавающая точка” пересечения графиков. Такое явление довольно обычно для подобных экспериментов.
Причина, наверное, состоит в погрешностях приборов. Из графика 3 видно, что уменьшение концентрации субстрата приводит к увеличению точности нанесения точек по оси ординат в ущерб точности нанесения точек по оси абсцисс. Мы не можем брать очень близкие между собой концентрации субстрата, так как иначе из экспериментального графика (см. Приложение) в силу случайных или систематических ошибок невозможно с хорошей точностью рассчитать начальную скорость.
Таблица 3
|
Концентрация субстрата, моль/л |
0,0028 |
0,0055 |
0,0138 |
0,0276 |
0,0553 |
0,1106 |
0,2764 |
|
Скорость реакции, мкмоль/(мл*мин) |
0,00053 |
0,00079 |
0,00168 |
0,00280 |
0,00380 |
0,00483 |
0,00502 |
|
Обратная скорость, мл*мин/мкмоль |
1887 |
1266 |
595 |
357 |
263 |
207 |
199 |
Из графика 3 находим, что константа Михаэлиса находится в пределах 0,008-0,020моль/л, что совпадает с результатом, полученным методом двойных обратных координат Лайнуивера-Берка. Максимальная скорость реакции определена как 0,0053-0,0059 мкмоль/(мл*мин).
График Иди-Хофсти
Таблица 4
|
Скорость реакции, мкмоль/(л*мин) |
0,5278 |
0,7895 |
1,6786 |
2,8042 |
3,8048 |
4,8295 |
5,0188 |
|
Скорость / Концентрация субстрата *10-6,мин-1 |
192 |
144 |
121 |
101 |
69 |
44 |
18 |
|
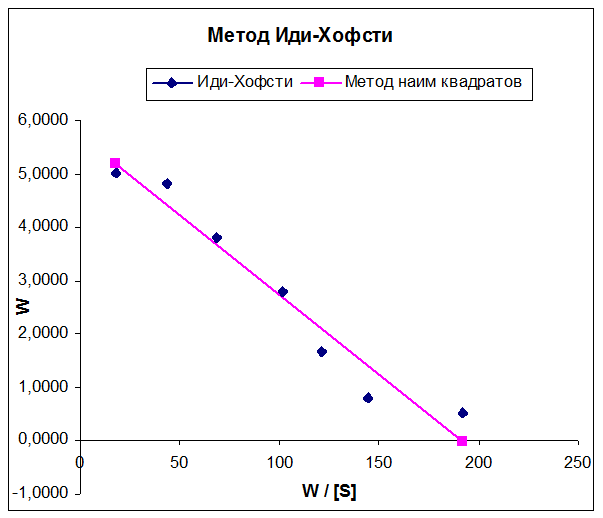
Построенный по экспериментальным данным график был приближен прямой по методу наименьших квадратов. Было получено уравнение прямой в координатах (W, W/[S]), что позволило определить константу Михаэлиса как –tg угла наклона прямой графика с положительным направлением оси абсцисс. Фактически константа Михаэлиса – коэффициент пропорциональности в уравнении прямой. Получено среднее значение 0,030 моль/л, пределы 0,023-0,037 моль/л.
Список литературы.
1. К.И. Замураев. Химическая кинетика. Курс лекций, часть 1. Новосибирск, НГУ, 2004.
2. Д.Г. Кнорре, С.Д. Мызина. Биоорганическая химия.
3. А. Ленинджер. Основы биохимии, т. 1. Москва, 1985.
4. Большая Советская Энциклопедия, 2-е издание; т. 11, с 539..
5. Е.С. Рудаков и др. Практикум по химической кинетике. Новосибирск, НГУ, 1999.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.