|
T, К |
Cигнал |
ширина пика, мм |
ширина пика, Гц |
высота пика, мм |
площадь, мм*мм |
константа равновесия, К |
R*ln K |
1/T*R*ln K |
|
297,5 |
CH |
35 |
17,5 |
116 |
2030 |
11,3884993 |
20,22467 |
0,0679821 |
|
CH2 |
23 |
11,5 |
31 |
356,5 |
||||
|
323 |
CH |
33 |
16,5 |
98 |
1617 |
8,52173913 |
17,81375 |
0,0551509 |
|
CH2 |
23 |
11,5 |
33 |
379,5 |
||||
|
343 |
CH |
30 |
15 |
85 |
1275 |
6,18181818 |
15,14489 |
0,0441542 |
|
CH2 |
25 |
12,5 |
33 |
412,5 |
||||
|
353 |
CH |
29 |
14,5 |
80 |
1160 |
4,88421053 |
13,18607 |
0,0373543 |
|
CH2 |
25 |
12,5 |
38 |
475 |
||||
|
358 |
CH |
26 |
13 |
72 |
936 |
3,56571429 |
10,57012 |
0,0295255 |
|
CH2 |
25 |
12,5 |
42 |
525 |
||||
|
363 |
CH |
26 |
13 |
61 |
793 |
2,77272727 |
8,478878 |
0,0233578 |
|
CH2 |
26 |
13 |
44 |
572 |
||||
|
368 |
CH |
24 |
12 |
61 |
732 |
2,61896243 |
8,004538 |
0,0217515 |
|
CH2 |
26 |
13 |
43 |
559 |
||||
|
373 |
CH |
25 |
12,5 |
56 |
700 |
2,4137931 |
7,326292 |
0,0196415 |
|
CH2 |
29 |
14,5 |
40 |
580 |
||||
|
378 |
CH |
24 |
12 |
51 |
612 |
2,30075188 |
6,927524 |
0,0183268 |
|
CH2 |
28 |
14 |
38 |
532 |
На основании данных таблицы рассчитали приближение по методу наименьших квадратов и построили график. ∆H0T= + 20264 Дж/моль, ∆S0T= - 51,88 Дж/(моль*К). Положительная величина ∆H0T соответствует эндотермической реакции. Чем больше тепла будет сообщено системе, тем глубже пройдёт реакция.
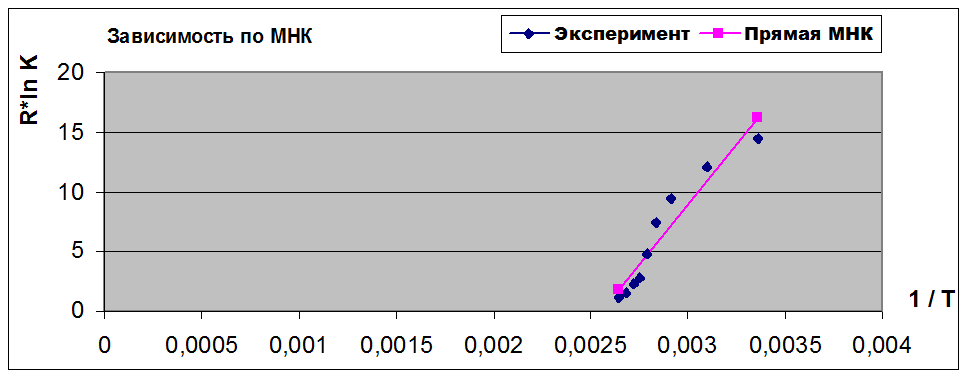
Рассчитали стандартные отклонения для ∆H0T и ∆S0T. Для расчёта использовали формулы:
σy2=Σ(y-y(av))2/(n-1);
σk=[σy2/(Σ(Xi2)-(ΣXi)2/n)]½;
σb=[σy2*Σ(Xi2)/(n*Σ(Xi2)- (ΣXi)2)]½.
В приведённых формулах величина X соответствует обратной температуре (1/T), а величина y – (+ R*lnK). Значение n – число проведённых измерений (9).
Величины σk и σb представляют собой стандартные отклонения энтальпии и энтропии соответственно (таблица 2). Их значения довольно велики: 7495 Дж/моль для энтальпии и 21,54 Дж/(моль* К) для энтропии. Результаты занесены в таблицу.
Таблица 2
|
1/Т |
1/(R*ln K) (av) -1/(R*ln K) |
R*ln K |
|||
|
0,003361345 |
68,23733324 |
14,4618441 |
Значение изменения энтальпии |
Значение изменения энтропии |
|
|
0,003095975 |
34,21858952 |
12,05092071 |
20264,29642 |
-51,88434453 |
|
|
0,002915452 |
10,11752146 |
9,382060104 |
Дисперсия |
Дисперсия |
|
|
0,002832861 |
1,49325244 |
7,423242031 |
56172554,91 |
464,1767728 |
|
|
0,002793296 |
1,943116197 |
4,807297916 |
Стандартное отклонение |
Стандартное отклонение |
|
|
0,002754821 |
12,14663475 |
2,71605269 |
7494,835215 |
21,54476207 |
|
|
0,002717391 |
15,67797658 |
2,241712473 |
|||
|
0,002680965 |
21,50908395 |
1,563466253 |
|||
|
0,002645503 |
25,36690358 |
1,164698226 |
|||
Итоговые значения ∆H0T= 20 ± 7 кДж/моль; ∆S0T= - 52 ± 22 Дж/(моль*К).
ВАНЯ! ДАННЫЕ ТАБЛИЦ СЛЕДУЕТ НЕСКОЛЬКО ИСПРАВИТЬ, ТАК КАК ОНИ СОДЕРЖАТ ЧЕРЕСЧУР МНОГО ЗНАЧАЩИХ ЦИФР.
СЛЕДУЕТ ОСТАВИТЬ ЗНАЧЕНИЯ КОНСТАНТЫ РАВНОВЕСИЯ ДО СОТЫХ И Т.Д.
ЗНАЧЕНИЯ КОНСТАНТЫ В EXCEL БЫЛИ РАССЧИТАНЫ ПО ПИКАМ ГРУПП CH и CH2, ПОЭТОМУ В СТОЛБЦЕ КОНСТАНТА В EXCEL СТОИТ МНОЖИТЕЛЬ 2, ТАК КАК CH2-ГРУППА ИМЕЕТ ВДВОЕ БОЛЬШЕ ПРОТОНОВ, НА САМОМ ДЕЛЕ ОТ ВЕЛИЧИНЫ КОНСТАНТЫ ВАШИ ОТВЕТЫ НЕ ЗАВИСЯТ (МЫ НА 2 УМНОЖИТЬ ЗАБЫЛИ, НО ПОЛУЧИЛИ ТЕ ЖЕ ЗНАЧЕНИЯ).
УДАЧИ!
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.