Точка, описывающая состояние активированного
комплекса, движется вдоль пути реакции со скоростью порядка скоростей
относительного движения атомов, т. е. со средней скоростью ![]() порядка тепловой. Время пребывания ее на
отрезке
порядка тепловой. Время пребывания ее на
отрезке ![]() , т. е. время жизни активированного
комплекса порядка
, т. е. время жизни активированного
комплекса порядка ![]() . Для характерных
. Для характерных ![]() см и
см и ![]() см/c
см/c ![]() cи время
жизни комплекса много меньше характерного времени реакции (времени достижения
химического равновесия в смеси газов), что дает обоснование высказанному выше
утверждению (9.21).
cи время
жизни комплекса много меньше характерного времени реакции (времени достижения
химического равновесия в смеси газов), что дает обоснование высказанному выше
утверждению (9.21).
Если считать, что каждый образовавшийся комплекс
распадается в сторону продуктов реакции, то число актов реакции в ед. объема и
в ед. времени равно числу распадов комплекса, т. е. числу комплексов в ед.
объема, поделенному на время их жизни. Обозначив через ![]() плотности
реагентов, а
плотности
реагентов, а ![]() комплексов (для реакции (9.21)
комплексов (для реакции (9.21) ![]() есть
есть ![]() и
и ![]() , а
, а ![]() ),
получим для прямой реакции
),
получим для прямой реакции
![]() (9.22),
откуда константа скорости прямой реакции есть
(9.22),
откуда константа скорости прямой реакции есть
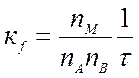 (9.23).
(9.23).
По закону действующих масс отношение чисел частиц,
участвующих в реакции ![]() , в состоянии равновесия равно
отношению статистических сумм частиц. Как и ранее, разделим обе части равенства
на объем, занимаемый газом (с учетом того, что объем входит линейным
множителем только в поступательные статистические суммы), выделим из
статистических сумм множители типа
, в состоянии равновесия равно
отношению статистических сумм частиц. Как и ранее, разделим обе части равенства
на объем, занимаемый газом (с учетом того, что объем входит линейным
множителем только в поступательные статистические суммы), выделим из
статистических сумм множители типа ![]() , соответствующие энергии
частиц в основном состоянии, и замечая, что
, соответствующие энергии
частиц в основном состоянии, и замечая, что ![]() равно
энергии активации, получим
равно
энергии активации, получим
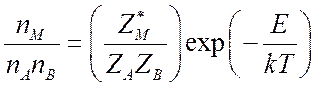 (9.24).
(9.24).
В
статистической сумме переходного комплекса необходимо учесть то, что
поступательное движение комплекса вдоль координаты реакции считается
независящим от других степеней свободы. Поэтому полная статистическая сумма ![]() должна быть представлена в виде двух
сомножителей: трансляционной (поступательной) статсуммы на участке
должна быть представлена в виде двух
сомножителей: трансляционной (поступательной) статсуммы на участке ![]() вдоль координаты реакции равной
вдоль координаты реакции равной 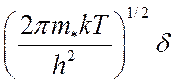 , где
, где ![]() эффективная
масса комплекса и статсуммы для остальных степеней свободы комплекса
эффективная
масса комплекса и статсуммы для остальных степеней свободы комплекса ![]() :
:
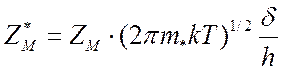 (9.25).
(9.25).
Подставляя
(9.24) и (9.25) в (9.23) с учетом ![]() , где
, где ![]() - средняя скорость поступательного
движения вдоль координаты разложения, для константы скорости получим
- средняя скорость поступательного
движения вдоль координаты разложения, для константы скорости получим
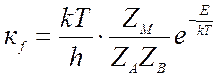 (9.26).
(9.26).
Следует
отметить, что неопределенные величины ![]() и
и ![]() сократились и в конечное выражение для
константы реакции не входят. Вводят еще так называемый трансмиссионный
коэффициент
сократились и в конечное выражение для
константы реакции не входят. Вводят еще так называемый трансмиссионный
коэффициент ![]()
![]() , характеризующий
вероятность распада комплекса в сторону продуктов реакции, который обычно
порядка единицы и окончательно
, характеризующий
вероятность распада комплекса в сторону продуктов реакции, который обычно
порядка единицы и окончательно
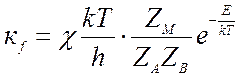 (9.27).
(9.27).
Вычисление
статсумм в уравнении (9.27) производится с использованием представления ![]() в виде произведения поступательной,
вращательной, колебательной и электронной статсумм
в виде произведения поступательной,
вращательной, колебательной и электронной статсумм
![]() (9.28).
(9.28).
![]() равно
кратности электронного вырождения молекулы, а
равно
кратности электронного вырождения молекулы, а ![]() вычисляются
на основе стандартных формул статистической физики:
вычисляются
на основе стандартных формул статистической физики:
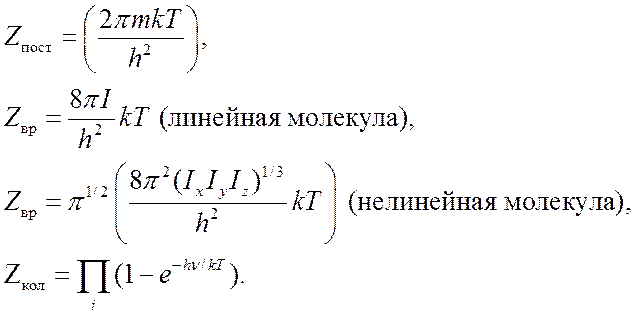 (9.29).
(9.29).
Для
поступательной статсуммы комплекса ![]() , а объем, входящий в
качестве сомножителя в формулу опущен.
, а объем, входящий в
качестве сомножителя в формулу опущен.
Самым слабым местом в теории МПС является вопрос конструирования переходного комплекса, что часто дает повод к утверждению, что по МПС можно получить любое значение константы скорости, стоит только соответствующим образом сконструировать переходной комплекс.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.