Сумма
![]() называется энтальпией системы. Это
ещё одна функция состояния, то есть функция, изменение которой не зависит от
процесса, а определяется только начальным и конечным состоянием газа. Напомним,
что к функциям состояния относятся также, например, такие параметры как объём,
давление, энергия, энтропия газа.
называется энтальпией системы. Это
ещё одна функция состояния, то есть функция, изменение которой не зависит от
процесса, а определяется только начальным и конечным состоянием газа. Напомним,
что к функциям состояния относятся также, например, такие параметры как объём,
давление, энергия, энтропия газа.
Итак, мы пришли к выводу, что в процессе Джоуля-Томсона энтальпия газа не меняется, то есть процесс изоэнтальпный.
![]() и
и
![]() , (3.8)
, (3.8)
Будем
рассматривать процесс при малых перепадах давления ![]() и при
малых, соответственно, изменениях температуры газа
и при
малых, соответственно, изменениях температуры газа ![]() . Такой
процесс называют дифференциальным процессом Джоуля-Томсона, в отличие от
интегрального процесса, где перепады давления могут составлять десятки и даже
сотни атмосфер.
. Такой
процесс называют дифференциальным процессом Джоуля-Томсона, в отличие от
интегрального процесса, где перепады давления могут составлять десятки и даже
сотни атмосфер.
В случае дифференциального процесса, нулевое изменение энтальпии можно записать так:
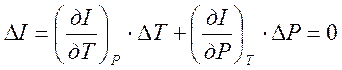 , (3.9)
, (3.9)
Учитывая,
что ![]() , а
, а ![]() ,
находим коэффициент Джоуля-Томсона, представляющий собой отношение изменения
температуры
,
находим коэффициент Джоуля-Томсона, представляющий собой отношение изменения
температуры ![]() к перепаду давления на пробке
к перепаду давления на пробке ![]() .
.
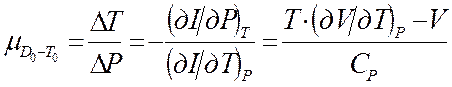 . (3.10)
. (3.10)
Воспользовавшись уравнением (3.10), вычислим коэффициент Джоуля-Томсона для идеального газа. В этом случае:
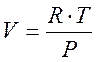 и
и 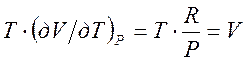 .
.
Подставляя
этот результат в (3.10), находим, что для идеального газа коэффициент
Джоуля-Томсона ![]() . Это значит, что при расширении
идеального газа в процессе Джоуля-Томсона, его температура остаётся постоянной,
то есть температурный перепад
. Это значит, что при расширении
идеального газа в процессе Джоуля-Томсона, его температура остаётся постоянной,
то есть температурный перепад ![]() .
.
Теперь рассмотрим поведение реального газа в процессе Джоуля-Томсона. Общая термодинамическая теория эффекта остаётся прежней, но для получения из неё конкретных результатов, воспользуемся на этот раз термическим уравнением состояния реальных газов Ван-дер-Ваальса:
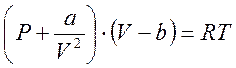 . (3.11)
. (3.11)
для
расчёта коэффициента Джоуля-Томсона ![]() необходимо знать
производную
необходимо знать
производную ![]() (см. 3.10). Для её отыскания
продифференцируем (3.11) по T, считая давление P
постоянным:
(см. 3.10). Для её отыскания
продифференцируем (3.11) по T, считая давление P
постоянным:
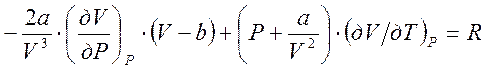 .
.
Отсюда следует, что:
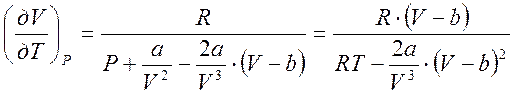 .
.
Упростим задачу, ограничившись рассмотрением разрежённого реального газа. В этом случае слагаемые, содержащие постоянные a и b, являются малыми поправками. В связи с этим можно пренебречь всеми членами с высшими степенями aи b. В этом приближении:
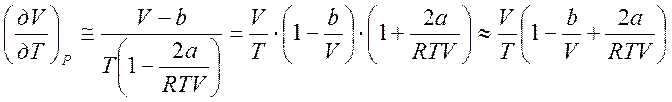 , (3.12)
, (3.12)
Используя последний результат в формуле (3.10), получим выражение коэффициента Джоуля-Томсона для разрежённых газов:
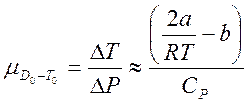 . (3.13)
. (3.13)
Таким образом, дифференциальный эффект Джоуля-Томсона для реальных газов зависит от поправок a и bв уравнение Ван-дер-Ваальса, причём они доказывают противоположное влияние на знак эффекта.
Если
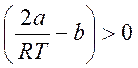 , то
, то ![]() и газ
при протекании через пробку охлаждается. (Здесь уместно напомнить, что в
процессе Джоуля-Томсона
и газ
при протекании через пробку охлаждается. (Здесь уместно напомнить, что в
процессе Джоуля-Томсона ![]() ). Этот эффект
называется положительным.
). Этот эффект
называется положительным.
Эффект
отрицателен, когда 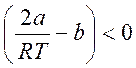 и, соответственно,
и, соответственно, 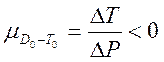 . При отрицательном эффекте температура
газа в процессе Джоуля-Томсона увеличивается. Легко видеть, что при
. При отрицательном эффекте температура
газа в процессе Джоуля-Томсона увеличивается. Легко видеть, что при ![]() и
и ![]() газ
всегда охлаждается, а при
газ
всегда охлаждается, а при ![]() и
и ![]() - всегда нагревается. Если присутствуют
обе поправки, то можно указать температуру газа, когда эффект отсутствует:
- всегда нагревается. Если присутствуют
обе поправки, то можно указать температуру газа, когда эффект отсутствует:
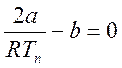 ;
; 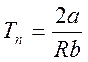 (3.14)
(3.14)
Эта
рубежная температура ![]() называется температурой
инверсии. При такой температуре газа эффект Джоуля-Томсона отсутствует,
называется температурой
инверсии. При такой температуре газа эффект Джоуля-Томсона отсутствует, ![]() . При температуре газа, выше температуры
инверсии
. При температуре газа, выше температуры
инверсии ![]() , газ в процессе Джоуля-Томсона
охлаждается, при
, газ в процессе Джоуля-Томсона
охлаждается, при ![]() - нагревается.
- нагревается.
Для
большинства газов температура инверсии значительно выше комнатной температуры,
поэтому чаще в опыте Джоуля-Томсона газ охлаждается, то есть существенней
оказывается влияние на эффект поправки ![]() .
.
В
данной работе измеряют коэффициент Джоуля-Томсона ![]() для
воздуха при комнатной температуре и оценивают значение постоянной
для
воздуха при комнатной температуре и оценивают значение постоянной ![]() в уравнении Ван-дер-Ваальса (3.4).
в уравнении Ван-дер-Ваальса (3.4).
5. Экспериментальная установка
Рабочим элементом установки является текстолитовая
гильза (поз. 1), в которой находится войлочная пробка (поз. 2), образующая
пористую перегородку. Воздух прокачивается сквозь перегородку при помощи
компрессора (поз. 3). Избыточное давление на перегородке регулируется вентилем
(поз. 4.), соединяющим линию с атмосферой. Закрывая вентиль, можно поднимать
давление на перегородке от 0 до 0,6 МПа. Это избыточное давление регистрируется
манометром (поз. 5). Температура воздуха перед перегородкой (поз. 6),
расположенной на входе газового потока. Температурный перепад ![]() на пористой пробке измеряется с помощью
дифференциальной хромель-копелевой термопары, спаи которой расположены в потоке
по обе стороны от перегородки (поз. 7).
на пористой пробке измеряется с помощью
дифференциальной хромель-копелевой термопары, спаи которой расположены в потоке
по обе стороны от перегородки (поз. 7).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.