Министерство Образования Российской Федерации
Филиал ГОУВПО
«Московский энергетический институт
(технический университет)»
в г.Волжском
Кафедра промышленной теплоэнергетики
Лабораторная работа №2
по курсу термодинамики
Изучение эффекта Джоуля-Томсона
Студент Парасоцкий А.Б.
Группа АТП-02
Преподаватель Шевцова С.Б.
Волжский 2004
1. Цель работы
Экспериментальное исследование эффекта Джоуля-Томсона, изучение термодинамической теории этого процесса.
2. Содержание работы
Проведение опыта. Обработка результатов измерений. Расчёт эффекта Джоуля-Томсона. Определение константы Ван-дер-Ваальса.
3. Теоретические основы работы
Термодинамическое состояние системы задаётся двумя уравнениями:
термическим уравнением, связывающим макропараметры системы:
![]() , (3.1)
, (3.1)
и калорическим уравнением состояния:
![]() , (3.2)
, (3.2)
представляющим собой зависимость внутренней энергии системы от её объёма и температуры.
При рассмотрении свойств газа в качестве термического уравнения используют, как правило, одно из двух уравнений состояния:
в случае идеального газа это уравнения Клапейрона:
![]() , (3.3)
, (3.3)
в случае реального газа – не менее известное уравнение Ван-дер-Ваальса
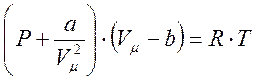 , (3.4)
, (3.4)
где
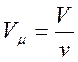 ;
; ![]() - число
молей.
- число
молей.
В этом выражении характерные для конкретного газа постоянные aи b называются поправками Ван-дер-Ваальса. Они учитывают неидеальность газа, связанную с межмолекулярным взаимодействием (поправка a) и с собственным объёмом молекул (поправка b).
Оба последних уравнения записаны для одного моля газа.
Что качается калорического уравнения (3.2), то прежде всего нужно отметить, что установлению зависимости внутренней энергии газа от объёма посвятили свои экспериментальные работы Гей-Люссак, Джоуль, Томсон и ряд других учёных. Опыты же Джоуля и Томсона, поставленные ими в середине прошлого века, и сегодня ещё рассматриваются как классика теплофизического эксперимента.
3. Опыт Джоуля-Томсона
![]()
![]()
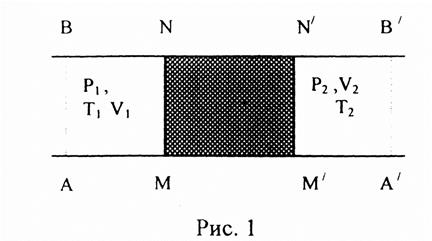 В опытах Джоуля и Томсона исследовалось течение газа через
пористую перегородку. Перегородка в виде пробки из прессованного войлока
устанавливалась внутри цилиндрической трубки. Трубка со всей тщательностью теплоизолировалась,
что обеспечивало адиабатический характер течения газа.
В опытах Джоуля и Томсона исследовалось течение газа через
пористую перегородку. Перегородка в виде пробки из прессованного войлока
устанавливалась внутри цилиндрической трубки. Трубка со всей тщательностью теплоизолировалась,
что обеспечивало адиабатический характер течения газа.
Газ протекал по трубке под действием невысокого – порядка 3-8 атмосфер – перепада давления. Таким образом, обеспечивалось ламинарное течение газа с невысокими скоростями как до, так и после пробки.
Газ, конечно, обменивался теплом с пробкой. Но вскоре после начала течения, процесс становился стационарным, теплообмен прекращался, а потому физическое состояние пробки и её внутренняя энергия стабилизировались.
Подобное стационарное течение газа через пористую перегородку получило название «процесс Джоуля-Томсона», а изменение температуры газа, наблюдаемое при этом, называется эффектом Джоуля-Томсона.
Рассмотрим
процесс Джоуля-Томсона с позиции первого начала термодинамики. Выделим слева от
пробки порцию газа объёмом ![]() . Давление здесь перед
пробкой -
. Давление здесь перед
пробкой - ![]() (Рис. 1). За пробкой эта порция,
расширившись, займёт объём
(Рис. 1). За пробкой эта порция,
расширившись, займёт объём ![]() , давление газа при этом
упадёт до
, давление газа при этом
упадёт до ![]() . При этом переходе газ совершает работу:
. При этом переходе газ совершает работу:
![]() (3.5)
(3.5)
Действительно,
при течении газа граница AB выделенного объёма ![]() перейдёт
в положение MNи
над газом при этом будет совершена работа
перейдёт
в положение MNи
над газом при этом будет совершена работа ![]() . За то
же время граница
. За то
же время граница ![]() объёма
объёма ![]() переместится
на расстояние
переместится
на расстояние ![]() . В этом процессе газ совершит
работу
. В этом процессе газ совершит
работу ![]() . Полная работа газа, таким образом,
. Полная работа газа, таким образом, ![]() . Напомним, что речь идёт о стационарном
адиабатическом процессе, в котором теплообмен исключён. Поэтому работа,
совершаемая газом, продлена только за счёт изменения внутренней энергии:
. Напомним, что речь идёт о стационарном
адиабатическом процессе, в котором теплообмен исключён. Поэтому работа,
совершаемая газом, продлена только за счёт изменения внутренней энергии:
![]() (3.6)
(3.6)
Это уравнение первого начала термодинамики для процесса Джоуля-Томсона. Можно, учитывая (3.5) записать в виде:
![]() (3.7)
(3.7)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.