Нижняя кривая (1) показывает зависимость температуры кипения от состава жидкой фазы, верхняя (2) - состав пара, находящегося в равновесии с жидкостью при каждой температуре. Ниже линии (1) существует жидкая фаза (ж), поэтому ещё эту линию называют линией жидкости. Выше линии (2), называемой линией пара, существует парообразная фаза (П). Область между этими двумя кривыми соответствует гетерогенному равновесию жидкость - пар. Любой точке в этой области (например К) отвечает жидкость состава I и пар состава m. Относительное количество жидкой и парообразной фаз можно вычислить по правилу рычага.
Для разгонки раствора пар, получаемый при кипении жидкости, подвергается постепенному охлаждению, приводящему к последовательному обогащению пара более летучим компонентом.
Предположим, что мольная доля хлорбензола (компонент В) в исходной жидкости nb = 0, 55 (точка C1). Этот раствор кипит при t1 = 141 0С. Первые порции образовавшегося пара имеют состав определённый точкой С1, с повышением содержания хлорбензола по сравнению с исходным равновесным раствором (nb = 0.78). Пар охлаждают, в следствие чего он конденсируется (точка C2). Полученный конденсат кипит при температуре t1 = 137°C. При этой температуре отгоняется пар, ещё более обогащенный хлорбензолом (точка С2, nb = 0, 92).
В результате последовательного охлаждения и выделения из пара двух равновесных фаз различного состава можно получить конденсат, приближающийся по составу к чистому хлорбензолу.
После отделения пара в жидкости увеличиваются относительное содержание бромбензола (например, точка С3, nb=0,5), в следствие чего, температура кипения её повысится по сравнению с исходным раствором (t3=144°C). При последовательном пара жидкость в перегонной колбе постепенно будет обогащаться бромбензолом, пока не приблизится по составу к практически чистому бромбензолу. Этот принцип разделения используют в ректификационных аппаратах, где пар, поднимаясь вверх, конденсируется на охлаждаемых приспособлениях, обогащаясь постепенно более летучим компонентом, а жидкость, обогащаясь менее летучим компонентом, стекает вниз и накапливается в перегонной колбе.
Степень разделения зависит от различия в температурах кипения двух компонентов, от различия в составе жидкости и пара, от температуры охлаждающих поверхностей и т. д. II закон Коновалова - точки максимума или минимума на кривой общего давления пара отвечают растворам, состав которых одинаков с составом равновесного с ним пара. Точке максимума на данной кривой давление - состав (рис 3.2, точка С) отвечает минимуму на кривой температура состав (рис 3.3, точка С).
По второму закону Коновалова максимум на кривой общего давления пара (рис 3.2, точка С) отвечает минимум на кривой температуры кипения (рис 3.3, точка С), а минимум на кривой общего давления пара (рис 3.4, точка С) отвечает максимум на кривой температуры кипения (рис 3.5, точка С).
В этих точках состав жидкости совпадает с составом разновесного с ней пара.
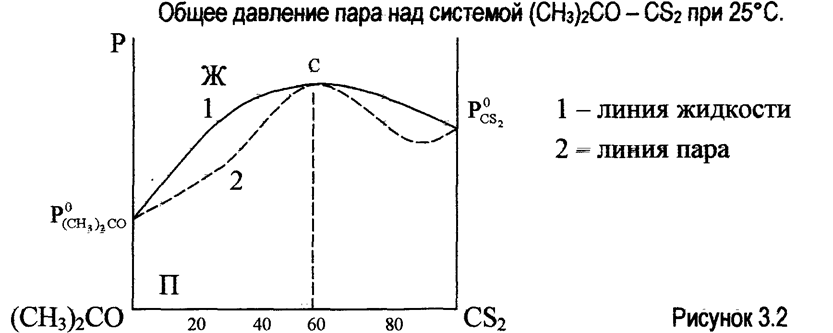
Растворы, отвечающие по составу этим экстремальным точкам, называются азеотропными, нераздельно кипящими. Состав их не меняется при кипении и температура кипения при заданном внешнем давлении остаётся постоянной, как у чистых веществ. Как видно из рисунков 3.3 и 3.5, при наличии экстремальных точек полное разделение смеси перегонкой невозможно. При фракционной перегонке систем, имеющих min на кривой (t-c), состав дистиллята последовательно приближается к азеотропному, а оставшаяся в перегонном кубе жидкость обогащается компонентом, который в исходном растворе был в избытке по отношению к составу азеотропного раствора. Так при разгонке смесей с исходным составом от О до 50% CS2 оставшаяся жидкость будет приближаться по составу к чистому ацетону, а при исходном составе от 50 до 100% CS2 в оставшейся жидкости будет накапливаться сернистый углерод.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.