фаз. За кривой Е С видно, что с повышением температуpы состав обеих фаз сближается ( точки F и Р при температуре ), так как растворимость каждой жидкости в другой увеличивается с ростом температуры. При температуре tK оба слоя идентичны по составу и сливаются в точке L. Температура tK называется верхней критической температурой. Выше нее две ограниченно смешивающиеся жидкости становятся неограниченно смешивающимися. Кривая ELC -(кривая расслоения) разделяет области гомогенных и гетерогенных систем. Любая точка в области, ограниченной кривой Е С и осью абсцисс (заштрихована на рис.1), отвечает двухслойной системе. Область вне кривой отвечает гомогенной однослойной системе. Состав сдоев в гетерогенной области определяется точками на кривой при одной и той же температуре, так. точка M указывает на систему иэ двух слоев с составами N и Р, отвечающими точками Q и К. Если при постоянной температуре увеличивать содержание компонентов В в смеси, то точка а передвигается вправо вдоль горизонтальной линии. Когда состав смеси пересечет кривую ELC (точка Q ), начнет формироваться второй слой состава Р. При дальнейшем повышении содержания компонента Б относительное количество слоя состава N будет уменьшаться , а слоя состава Р увеличиваться, но состав каждого слоя останется неизменным при данной температуре, пока в системе присутствуют две фазы. Когда состав системы достигнет состава Р, слой состава N перестанет существовать, и от точки К до точки У и далее смесь компонентов А и В образует один слой ненасыщенного раствора компонента А в компоненте В. В гетерогенной области С=2-2+1=1. Поэтому, если указана температура, то состояние системы полностью определено, так как состав обеих фаз можно узнать по пересечению линии температуры с кривой ELC . Наоборот, если задан состав одной из фаз то температуру можно определить no кривым EL или LС.
ДИАГРАММЫ ВЗАИМНОЙ РАСТВОРИМОСТИ.
|
С верхней критической температурой |
С нижней критической температурой |
С верхней и нижней критической температурой |
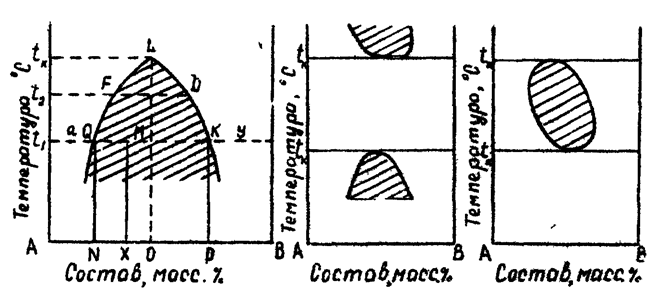
Рис.2 Рис.3 Рис.4
Для определения критической температуры растворения Алексеев предложил использовать приближенное правило прямолинейного диаметра, согласно которому среднее арифметическое из состава равновесных (жидких) фаз является линейной функцией температуры. Точка пересечения этой прямой L0 с кривой растворения отвечает критической температуре растворения tK. Диаграмма температура расслоения - состав позволяет определить как состав системы, так и количественное соотношение фаз в любой точке. Например, в точке М общий состав смеси х, состав первой фазы -N, состав второй фазы - Р, а относительно количества фаз можно определить по правилу рычага по конноде ОК:
масса первой Фазы = отрезок КМ
масса второй фазы отрезок ом .
Массы фаз выражаются в мольных долях, в массовых или мольных процентах. Если растворимость жидкостей повышается с понижением температуры, то область сосуществования обеих жидких фаз определяется кривой с минимумом и нижней критической температурой (рис.3. ).
Ниже нее жидкости вплоть до температуры кристаллизации смешиваются во всех отношениях, как, например, а системе вода-диэтидамин.
Двух компонентная системы может характеризоваться одновременно верхней и нижней" критической температурой. Здесь возможны 2 случая: 1) верхняя критическая температура выше нижней и неограниченное смещение наблюдается при соотношении компонентов, отвечающих составам, которые лежат за пределами заштрихованной области (рис.4), например в системах никотин-вода, метилпиперидин-вода; 2) нижняя критическая температура выше верхней и область неограниченного смещения лежит между кривыми, например, в системе поливинилацетат-метиловый спирт (рис.3). Чаще всего встречаются системы с одной верхней критической температурой.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РФ
ВОЛЖСКИЙ ПОЛИТЕХНИЧЕСКИЙ ИНСТИТУТ ВОЛГТУ
Кафедра химии, экономии и биотехнологии.
Лабораторная работа по физической химии № 5.
Выполнила: студент гр. ВХЭ-385
Савельева Н.Г.
Проверил: Курунина Г.М.
г. Волжский 2001 год.
|
№ пр-ки |
Состав системы фенол-вода масс % |
Температура гомогениза- ции |
Температура гетерогениза-ции |
Температура |
|
1 |
5:95 |
43 |
41 |
42 |
|
2 |
13:87 |
62 |
61 |
61,5 |
|
3 |
25:75 |
75 |
74 |
74,5 |
|
4 |
40:60 |
76 |
74 |
75 |
|
5 |
45:55 |
80 |
79 |
79,5 |
|
6 |
55:45 |
78 |
76,5 |
77 |
|
7 |
70:30 |
66 |
64 |
65 |
|
8 |
80:20 |
55 |
54 |
54,5 |
|
9 |
90:10 |
12 |
14 |
13 |
|
10 |
95:5 |
5 |
7 |
6 |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.