ЛЕКЦИЯ 10. ГАЗОВАЯ КОРРОЗИЯ В ВОДООТВОДЯЩИХ КОЛЛЕКТОРАХ
10.1. Условия эксплуатации водоотводящих сетей
Самотечные водоотводящие сети пропускают сточную воду неполным сечением. Воздушное пространство оставляется для вентиляции сети.
В коллекторах водоотведения над водой скапливаются пары воды и следующие газы: сероводород, аммиак, углекислый газ, метан, пары бензина и др. нефтепродуктов.
С производственными водами в коллекторы поступают углерод, аммиак, хлор и масса других веществ.
Количественный состав газов колеблется в широких пределах. Так метана - 1,5-15%, углекислого газа - 0,1-10%, сероводорода - 0,01-0,1% по объёму.
Смесь кислорода воздуха с водородистыми и метановыми газами может оказаться взрывоопасной. Вредные газы опасны для здоровья рабочих, обслуживающих водоотводящие сети.
Присутствие в стоках сероводорода, серной кислоты и углекислого газа создают условия для разрушения бетонных и железобетонных труб.
Источником сероводорода и других газов являются сточная жидкость и разлагающиеся органические вещества.
Процессы разложения органических соединений идут по следующим реакциям:
а) в присутствии свободного кислорода
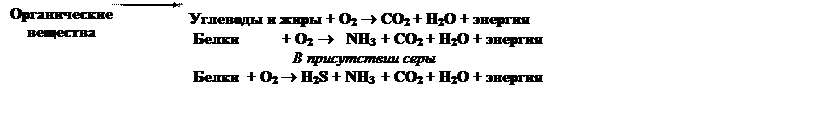
В случае отсутствия свободного кислорода анаэробные бактерии используют кислород, содержащийся в других соединениях, нитритах, сульфатах, углекислотах.
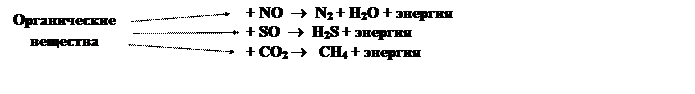
Из схем видно, какие газы могут находиться в атмосфере коллектора. Это CO2, H2S, NH3 (аммиак), СH4 (метан).
В стоках могут содержаться более 50 видов газов. Они могут иметь неприятный запах быть токсичными и агрессивными по отношению к материалу трубопроводов.
Наиболее агрессивным газом в городских коллекторах является сероводород. Этот газ - основная причина коррозии сводов коллекторов. На которую приходится 24% всех разрушений коллекторов.
На следующем рисунке представлены условия отсутствия газовой коррозии и условия, способствующие её появлению.
Рис. 75. Схема образования сероводорода в сточных водах в зависимости от содержания растворённого кислорода
На стенке трубы, погружённой в сточную воду, образуется биологическая плёнка. Толщина плёнки колеблется от 0,3 мм до 3 мм при больших и малых скоростях движения стоков соответственно. При нормальных скоростях - 1 мм.
Условия достаточного содержания кислорода
Растворённый кислород проникает внутрь плёнки и потребляется бактериями из её аэробного слоя. Это обстоятельство препятствует развитию бактерий в анаэробном слое (0,3 мм), продуцирующим сероводород. Непосредственно на стенке находится инертный анаэробный слой, бактерии которого не получают достаточно пищи для своего развития. В этих условиях образование сероводорода почти не происходит и поэтому трубы не разрушаются.
Условия недостаточного содержания кислорода
При недостаточном количестве кислорода в сточных водах (меньше 0,1 мг/л) процесс образования сероводорода интенсифицируется серобактериями.
Эти бактерии хорошо сопротивляются дизенфектантам, антибиотикам, размножаются при рН от 5 до 9,5 и температуре от 10 до 50 оС , не погибают при давлении до 105 кПа.
О содержании сероводорода в воде можно судить по количеству сульфидов растворённых (Н2S, HS-, S2-) и нерастворённых (FeS, ZnS), выпавших в осадок.
Выделяясь из воды, сероводород насыщает атмосферу коллектора и проникает в поры бетона на его стенах и сводах. В порах бетона размножаются тионовые бактерии, продуцирующие серную кислоту. Эти бактерии существуют при рН до 7,5. Их присутствие обнаруживали в очень кислой среде (рН меньше 1) при очень сильном разрушении труб.
В конденсате происходит биохимическое аэробное окисление сероводорода по следующим реакциям.
При избытке кислорода в воздухе:
2Н2S + 3O2 = 2SO2 + 2H2O.
При недостатке кислорода:
2Н2S + O2 = 2S + 2H2O.
Сера окисляется в сульфаты или серную кислоту:
2S + 3O2 + 2H2O = 2Н2SО4.
Основой бетонных и железобетонных труб является гидроксид кальция Са(ОН)2. Воздействие на бетон серной кислоты вызывает образование новых соединений кальция. Характерная черта этих соединений - резкое увеличение в объёме по сравнению с объёмом гидроксида кальция. Это обстоятельство приводит к разрушению бетона.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.