
Федеральное агентство по образованию Российской Федерации
Санкт-Петербургский государственный горный институт им. Г.В. Плеханова
(технический университет)

Кафедра ОТХ
Выполнили:
Студенты гр. ЭП-04:
/___________/ Тюрикова С.В.
/___________/ Синяков Д. В.
Проверил:
Ассистент каф. ОТХ:
Кужаева А.А.
Оценка: /________/
Подпись: /____________/
Санкт-Петербург
2005 год
Цель работы: определение теплового эффекта процесса нейтрализации кислоты щелочью.
Сущность работы: реакция нейтрализации любой сильной кислоты щелочью сопровождается экзотермическим тепловым эффектом. Для измерения тепловых эффектов реакций в растворах чаще всего применяют диатермические калориметры, для которых энтальпия калориметрической системы постоянна. Для определения теплового эффекта реакции достаточно знать теплоемкость системы и вызванное реакцией изменение температуры системы.
Серная кислота
Vщ = 20 мл; СKOH
=1 H; V![]() =300 мл;
С
=300 мл;
С![]() = 0,2 Н; VHg
= 3,5 мл;
= 0,2 Н; VHg
= 3,5 мл;
m = 344,7 г; mпипетки = 39,4 г; mпипетки с раствором = 59,5 г; mKOH = 20,1 г;
mстакана с раствором =545,3 г; mстакана = 245 г; mр-р= 300,4 г.
Таблица измерений:
|
|
Температура,°Б |
Время, с |
Температура,°Б |
Время, с |
Температура,°Б |
||
|
Начальный период |
Главный период |
Конечный период |
|||||
|
30 |
2,95 |
330 |
3,44 |
360 |
4,09 |
||
|
60 |
3,44 |
360 |
4,09 |
390 |
4,10 |
||
|
90 |
3,45 |
420 |
4,11 |
||||
|
120 |
3,45 |
450 |
4,12 |
||||
|
150 |
3,45 |
480 |
4,13 |
||||
|
180 |
3,45 |
510 |
4,14 |
||||
|
210 |
3,44 |
540 |
4,15 |
||||
|
240 |
3,44 |
570 |
4,15 |
||||
|
270 |
3,44 |
600 |
4,15 |
||||
|
300 |
3,44 |
630 |
4,15 |
||||
График:
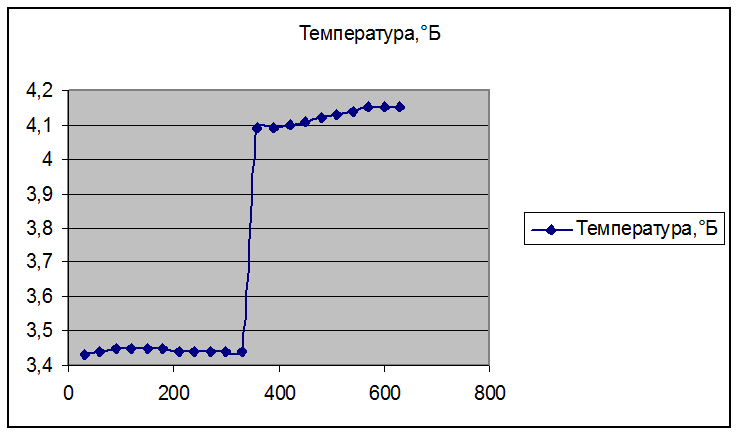
Теплоемкость калориметрической установки:
Сcal = Cр-р(mp-p + mKOH) + СHgVHg + Cстm, Дж/К,
где Cр-р – удельная теплоемкость раствора, 4,18 Дж/г×К; mp-p – масса раствора во внутреннем стакане, г; mKOH – масса раствора щелочи в пипетке, г; СHg – объемная теплоемкость ртути и стекла, 1,92 Дж/см3×К, VHg – объем баллона термометра, содержащего ртуть, мл; Cст – удельная теплоемкость стекла, 0,79 дж/г×К; m – общая масса стеклянных частей калориметрической установки, г.
Сcal =4,18·(300,4+20,1)+1,92·3,5+0,79·344,7=1618,7 (Дж/К)
Тепловой эффект процесса нейтрализации:
![]()
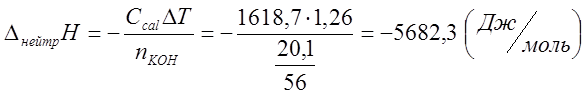
где nKOH – количество вещества щелочи в пипетке, моль.
Уксусная кислота
Vщ = 20 мл; СKOH
=1 H; V![]() =300 мл;
С
=300 мл;
С![]() = 0,2 Н; VHg
= 3,5 мл;
= 0,2 Н; VHg
= 3,5 мл;
m = 344,7 г; mпипетки = 39,4 г; mпипетки с раствором = 59,5 г; mKOH = 20,1 г;
mстакана с раствором =540,7,9 г; mстакана = 245 г; mр-р= 300,4 г.
|
|
Температура,°Б |
Время, с |
Температура,°Б |
Время, с |
Температура,°Б |
||
|
Начальный период |
Главный период |
Конечный период |
|||||
|
30 |
3,45 |
330 |
4,14 |
360 |
4,71 |
||
|
60 |
4,14 |
360 |
4,71 |
390 |
4,7 |
||
|
90 |
4,15 |
420 |
4,69 |
||||
|
120 |
4,15 |
450 |
4,69 |
||||
|
150 |
4,15 |
480 |
4,68 |
||||
|
180 |
4,15 |
510 |
4,67 |
||||
|
210 |
4,15 |
540 |
4,66 |
||||
|
240 |
4,14 |
570 |
4,66 |
||||
|
270 |
4,14 |
600 |
4,66 |
||||
|
300 |
4,14 |
630 |
4,66 |
||||
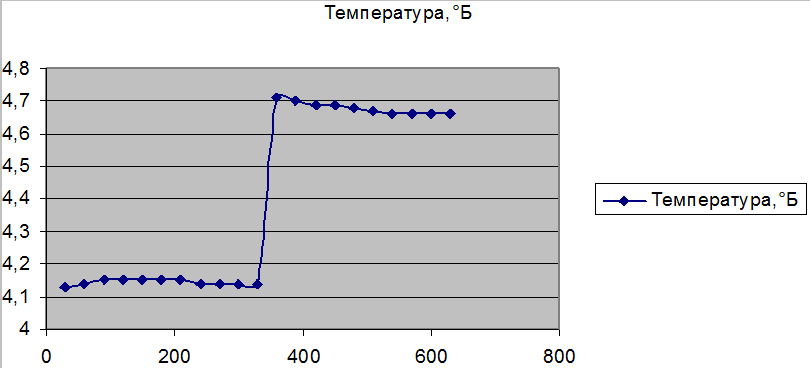
Теплоемкость калориметрической установки:
Сcal = Cр-р(mp-p + mKOH) + СHgVHg + Cстm, Дж/К,
где Cр-р – удельная теплоемкость раствора, 4,18 Дж/г×К; mp-p – масса раствора во внутреннем стакане, г; mKOH – масса раствора щелочи в пипетке, г; СHg – объемная теплоемкость ртути и стекла, 1,92 Дж/см3×К, VHg – объем баллона термометра, содержащего ртуть, мл; Cст – удельная теплоемкость стекла, 0,79 дж/г×К; m – общая масса стеклянных частей калориметрической установки, г.
Сcal =4,18·(300,4+20,1)+1,92·3,5+0,79·344,7=1618,7 (Дж/К)
Тепловой эффект процесса нейтрализации:
![]()

где nKOH – количество вещества щелочи в пипетке, моль.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.