Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Российской Федерации
Санкт-Петербургский государственный горный институт им. Г.В. Плеханова
(технический университет)
Автор: студенты гр. АПМ-02 _____________ /Руссович К.А./
/Ярыгина Ю.Н./
/Михайлова А.С./
(подпись) (Ф.И.О.)
Руководитель проекта __доцент ____________ /Смирнов Ю.М./
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
2005 год
Цель работы: исследовать кинетику окисления Fe(II) до Fe(III) диоксидом марганца (пиролюзитом) и осаждение Fe(III) гидролизом при использовании в качестве нейтрализатора серной кислоты для повышения pH пульпы цинкового огарка.
Краткие теоретические сведения:
Гидролитическая очистка растворов сульфата цинка от примесей основана на различии pH гидратообразования цинка и металлов-примесей, находящихся в растворе. Этим способом в осадок могут быт переведены примеси, имеющие более низкие равновесные величины pH гидратообразования, чем цинк, т.е. железо трёхвалентное, алюминий, хром, частично медь. Железо двухвалентное имеет более высокие равновесные значения pH гидратообразования, чем цинк, поэтому оно не будет гидролизоваться при нейтральном выщелачивании цинкового огарка. Поскольку а растворах, получаемых в кислом цикле выщелачивания цинкового огарка и направляемых в нейтральный цикл, железо частично находится в форме FeSO4, то для обеспечения возможности очистки растворов от железа гидролитическим путем необходимо окислить двухвалентное железо до трехвалентного.
Окисление железа можно провести кислородом воздуха или пиролюзитом. Окисление железа пиролюзитом идет в кислой среде по реакции:
2FeSO4+MnO2+2H2SO4=Fe2(SO4)3+MnSO4+2H2O (1)
В обоих случаях скорость процесса увеличивается с повышением температуры.
Гидролиз сульфата трехвалентного железа сопровождается выделением свободной серной кислоты:
Fe2(SO4)3+6H2O↔2Fe(OH)3↓+3H2SO4 (2)
Для более полного протекания гидролиза необходимо удалять серную кислоту, что обеспечивается взаимодействием ее с оксидом цинка по реакции:
H2SO4+ZnO=ZnSO4+H2O (3)
Чтобы процесс гидролиза и очистки раствора от примесей при нейтральном выщелачивании протекал успешно, необходимо иметь в твердой части пульпы избыток оксида цинка.
Порядок выполнения работы:
Изучение процесса окисления сульфата двухвалентного железа пиролюзитом проводят в стакане ёмкостью 0,5 л при перемешивании раствора механической или магнитной мешалкой. Для проведения эксперимента готовят раствор сульфата двухвалентного железа заданной концентрации (3 г/л), используя его концентрированный раствор в воде. Раствор подкисляют до такой степени, чтобы количество серной кислоты было равно примерно 1,5-кратному от стехиометрически необходимого для окисления железа по реакции (1). Концентрацию Fe2+ и серной кислоты в приготовленном растворе проверяют титрованием. Зная объём раствора и содержание в нем Fe2+ , по реакции (1) рассчитывают теоретически необходимое количество MnO2. Для определения практически необходимого количества пиролюзита нужно учесть его активность и кратность расхода от теоретически необходимого.
Наладив перемешивание приготовленного раствора сульфата с достаточной скоростью, засыпают в него рассчитанное количество пиролюзита и отмечают время начала опыта. Контроль за ходом процесса ведут путем отбора проб через 5-10 мин, анализируя их на содержание Fe2+ по известной методике. Процесс ведут либо в течение заданного времени, либо до заданного содержания Fe2+ в растворе.
Исходные данные:
Vраствора=0,5 л
C(Fe2+)=3 г/л
C(H2SO4)=16 г/л
m(H2SO4)=16 г/л*0,5 л=8 г=8 мл
m(FeSO4*7H2O)= 4 г
Т(H2SO4) = 0,0049 г/мл
Т(Fe2+)=0,00559 г/мл
Определим содержание в исходном растворе Fe2+ и H2SO4 :
С(H2SO4)= VNaOHT103/A = (3,7*0,0049* 103)/1=18,3 г/л
С(Fe2+)= VKMnO4 T103/A = (0,2*0,00559* 103)/10=0,11 г/л
По реакции (1) рассчитали расход диоксида марганца:
X(MnO2)= 0,17 г/л
Результаты наблюдений и вычислений представлены в таблице:
|
Время от начала опыта, мин |
Концентрация в растворе, г/л |
|
|
H2SO4 |
Fe2+ |
|
|
10 |
9,8 |
0,28 |
|
20 |
13,7 |
0,22 |
|
30 |
6,37 |
0,45 |
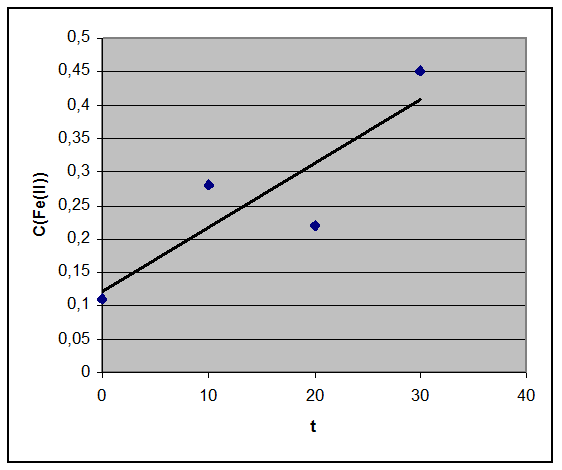
Построим график изменения С(Fe2+)=f(τ):
 |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.