




















Термодинамика
1. Внутренняя энергия................................................................. 2
2. Первое начало термодинамики............................................... 2
3. Работа газа при изменении его объёма.................................. 3
4. Теплоёмкость идеального газа. Уравнение Майера.............. 4
5. Адиабатический процесс. Уравнение адиабаты.................... 7
6. Работа, теплота и внутренняя энергия при изопроцессах и адиабатическом процессе......................................................... 9
7. Макро и микросостояния...................................................... 10
8. Энтропия................................................................................. 12
9. Круговые процессы................................................................ 17
10. Тепловые двигатели. Цикл Карно и его КПД для идеального газа....................................................................... 18
11. Второе начало термодинамики........................................... 18
12. Реальный газ......................................................................... 19
13. Изотермы Ван-дер-Ваальса и их анализ............................. 20
14. Внутренняя энергия реального газа................................... 22
1. Внутренняя энергия.
Внутренняя энергия – это кинетическая энергия хаотического движения частиц и потенциальная энергия их взаимодействия.
Во внутреннюю энергию не входят кинетическая энергия движения системы как целого и потенциальная энергия частиц во внешних полях.
Если рассматривать идеальный газ, где нет взаимодействия между частицами (т.е. нет притяжения и отталкивания), то во внутреннюю энергию входит только кинетическая энергия теплового хаотического движения.
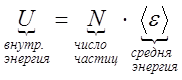
![]()
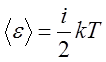 (
(![]() - число степеней свободы)
- число степеней свободы)
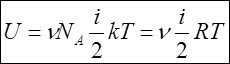
Внутренняя энергия является функцией состояния. Это
означает, что внутренняя энергия определяется только параметрами данного
состояния. При переходе из первого состояния во второе: ![]() ,
и
,
и ![]() не зависит от способа перехода из первого
состояния во второе.
не зависит от способа перехода из первого
состояния во второе.
 Если процесс совершается по кругу, т.е.
система переходит в начальное состояние, то
Если процесс совершается по кругу, т.е.
система переходит в начальное состояние, то ![]() .
.
![]()
Если ![]() , то
, то ![]() является полным дифференциалом.
является полным дифференциалом.
2. Первое начало термодинамики.
Внутренняя энергия может изменятся в основном за счёт двух процессов: за счёт работы, совершаемой над системой, и за счёт сообщения системе некоторого количества теплоты.
Например, работа изменяется при движении поршня, когда внешние силы совершают работу над газом, при этом увеличивается его температура, т.е. увеличивается и внутренняя энергия.
Или, например, за счёт сообщения количества теплоты, можно увеличить внутреннюю энергию. Изменение внутренней энергии при этом обусловлено тем, что при столкновениях молекул более нагретого тела с молекулами менее нагретого, первые передают последним часть своей энергии. В результате увеличивается кинетическая энергия, а значит и температура.
Изменение внутренней энергии может происходить также за счёт излучения.
Совокупность микропроцессов, которые приводят к
передаче энергии от одного тела к другому, называется теплопередачей.
Количество энергии, переданное от одного тела к другому в результате
теплопередачи, называется количеством теплоты ![]() .
.
Опыт показывает, что изменение внутренней энергии, независимо от способа перехода из одного состояния в другое, обусловлено количеством теплоты, сообщенным системе, и работой, совершённой над системой внешними силами.
Количество теплоты считается положительным, если оно сообщается системе, и отрицательным, если отнимается.
Работа считается положительной, если она совершается над внешними силами (газ расширяется), и отрицательной, если она совершается внешними силами над системой.
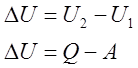
Количество теплоты, сообщённое системе идёт на изменение её внутренней энергии и на работу против внешних сил.
![]()
![]() означает, что
означает, что ![]() является полным дифференциалом (
является полным дифференциалом (![]() ).
).
![]() означает, что
означает, что ![]() и
и ![]() не
являются полными дифференциалами.
не
являются полными дифференциалами.
Первое начало термодинамики:
Если совершается
круговой процесс, то ![]() , и тогда
, и тогда ![]() .
Это показывает, что вечный двигатель первого рода (т.е. периодически
действующий двигатель) не может существовать, поскольку работа никогда не может
быть больше количества теплоты, сообщённого системе.
.
Это показывает, что вечный двигатель первого рода (т.е. периодически
действующий двигатель) не может существовать, поскольку работа никогда не может
быть больше количества теплоты, сообщённого системе.
3. Работа газа при изменении его объёма.

![]() - очень
маленький
- очень
маленький
![]() при
при ![]()
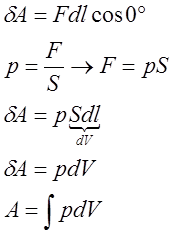 (
(![]() - изменение объёма)
- изменение объёма)
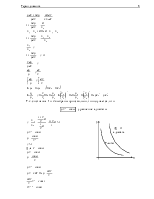
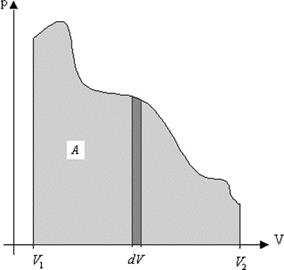 Работа газа численно равна
площади под графиком
Работа газа численно равна
площади под графиком ![]() .
.
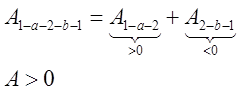
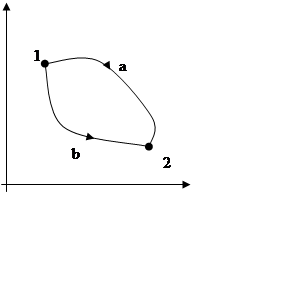
Тогда полная работа численно равна площади,
охватываемой контуром. Если ![]() в ходе цикла и цикл
проходит по часовой стрелке, то цикл – прямой. Если
в ходе цикла и цикл
проходит по часовой стрелке, то цикл – прямой. Если ![]() и цикл
проходит против часовой стрелки, то цикл – обратный.
и цикл
проходит против часовой стрелки, то цикл – обратный.
4. Теплоёмкость идеального газа. Уравнение Майера.
Молярная теплоёмкость ![]() - это
количество теплоты, сообщаемой 1 молю вещества, чтобы нагреть его на
- это
количество теплоты, сообщаемой 1 молю вещества, чтобы нагреть его на ![]() .
.
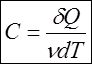
Удельная теплоёмкость ![]() - это
количество теплоты, сообщаемой 1 кг вещества, чтобы нагреть его на
- это
количество теплоты, сообщаемой 1 кг вещества, чтобы нагреть его на ![]() .
.
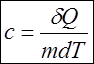
Связь между молярной и удельной теплоёмкостями:
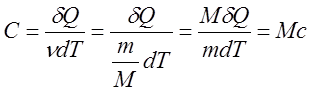
Теплоёмкость при постоянном объёме.
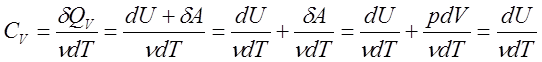 , т.к.
, т.к. ![]()
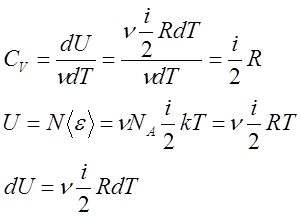
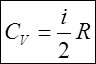
Число степеней свободы – это число независимых переменных, с помощью которых можно задать положение молекулы.
1. Одноатомные молекулы.

2. Двухатомные молекулы.

3. Трёхатомные молекулы.
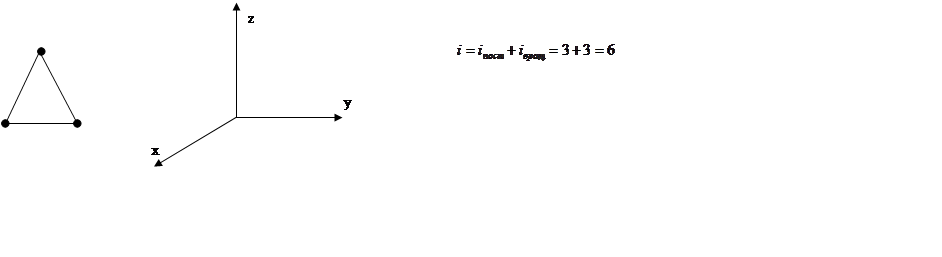
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.