7 Коэффициент пропорциональности k, выражающей зависимость массы выделенного при электролизе вещества от его рода, называют электрохимическим эквивалентом вещества.
8 Электрохимические эквиваленты различных веществ прямо пропорциональны их химическим эквивалентам.
9 Элемент Вольта: слабый раствор серной кислоты в воде, в который опущены медная и цинковая пластины. Элемент Лекланше: цинковая пластина (анод), графитовый стержень (катод), раствор нашатыря в воде (электролит), двуокись марганца HnO2 (деполяризатор).
10 Пропускание тока через аккумулятор, называют его зарядкой.
11 Емкостью аккумулятора называют максимальное количество электричества, которое может пройти по цепи за время разрядки полностью заряженного аккумулятора.
Электрический ток в электролитах
Вариант 1
1 С помощью ионов разных знаков происходит перенос электрических зарядов в электролите.
2 Рекомбинация ионов – процесс восстановления ионов в нейтральные молекулы.
3 Зависит т.к. диссоциация – это проникновение одного вещества в другое. Чем выше температура, тем больше скорость молекул, следовательно, и диссоциация происходит быстрее.
4 m = kq = kIt – первый закон Фарадея
5 q = 1K и m = kq → m = k
6
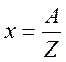 ,
химический эквивалент
,
химический эквивалент
А – атомная масса вещества
у многовалентного вещества x<A
7 Молярная масса вещества равна отношению его массы к количеству вещества, т.е. это масса 1 моль вещества.
8 q = Ze Z=1 q=e
Вариант 2
1 Молекулы воды обволакивают ионы, а это затрудняет рекомбинацию ионов, затрудняется движение ионов, следовательно, диссоциация.
2 Скорость движения зависит от температуры.
3 Положительно заряженные ионы движутся к отрицательному электроду (катоду), отрицательные ионы к положительному электроду (аноду).
4
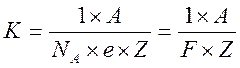 ,
второй закон Фарадея.
,
второй закон Фарадея.
5 Химический эквивалент – отношение атомной массы вещества к его валентности (A/Z).
6
7 F = 9,6485×104 Кл/моль – число Фарадея
8
Z = 2
1моль m = A
Электрический ток в газах
Вариант 1
1 Плазмой называют вещество в таком состоянии, когда оно в целом электрически нейтрально, но содержит равные количества свободных положительных и отрицательных зарядов.
2 Электрический ток , который возникает при несамостоятельном разряде, называют несамостоятельным.
3 Разряд в газе, который происходит только при действии постороннего ионизатора, называется несамостоятельным.
4 Дуговым называется разряд, в газе происходящий при раскаленном катоде или при высоком напряжении между электродами.
5
Высокая температура,
рентгеновское, ультрафиолетовое, α – излучение и т.д. ![]()
6 Потенциал φu называют потенциалом ионизации атома или молекулы. Его величина зависит от рода атомов и молекул.
7
Простейшая лампа с двумя
электродами называется диодом. Устройство: 1) вольфрамовая проволочка, концы
которой выведены из лампы (катод);
2) вторая проволока – анод. Внутри лампы высокий вакуум.
Вариант 2
1 Образование нейтральных молекул из ионов газа называется рекомбинацией.
2 Такой ток в газе, значение которого не зависит от напряжения , называют током насыщения.
3 Разряд в разряженном газе, сопровождающийся свечением, называют тлеющим.
4 Коронный разряд возникает около проводов, находящихся под высоким напряжением, находящихся под высоким напряжением. Он сопровождается слабым свечением и характерным треском, при этом происходит утечка передаваемой энергии.
5 График зависимости силы тока в газе от напряжения называется вольтамперной характеристикой.
6 Пучок электронов, летящих прямолинейно от катода при высоком вакууме в трубке, называют катодными лучами.
7 Электронную лампу с сеткой называют триодом. Устройство: анод, катод, сетка, внутри лампы высокий вакуум.
Электрический ток в газах
Вариант 1
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.