Ионогенные Неионогенные
способные к диссоциации не способные
в условиях организма
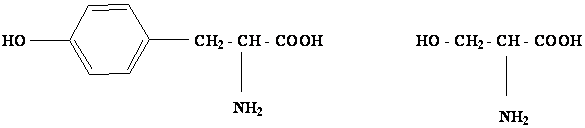
тирозин серин
Полярные аминокислоты с ионогенными группами в условиях организма могут находиться в виде анионов и катионов
В виде анионов В виде катионов
Асп Лиз
Глу Арг
Цис
Полярные ионогенные радикалы располагаются как на поверхности, так и внутри белковых молекул. Они участвуют в образовании водородных связей с другими полярными группами.
Все α-аминокислоты, за исключением глицина, имеют асимметрический атом углерода и существуют в виде энантиомеров, относящихся к D- и L-рядам. В белках животных организмов представлены L-аминокислоты, в белках микроорганизмов встречаются и аминокислоты D-ряда. D-аминокислоты животным организмом не усваиваются.

L-аланин L-треонин L-изолейцин
Три аминокислоты имеют два центра хиральностти: треонин, изолейцин, 4-гидроксипролин.
15.2. БИОСИНТЕТИЧЕСКИЕ ПУТИ ОБРАЗОВАНИЯ АМИНОКИСЛОТ
Биосинтез α-аминокислот осуществляется из α-кетокислот -
продуктов метаболизма углеводов. Возможны два пути превращения кетокислот в аминокислоты
1) Восстановительное аминирование с участием кофермента НАД-Н
О NH2
║ НАД-Н │
НООС – СН2 – СН2 – С – СООН → НООС – СН2 – СН2 – СH – СООН
α-кетоглутаровая кислота глутаминовая кислота
2) Трансаминирование (переаминирование), источником группы NH2 для кетокислот является другая аминокислота. Эта реакция протекает при участии кофермента пиридоксальфосфата
R–CH–COOH + HOOC-CH2-C-COOH→ R–C–COOH + HOOC-CH2-CH-COOH
│ ║ ║ │
NH2 О O NH2
Щавелевоуксусная кислота Аспарагиновая
Кислота
15.3. ХИМИЧЕСКИЕ СВОЙСТВА
Аминокислоты являются амфотерными органическими соединениями, поэтому в растворах существуют в виде биполярных ионов
Н3+N – СН – СОО-
R
Аминокислотам присущи все свойства как карбоновых кислот, так и аминов.
Реакции карбоксильной группы - образование функциональных производных кислот (сложных эфиров, амидов, солей,галогенангидридов).
Реакции аминогруппы - образование солей с сильными кислотами, образование N-ацилированных производных.
Кроме того для аминокислот характерен целый ряд специфических реакций, обусловленных наличием в их структуре COOH- и NH2- групп у одного и того же атома углерода. Рассмотрим реакции, протекающие в организме. Все эти реакции - ферментативные, хотя некоторые из них могут быть осуществлены in vitro.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.