1
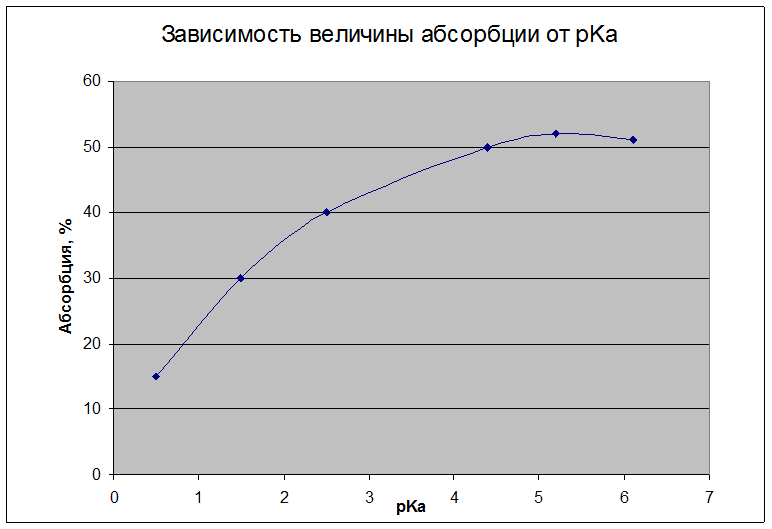
Из полученного графика зависимости величины абсорбции от pKa видно, что абсорбция всех токсикантов идет в ощутимых количествах. Значит во всех случаях должны преобладать нейтральные формы молекул токсикантов.
pH среды = const = 1.5 – 2.5
Формула Гендельсона-Гассельбаха связывает показатели pH и pKa.
pH-pKa=lg[A-]/[HA] (для кислот)
pH-pKa=lg[B]/[BH+] (для оснований)
1) 15% абсорбция, pKa=0,5
Предположим, что природа токсиканта №1 кислая, тогда верна формула для кислот
pH-pKa=lg[A-]/[HA] = 1,5(2,5) – 0.5 = 1 - 2 => [HA]/[A-] = 0.1-0.01, что не удовлетворяет нашему условию о том что в желудке преобладает нейтральная форма токсиканта.
Предположим, что природа токсиканта №1 основная, тогда верна формула для оснований pH-pKa=lg[B]/[BH+] = 1,5(2,5) – 0,5 = 1 – 2 => [B]/[BH+] = 10 - 100, что удовлетворяет нашему условию о том, что в желудке преобладает нейтральная форма токсиканта.
Значит сделанное нами предположение верное.
Природа токсиканта N1 – основная
2) 30% абсорбция, pKa=1,5
Предположим, что природа токсиканта №2 кислая, тогда верна формула для кислот
pH-pKa=lg[A-]/[HA] = 1,5(2,5) – 1,5 = 0 – 1 => [HA]/[A-] = 1- 0,1, что не удовлетворяет нашему условию о том что в желудке преобладает нейтральная форма токсиканта.
Значит сделанное нами предположение не верное.
Предположим, что природа токсиканта №2 основная, тогда верна формула для оснований pH-pKa=lg[B]/[BH+] = 1,5(2,5) – 1,5 = 0 – 1 => [B]/[BH+] = 1- 10, что удовлетворяет нашему условию о том, что в желудке преобладает нейтральная форма токсиканта.
Значит сделанное нами предположение верное
Природа токсиканта N2 – основная
3) 40% абсорбция, pKa=2,5
Предположим, что природа токсиканта №3 кислая, тогда верна формула для кислот
pH-pKa=lg[A-]/[HA] = 1,5(2,5) – 2,5 = -1 – 0 => [HA]/[A-] = 10- 1, что удовлетворяет нашему условию о том что в желудке преобладает нейтральная форма токсиканта.
Значит сделанное нами предположение верное
Природа токсиканта N3 – кислая
По аналогии, природа токсикантовN4 и N5 – кислые
Ответ – 1.природа токсикантов N1 и N2 – основные
2. природа токсикантов N3 - N5 – кислые
2
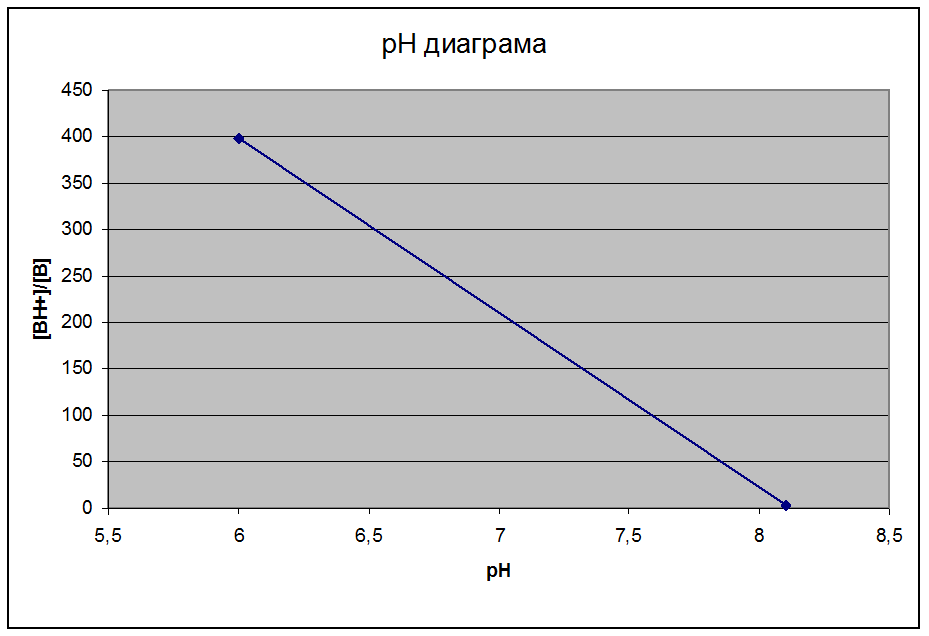
pH-pKa=lg[B]/[BH+] (для оснований)
pH кишечника – 6 – 8,1 ; pKa = 8.6
1) 6 – 8,6 = lg[B]/[BH+] = -2,6 => BH+/B = 102.6 = 398 преобладает катионная форма
2) 8,1 – 8,6 = lg[B]/[BH+] = -0,5 => BH+/B = 100,5 = 3,2 преобладает катионная форма
Ответ - во всем диапозоне pH преобладает С) катионная форма токсиканта
3
Vp = ОСО / С, - объем распределения
где ОСО - общее содержание вещества в организме,
С - его сывороточная концентрация.
OCO = 750мг
Vp(15кг) = 2л/кг *15 кг = 30л
С = ОСО / Vp = 750мг / 30л = 25мг/л
Ответ – максимальная концентрация принятого яда = 25мг/л
4
Элиминация этанола происходит по кинетике нулевого порядка. Это означает, что скорость элиминации одинакова (не зависит от концентрации этанола).
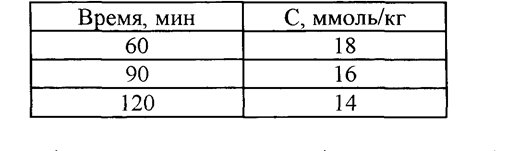
Из таблицы видно, что за 30мин концентрация этанола уменьшается на 2ммоль/кг.
Со(нач концентрация этанола)= (60мин/30мин)*2ммоль/кг + 18ммоль/кг=22ммоль/кг, тогда при t1/2 C=11ммоль/кг =>
t1/2 = [(22ммоль/кг-11ммоль/кг) / 2ммоль/кг]*30мин = 165мин
Ответ – период полувыведения этанола = 165мин
5
Vd = 2л/кг
t1/2 = 2-4часа
t1/2 = ln2/KE
Cl = KЕ*Vd = ln2 * Vd / t1/2 = 0,693* 2 /(2 - 4) = (0,693 – 0.3465)л/(кг*ч)
Ответ: клиренс пиндолола – 0,693 – 0,3465л/(кг*ч)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.