Кинетика
1. Основные понятия и определения химической кинетики
А) скоростью химической реакции называют
V= 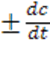
Б) закон действующих масс:
V= K[![]()
Физический смысл: К скорости при [А][В][С]=1 м/л равна V реакции
V=К скорости
2. Кинетическая классификация гомологических химических реакций
А) n=1 A→ продукты V= K [A]
Б) n=2 2A→продукты V= K[![]()
![]() +
+![]() V= K[
V= K[![]() ][
][![]() ]
]
В) n=3 3A→ продукты V= K[![]()
![]() +
+![]() +
+![]() → продукты V= K[
→ продукты V= K[![]() ][
][![]() ][
][![]() ]
]
3. Для характеристики кинетических уравнений пользуются:
К скорости;![]() время полупр-я – время за которое прор-т половина исх-й
к-ии.
время полупр-я – время за которое прор-т половина исх-й
к-ии. 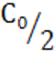
Способы определения n:
1.
n можно рассчитать по 1-в-ву,
посмотрев график ![]() от ln
от ln
2.
n= tg ![]() + tg
+ tg![]()
![]() =
=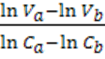 ;
;
![]() n
n
3. Способ подстановки: если расчетные значения К по одной из формул = const для разных моментов времени, то эта формула для экспериментального изучения реакции.
4.
![]()
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.