ЛАБОРАТОРНА РОБОТА 4
ВЛАСТИВОСТІ КОЛОЇДНИХ РОЗЧИНІВ
Мета: вивчення коагуляції золів електролітами; коагулюючу дію іонів; визначення порогу коагуляції; коагуляція сумішшю електролітів; залежність швидкості коагуляції від концентрації електроліту; взаємна коагуляція золів. Перевірка справедливості правила Шульца-Гарді.
Короткі теоретичні положення
Ліофобні золі дуже чутливі до впливу електролітів. Золі втрачають свою стійкість і руйнуються при додаванні навіть невеликих кількостей їх. Мінімальна концентрація електроліту, що призводить до коагуляції колоїду за певний проміжок часу, називається його порогом коагуляції (ПК). Коагулюючу дію на золь надають іони, що мають заряд протилежний заряду колоїдної частинки. Вона тим вище, чим більше заряд іону - коагулятора. При цьому виконується правило значності. Руйнування колоїдів може спостерігатися при змішуванні двох золів, що мають протилежні заряди гранул. У таких випадках повна коагуляція настає, коли загальний заряд частинок одного колоїду точно відповідає протилежному заряду іншого. В іншому випадку утворюється новий золь, частинки якого несуть заряд того з колоїдів, чий заряд опинився в надлишку. Стійкість колоїду до впливу електролітів можна підвищити додаванням до нього ПАР або ВМС, що змінюють поверхневі властивості колоїдних часток. При цьому поверхня частинок стає гідрофільною, і золь набуває додаткової стабільністі. Ступінь захисної дії речовини залежить від природи речовини, і природи золю і характеризується відповідним числом. Колоїдні частинки золю отриманого гідролізом FeCl3, заряджені позитивно:
{[mFe (OH)3] • nFe3 + (3-x)n Cl-} x +, тому коагулюючу дію мають аніони електроліту - коагулянту. Згідно з правилом Шульце-Гарді ПК золю електролітом (Ск) обернено пропорційний заряду коагулюючого іону (Z) у шостому ступені:
Ск = K/Z6,
де К - const для даного золю величина.
ДОСЛІД 1 ВИЗНАЧЕННЯ ПОРОГУ КОАГУЛЯЦІЇ ЗОЛЮ ГІДРОКСИДУ ЗАЛІЗА Fе(OH) 3 ЕЛЕКТРОЛІТАМИ КС1, K2SO4, K3 [Fе (CN) 6]
Необхідні реактиви, посуд та обладнання: електроплитка; склянку на 150 см3; конічні колби на 100 см3 - 3 шт.; Піпетка або бюретка - 3 шт.; Циліндр на 5-10 см3; розчини FeCl3 2%; КС1 (2 моль/дм3 ); K2SO4 (0,05 моль / дм 3); K3 [Fe (CN) 6] (0,005 моль/дм3)
Методика виконання роботи
1. Приготуйте для досліджень гідрозолі Fe(OH)3. Для цього в 150 см3 киплячої дистильованої води влийте тонкою цівкою 6 см3 2%-ного розчину FeCl3.
2. Золь охолодіть до кімнатної температури.
3. У 3 сухі конічні колби на 100 см3 внесіть по 35 см3 гідрозолю Fe (OH) 3.
4. Три бюретки заповніть розчинами електролітів-коагулянтів:
першу - КС1 (2М), другу - K2SO4 (0,05 М) і третю - K3 [Fe (CN) 6] (0,005 М).
5. У кожну колбу з золем (по черзі) додайте із бюретки по краплях розчини досліджуваних електролітів до появи перших ознак коагуляції. Початок коагуляції, тобто зміну числа частинок, можна точно спостерігати тільки за допомогою ультрамікроскопа. Неозброєним оком вдається помітити тільки початок явною коагуляції - поява муті.
6. Визначте кількість електроліту, з точністю до однієї краплі, яке було потрібно, щоб викликати коагуляцію золю (об’єм краплі ~ 0,05 см3).
7. Результати занесіть у табл. 1.
8. Поріг коагуляції Ск в ммоль/дм3 розрахуйте за формулою:
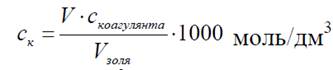
де V золю – об’єм золю, см3; С коагулянта - концентрація електроліту-коагулянту, моль/дм3; V - об'єм розчину електроліту, необхідний для коагуляції.
Таблиця 1 Коагуляція золю Fe (OH) 3 різними електролітами
|
Електроліт-коагулянт |
Концентрация електроліту- коагулянту |
Об’єм електроліту- коагулянту |
Порог коагуляції |
9. Напишіть молекулярне рівняння реакції одержання гідрозолі Fe (OH) 3.
________________________________________________________________________________________________________________________________________________________
10. Складіть іонні рівняння реакції, визначте знак заряду частинок золю і побудуйте формулу міцели.
________________________________________________________________________________________________________________________________________________________
11. Запишіть відповідні висновки.
________________________________________________________________________________________________________________________________________________________
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.