

Лекція № 1.1 Тема : Основи фізичної та колоїдної хімії. Розчини неелектролітів. Колегативні властивості
План
1. Загальна характеристика розчинів.
2. Способи вираження складу розчинів.
3. Характеристика розчинів неелектролітів. Закон Вант-Гоффа про осмотичний тиск.
4. Тиск пари розчинника над розчином. Діаграма стану води Перший закон Рауля
5. Температура замерзання та кипіння розчинів. Другий закон Рауля
Фізична хімія, це наука, що пояснює хімічні явища на основі фізичних принципів та законів.
Розчином називається гомогенна однорідна дисперсна система, що складається не менш чим із двох компонентів – розчинника і розчиненої речовини.
Розчинник по фазі збігається з розчином. Речовина, що розчиняється, може бути в будь-якій фазі (Г, Р, Т).
За агрегатним станом розчини бувають:
· рідкі (розчини солей у воді);
· тверді (різні сплави);
· газуваті (суміші газів, повітря
Масова частка речовини – це безрозмірна фізична величина, що дорівнює відношенню маси розчиненої речовини до загальної маси розчину:
mреч. × 100%
W = --------------------- , де
m розчину
Молярна концентрація (моль/л) – визначається відношенням кількості (моль) розчиненої речовини(n)до об’єму розчину (V) (л). См = n реч.: V розчину.
Моляльна концентрація (моль/кг) – визначається відношенням кількості (моль) розчиненої речовини(n)до маси розчинника (m) (кг). Сm = n реч.: m розчиника.
Мольна частка (Х) визначається відношенням моль розчиненої речовини до загальної суми моль розчинника та розчиненої речовини
X = n1/n1+n2
де n1- моль розчиненої речовини n2 – кількість моль розчинника
3. Властивості розведених розчинів неелектролітів
Неелектроліти – це речовини, розчини яких не проводять електричний струм. Якщо розчини розведені (концентрація розчиненої речовини мала), то їх можна розглядати як механічні суміші, тобто не враховувати слабку взаємодію між компонентами (сили міжмолекулярної взаємодії). Кожен компонент поводиться незалежно і властивості розчину визначаються тільки концентрацією розчиненої речовини.
Осмотичний тиск. Закон Вант-Гоффа про осмотичний тиск.
Осмотичний тиск – це тиск який чинила б розчинена речовина, якщо б вона при тих самих умовах перебувала в газоподібному стані і займала об’єм рідини. Осмотичний тиск можна визначити за формулою :
Росм = СмRT
См – молярна концентрація розчиненої речовини
R – універсальна газова стала
T – температура (К)
4. Тиск пари розчинника над розчином.
При даній температурі тиск насиченої пари над будь-якою рідиною – величина постійна (наприклад, таблиці пружності водяної пари).


![]()
 |
|||
 |
|||
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Рис.5. Залежність тиску насиченої пари розчину від температури.
При t°= 0°С р0 (Н2О) = 4,6 мм рт ст (чи 613 Па)
10°С р0 (Н2О) = 9,2 мм рт ст
100°С р0 (Н2О) = 760 мм рт ст (чи 101325 Па)
При розчиненні в рідині нелетучої речовини тиск насиченої пари розчинника зменшується, тому що знижується частка молекул розчинника як у всьому об’ємі, так і на поверхні поділу фаз. Таким чином, тиск насиченої пари розчинника над розчином завжди менше, ніж над чистим розчинником.
Закон Рауля: відносне зниження тиску насиченої пари розчинника над розчином дорівнює молярній (мольній) частці розчиненої речовини.
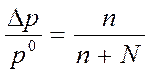 |
р - тиск пари розчинника над розчином,
Dр = р0 – р зниження тиску насиченої пари розчинника ,
n - число молів розчиненої речовини,
N - число молів розчинника.
Зниження тиску пари над розчином знаходить своє відображення на діаграмі стану. Розглянемо діаграму стану води і розчину нелетучого компонента Відповідно до закону Рауля при будь-якій температурі тиск водяної пари над водяним розчином нижче, ніж над водою. Тому крива фазового переходу від рідкого стану до пари для розчину розташована нижче, ніж для чистої води. Аналогічно змінюється положення кривої плавлення. Обидві криві для розчину будуть розташовуватися тим далі від відповідних криві води, чим більше концентрація розчину.


![]() Н2О розчин
Н2О розчин
Пар
![]()
![]()
![]() 101,3
кПа
101,3
кПа
Рідина
![]()
![]()
![]()
![]()
![]() Т
Т
100 t кіп. розчину
Температури фазових переходів ( кипіння чи плавління (замерзання)).
5. Індивідуальні речовини характеризуються строго визначеними температурами переходу одного агрегатного стану в інше (температура кипіння чи плавлення (замерзання)). Для води при нормальному тиску 101,3 кПа - це 100С и 0С.
Інакше обстоїть справа з розчинами. У більшості випадків кристалізується (при замерзанні) і википає (при кипінні) тільки розчинник. Будь-яка рідина закипає, коли тиск насиченої пари її стає рівним атмосферному тиску. Замерзає розчин тоді, коли тиск насиченої пари його стає рівним тиску насиченої пари твердого розчинника. Присутність розчиненої речовини знижує температуру замерзання і підвищує температуру кипіння (як це видно з діаграми стану).
Другий закон Рауля: підвищення температури кипіння і зниження температури замерзання
розведених розчинів неелектролітів пропорційні моляльній
концентрації розчиненої речовини і не залежать від природи речовини.
DТкип = Е × сm Тк = Е * Сm
DTзам = К × сm , де сm – моляльна концентрація розчиненої речовини
[моль/кг розчинника],
E, K – ебуліоскопічна и кріоскопічна константи,
Таким чином, суть законів Рауля зводяться до наступного ствердження:
зниження тиску пари розчинника, підвищення температури кипіння і зниження температури замерзання обумовлені тільки числом розчинених часток у визначеній кількості даного розчинника і не залежать від природи розчиненої речовини.
Закони Рауля в хімії використовують для визначення молекулярних мас синтезованих речовин.
2. Термінологічний словник
Розчини – це однорідні (гомогенні) системи, що складаються з двох і більше компонентів (складових частин) і продуктів їх взаємодії.
Розчинність– маса речовини (г), що може бути розчинена в 100 г розчинника при даній температурі до одержання насиченого розчину.
Сольвати – нестійкі сполуки частинок речовини з молекулами розчинника
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.